Clear Sky Science · nl
Pre-assemblage van biomoleculaire condensaatzaden drijft RSV-replicatie
Hoe sommige virusdeeltjes een voorsprong krijgen
Respiratoir syncytieel virus (RSV) is een belangrijke oorzaak van longinfecties bij zuigelingen, oudere volwassenen en mensen met een verzwakt immuunsysteem. Deze studie stelt een schijnbaar eenvoudige vraag met grote implicaties: wanneer een enkel RSV-deeltje op een cel landt, wat bepaalt dan of die infectie doorzet of stilletjes afsterft? Door individuele virale genomen in levende cellen te volgen, onthullen de auteurs verborgen verschillen tussen virusdeeltjes die verklaren waarom sommige infecties exploderen terwijl andere uitdoven.
Verborgen virale druppels in geïnfecteerde cellen
Eens binnen een cel bouwen veel RNA-virussen, waaronder RSV, kleine, membraanvrije “virale fabrieken”. Deze druppelachtige structuren concentreren virale componenten en zijn de belangrijkste locaties waar nieuwe virale genomen en eiwitten worden gemaakt. Er is echter een probleem: zulke druppels vormen zich meestal pas wanneer de eiwitniveaus al hoog zijn, terwijl virale eiwitten vroeg in de infectie schaars zijn. Met geavanceerde fluorescentiemicroscopie volgden de onderzoekers enkele RSV-genoomcomplexen, vRNPs genoemd, vanaf het moment dat ze de cellen binnengingen. Ze ontdekten dat virale fabrieken niet uit het niets verschijnen; in plaats daarvan groeien ze voort uit individuele binnenkomende vRNPs die geleidelijk opzwellen en samenvoegen tot grotere druppels.
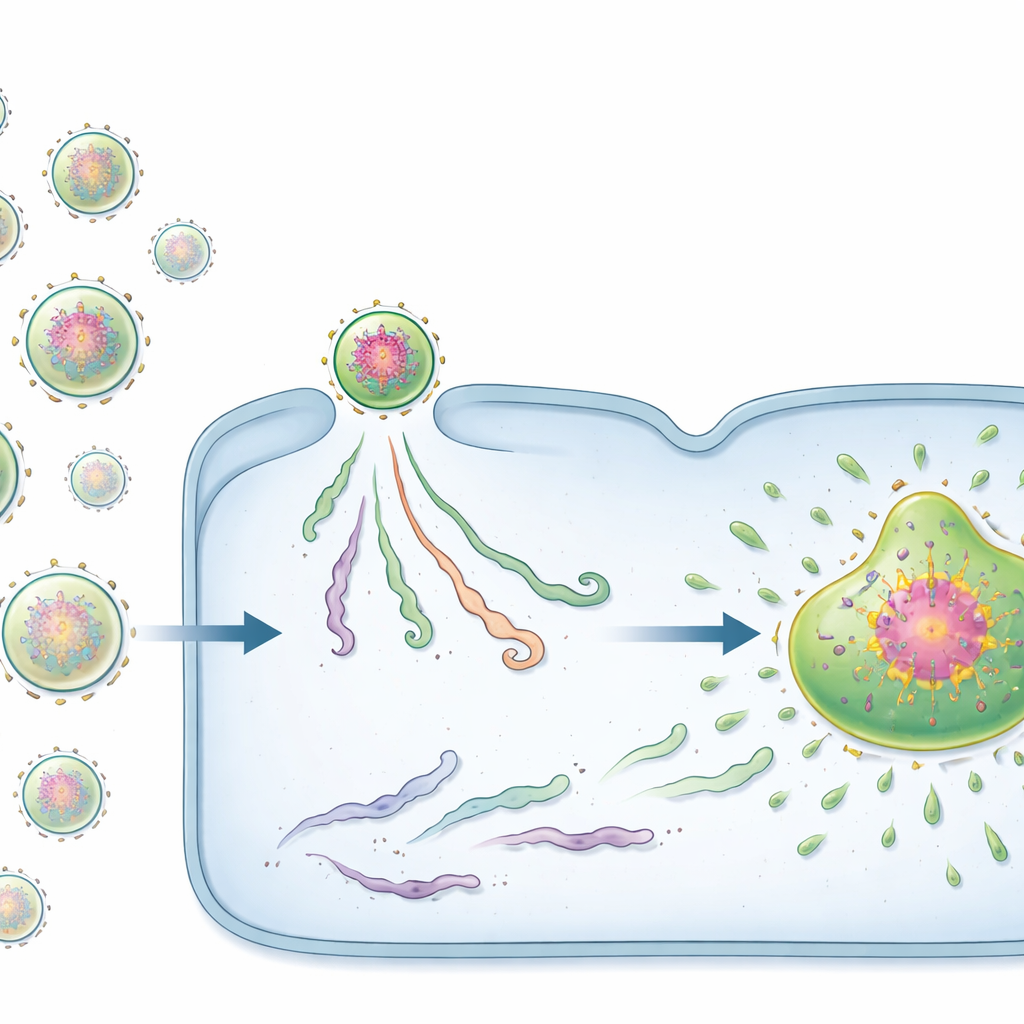
Twee soorten virale starters: zaden en passagiers
Verrassend genoeg gedroegen niet alle binnenkomende vRNPs zich hetzelfde. Met speciaal ontworpen fluorescerende probes ontdekte het team twee afzonderlijke toestanden. Een minderheid van vRNPs droeg al dichte clusters van virale eiwitten rond het genoom. Deze eiwitrijke complexen, die de auteurs pre-replicatiecentra (PRC’s) noemen, fungeerden als krachtige “zaden” voor virale fabrieken. Cellen die besmet werden door zelfs één enkele PRC vormden bijna altijd een fabriek en produceerden grote aantallen nakomend genoom. Daartegenover stonden de meeste vRNPs, die dit vooraf geladen eiwitnetwerk misten en passieve vRNPs werden genoemd. Infecties gestart door passieve vRNPs stokten vaak: het virale materiaal bleef klein en geïsoleerd, en er verscheen geen virale fabriek of nakomend genoom.
Waarom zaden slagen waar passagiers falen
Door virale activiteit in realtime te meten, toonden de auteurs aan dat PRC’s snel beginnen met het transcriberen van virale genen en dat dit veel sneller gebeurt dan bij passieve vRNPs. Gedetailleerde beeldvorming en biochemische analyses onthulden waarom. PRC’s dragen aanzienlijk meer kopieën van sleutelvirale eiwitten—vooral de polymerase en zijn co-factor—per genoom dan passieve vRNPs, al voordat ze de cel binnengaan. Eenmaal in het cytoplasma blijven deze eiwitten gebonden aan PRC’s, maar laten ze los bij passieve vRNPs. PRC’s functioneren ook als kleverige steigers die extra virale eiwitten en zelfs andere vRNPs aantrekken. Naarmate eiwitten zich opstapelen, overschrijden PRC’s de drempel die nodig is om te condenseren tot een druppelachtige virale fabriek, waar dan eindelijk genoomreplicatie wordt aangezet. Dit creëert een feedforward-cyclus: meer eiwitten maken een beter zaad, dat nog meer eiwitten vangt en snel uitgroeit tot een fabriek.
Ingebouwde verschillen tussen virusdeeltjes
De studie laat verder zien dat RSV-deeltjes die uit geïnfecteerde cellen worden vrijgegeven niet allemaal gelijk zijn. Sommige virions verpakken meerdere vRNPs, en velen bevatten ofwel voornamelijk PRC’s ofwel voornamelijk passieve vRNPs. Virions verrijkt in PRC’s hebben veel meer kans om een productieve infectie in een nieuwe cel te initiëren. Deze “virion-heterogeniteit” werd gezien bij laboratoriumstammen, klinische isolaten en virussen verzameld rechtstreeks van geïnfecteerde mensen, wat suggereert dat het een natuurlijke eigenschap van RSV-biologie is. Het aantal genomen per deeltje was veel minder bepalend dan of er minstens één PRC aanwezig was. Dus een kleine subset van goed uitgeruste deeltjes drijft waarschijnlijk de meeste succesvolle infecties, terwijl andere fungeren als onderbemande passagiers.
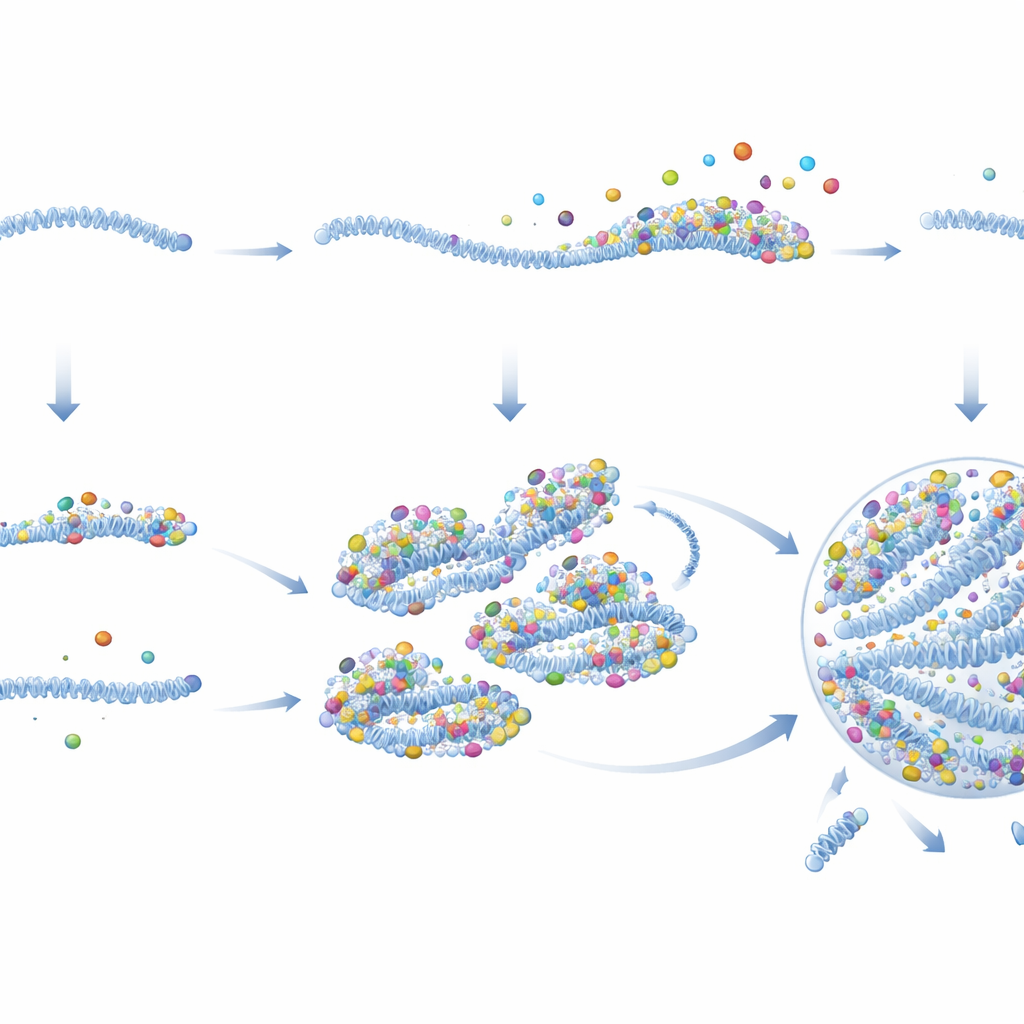
Waarom dit van belang is voor infectie en meer
In eenvoudige termen concluderen de auteurs dat RSV een schijnbaar kip-en-ei-probleem oplost—de noodzaak van hoge eiwitniveaus om virale fabrieken te bouwen, maar de behoefte aan fabrieken om eiwitten te maken—door eiwitrijke zaden vooraf te assembleren in sommige virions voordat ze een geïnfecteerde cel verlaten. Wanneer deze gezaden genomen een nieuwe cel binnengaan, beginnen ze onmiddellijk eiwitten te produceren en meer daaromheen te verzamelen, waardoor snel een virale fabriek wordt gekerneld en replicatie van start gaat. Passieve genomen daarentegen ontsnappen zelden aan deze laag-activiteitstoestand tenzij extra virale eiwitten worden geleverd. Dit werk verduidelijkt niet alleen waarom RSV-infecties zo veel kunnen variëren van cel tot cel, maar suggereert ook nieuwe strategieën: geneesmiddelen die deze zaden of hun vermogen om te condenseren verstoren, zouden de infectie in haar allereerste stappen kunnen afzwakken, en vergelijkbare principes kunnen bepalen hoe veel andere ziektegerelateerde biomoleculaire druppels zich in onze cellen vormen.
Bronvermelding: Ratnayake, D., Galloux, M., Boersma, S. et al. Pre-assembly of biomolecular condensate seeds drives RSV replication. Nature 652, 189–200 (2026). https://doi.org/10.1038/s41586-025-10071-5
Trefwoorden: respiratoir syncytieel virus, virale fabrieken, biomoleculaire condensaten, single-virus beeldvorming, infectie-heterogeniteit