Clear Sky Science · pl
Wstępne złożenie „zarodków” kondensatów biomolekularnych napędza replikację RSV
Dlaczego niektóre cząstki wirusa mają przewagę na starcie
Syncytialny wirus oddechowy (RSV) jest ważną przyczyną zakażeń płuc u niemowląt, osób starszych i osób z osłabionym układem odpornościowym. W tym badaniu postawiono pozornie proste pytanie o daleko idących konsekwencjach: gdy pojedyncza cząstka RSV zetknie się z komórką, co decyduje o tym, czy zakażenie się rozwinie, czy utknie w miejscu? Obserwując poszczególne genomowe kopie wirusa w żywych komórkach, autorzy odkryli ukryte różnice między cząstkami wirusa, które wyjaśniają, dlaczego jedne zakażenia wybuchają, a inne gasną.
Ukryte wirusowe krople wewnątrz zakażonych komórek
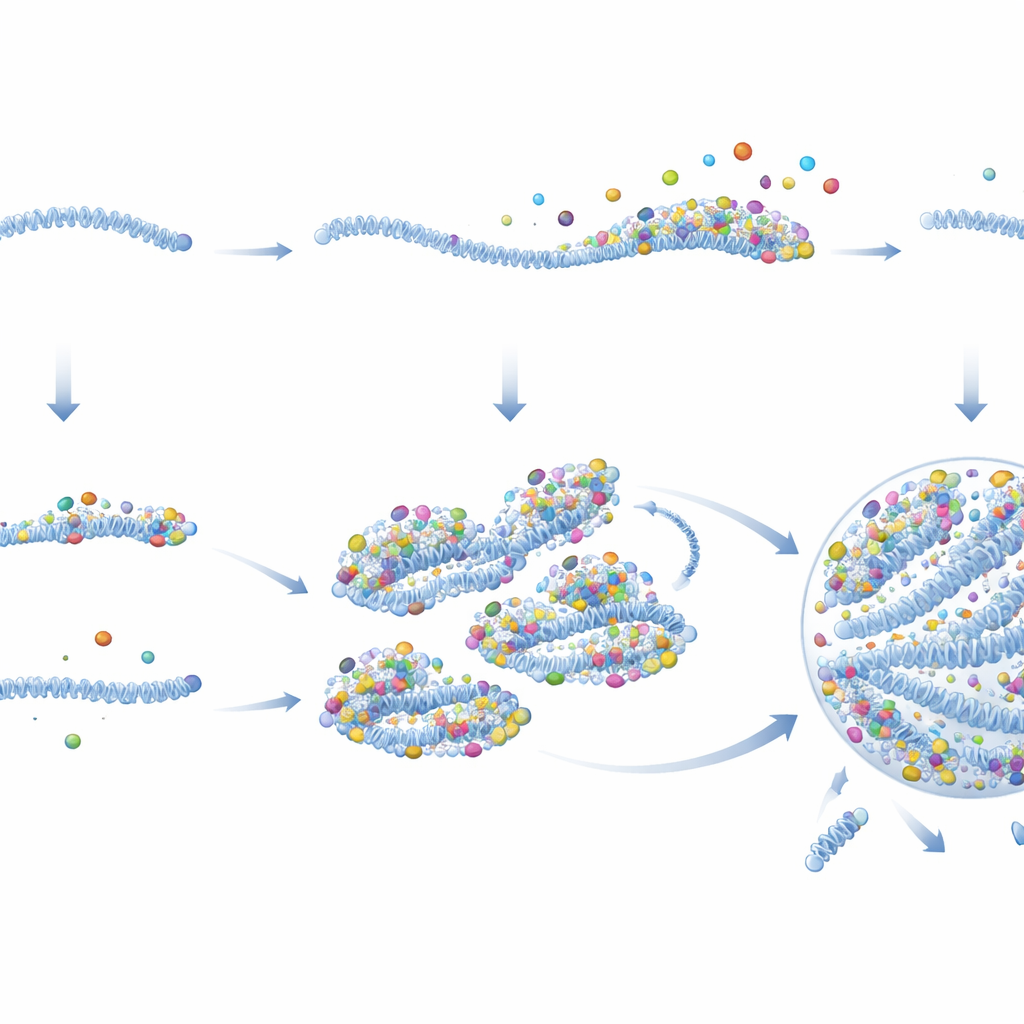
Po wejściu do komórki wiele wirusów RNA, w tym RSV, tworzy maleńkie, bezbłonowe „fabryki wirusowe”. Struktury przypominające krople koncentrują składniki wirusa i są głównymi miejscami, gdzie powstają nowe genomy i białka wirusowe. Jest jednak pewien problem: takie krople zwykle tworzą się dopiero przy wysokim stężeniu białek, podczas gdy we wczesnej fazie zakażenia białka wirusowe są rzadkie. Korzystając z zaawansowanej mikroskopii fluorescencyjnej, badacze śledzili pojedyncze kompleksy genomu RSV, zwane vRNP, od momentu ich wejścia do komórek. Stwierdzili, że fabryki wirusowe nie pojawiają się znikąd; zamiast tego rozwijają się z pojedynczych napływających vRNP, które stopniowo pęcznieją i łączą się w większe krople.
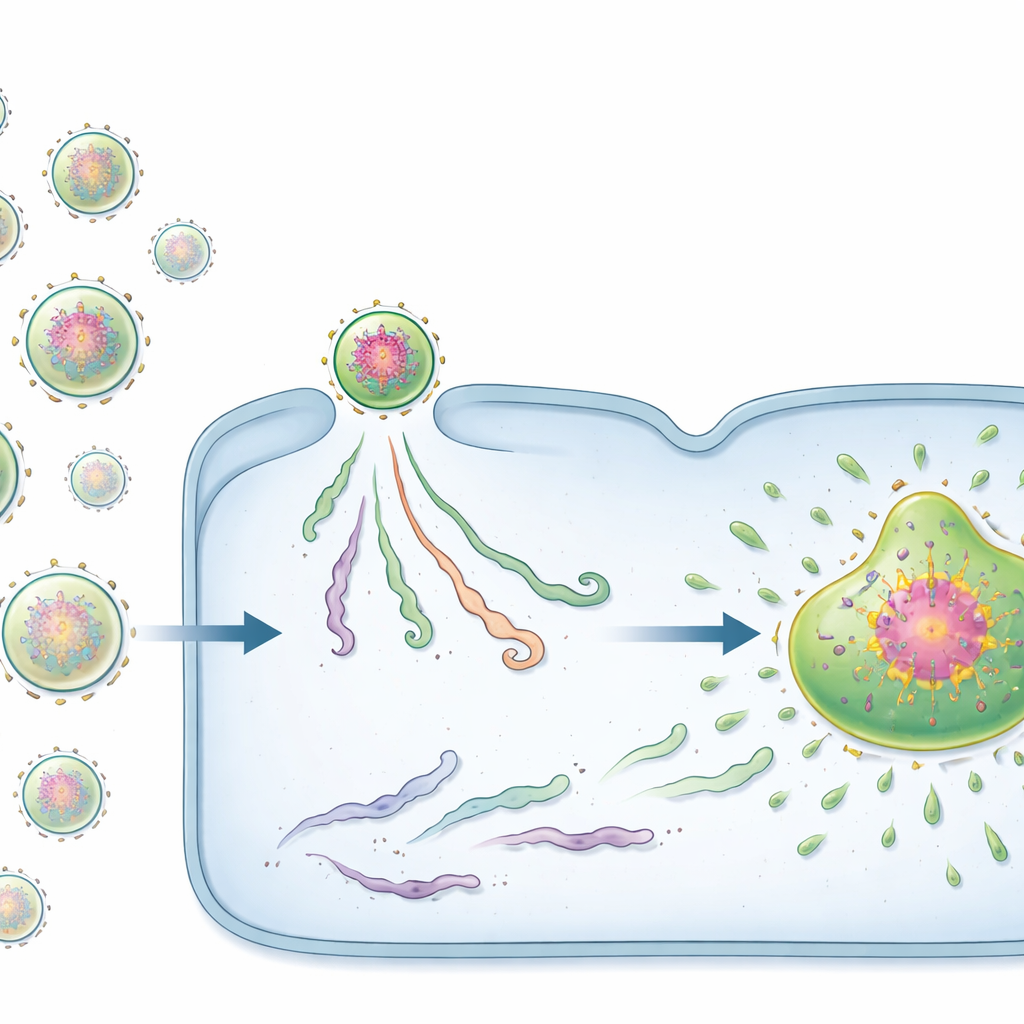
Dwa rodzaje startersów wirusowych: zarodki i pasażerowie
Ku zaskoczeniu, nie wszystkie napływające vRNP zachowywały się jednakowo. Dzięki specjalnie zaprojektowanym sondom fluorescencyjnym zespół odkrył dwa odrębne stany. Mniejszość vRNP niosła gęste skupiska białek wirusowych już złożonych wokół genomu. Te bogate w białko kompleksy, które autorzy nazywają pre‑centrum replikacji (PRC), działały jako silne „zarodki” dla fabryk wirusowych. Komórki zainfekowane nawet pojedynczym PRC niemal zawsze tworzyły fabrykę i produkowały dużą liczbę progenicznego materiału genomowego. W przeciwieństwie do nich większość vRNP nie miała takiej uprzednio załadowanej sieci białkowej i zostały nazwane pasywnymi vRNP. Zakażenia zapoczątkowane przez pasywne vRNP często utknęły: materiał wirusowy pozostawał mały i odizolowany, nie powstawały fabryki wirusowe ani progeniczne genomy.
Dlaczego zarodki odnosiły sukces, a pasażerowie zawodzili
Mierząc aktywność wirusa w czasie rzeczywistym, autorzy wykazali, że PRC szybko rozpoczynają transkrypcję genów wirusowych i robią to znacznie intensywniej niż pasywne vRNP. Szczegółowe obrazowanie i analizy biochemiczne ujawniły przyczynę. PRC zawierają znacznie więcej kopii kluczowych białek wirusowych — zwłaszcza polimerazy i jej kofaktora — na jeden genom niż pasywne vRNP, nawet przed wejściem do komórki. Po znalezieniu się w cytoplazmie te białka pozostają związane z PRC, podczas gdy odrywają się od pasywnych vRNP. PRC działają też jak „lepkie” rusztowania, przyciągające dodatkowe białka wirusowe, a nawet inne vRNP. W miarę kumulowania się białek PRC przekraczają próg potrzebny do skondensowania się w kroplopodobną fabrykę wirusową, gdzie w końcu uruchamia się replikacja genomu. Tworzy to pętlę dodatniego sprzężenia: więcej białek poprawia zarodek, który przyciąga jeszcze więcej białek i szybko przekształca się w fabrykę.
Wbudowane różnice między cząstkami wirusa
Badanie dodatkowo pokazuje, że cząstki RSV uwalniane z zakażonych komórek nie są sobie równe. Niektóre wiriony pakują wiele vRNP, a wiele zawiera przeważnie PRC albo przeważnie pasywne vRNP. Wiriony wzbogacone w PRC mają znacznie większe szanse na zainicjowanie produktywnego zakażenia w nowej komórce. Tę „heterogeniczność wirionów” zaobserwowano w szczepach laboratoryjnych, izolatów klinicznych i wirusach pobranych bezpośrednio od zakażonych osób, co sugeruje, że jest to naturalna cecha biologii RSV. Liczba genomów na cząstkę miała znacznie mniejsze znaczenie niż fakt, czy chociaż jeden z nich był PRC. Zatem niewielka podgrupa dobrze wyposażonych cząstek prawdopodobnie odpowiada za większość udanych zakażeń, podczas gdy inne działają jako niedołężni pasażerowie.
Dlaczego to ma znaczenie dla zakażeń i nie tylko
Mówiąc prosto, autorzy dochodzą do wniosku, że RSV rozwiązuje pozorny problem „co było pierwsze — jajko czy kura” — potrzebę wysokich poziomów białek do budowy fabryk wirusowych, a jednocześnie konieczność istnienia fabryk do produkcji białek — przez wstępne składanie bogatych w białko zarodków wewnątrz niektórych wirionów zanim opuszczą zakażoną komórkę. Gdy te zasiane genomy wejdą do nowej komórki, natychmiast zaczynają produkować białka i gromadzić je wokół siebie, szybko nukleując fabrykę wirusową i uruchamiając replikację. Genomy pasywne rzadko wychodzą z tego stanu niskiej aktywności, chyba że dostarczone zostaną dodatkowe białka wirusowe. Ta praca nie tylko wyjaśnia, dlaczego zakażenia RSV mogą tak bardzo różnić się między komórkami, lecz także sugeruje nowe strategie: leki zakłócające te zarodki lub ich zdolność do kondensacji mogłyby osłabić zakażenie na jego najwcześniejszych etapach, a podobne zasady mogą regulować tworzenie wielu innych patogennych kondensatów biomolekularnych wewnątrz naszych komórek.
Cytowanie: Ratnayake, D., Galloux, M., Boersma, S. et al. Pre-assembly of biomolecular condensate seeds drives RSV replication. Nature 652, 189–200 (2026). https://doi.org/10.1038/s41586-025-10071-5
Słowa kluczowe: syncytialny wirus oddechowy, fabryki wirusowe, kondensaty biomolekularne, obrazowanie pojedynczych wirusów, heterogeniczność zakażeń