Clear Sky Science · he
הכנה מוקדמת של זרעי עיבוד ביומולקולרי מניעה שכפול של RSV
איך חלק מחלקיקי הוירוס מקבלים יתרון ראשוני
וירוס הסינציטיאלי הנשימתי (RSV) הוא גורם מרכזי לזיהומי ריאות בתינוקות, מבוגרים בני גיל מתקדם ואנשים עם מערכת חיסונית מוחלשת. המחקר הזה שואל שאלה פשוטה לכאורה אך עם משמעויות גדולות: כשחלקיק RSV יחיד נוחת על תא, מה קובע אם ההדבקה תתפתח ותתרחב או תתהפך ותשקע ללא זיהוי? בעזרת מעקב אחר גנומים ויראליים בודדים בתאים חיים, המחברים חושפים הבדלים נסתרי בין חלקיקי הווירוס שמסבירים למה חלק מההדבקות מתפשטות בעוד שאחרות כושלות.
טיפות ויראליות חבויות בתוך תאים מודבקים
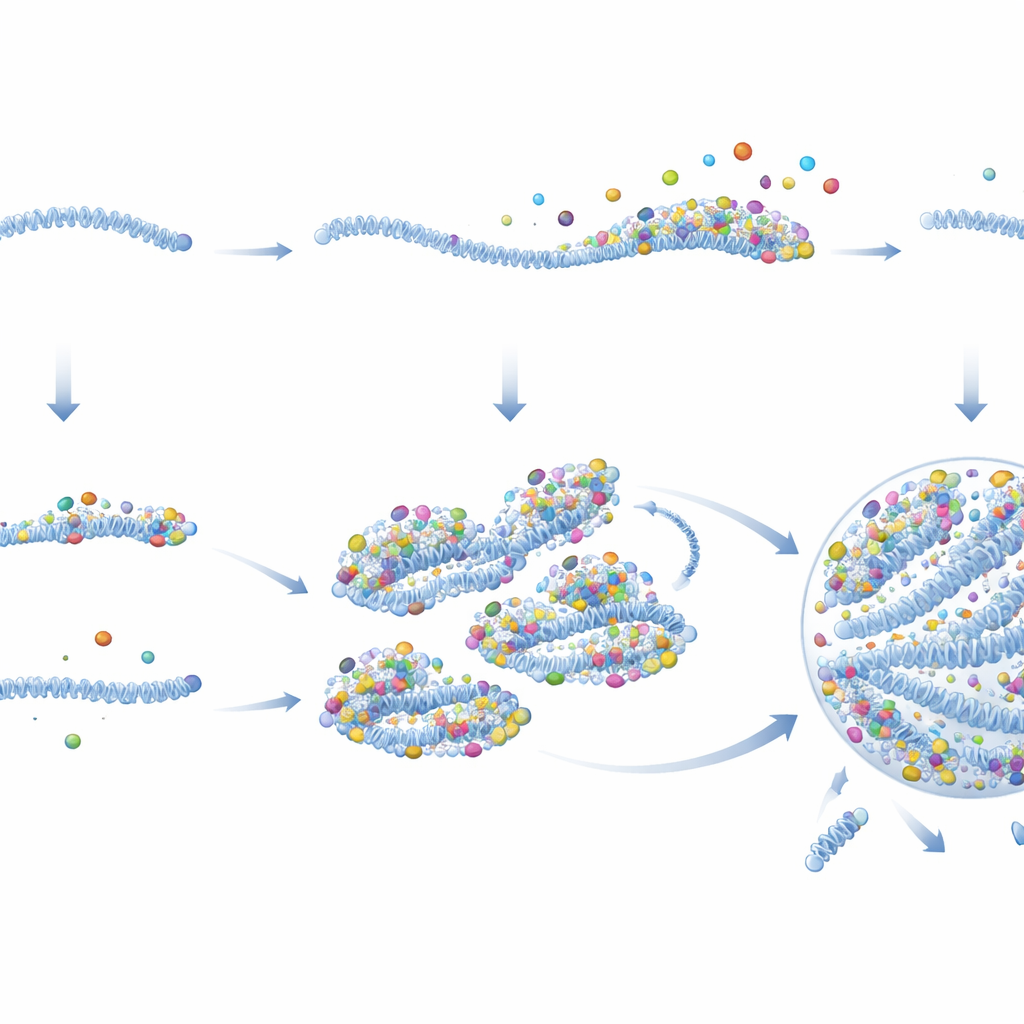
ברגע שהוירוס נכנס לתא, ורבים מן הרנא־וירוסים, כולל RSV, בונים "מפעלי וירוס" קטנים ללא ממברנה. מבנים דמויי טיפות אלה מרוכזים ברכיבים ויראליים והם האתרים העיקריים שבהם מיוצרים גנומים וחלבונים ויראליים חדשים. אך יש בעיה: טיפות אלה בדרך כלל נוצרות רק כאשר רמות החלבונים כבר גבוהות, בעוד שבשלבים מוקדמים של הדבקה חלבונים ויראליים נדירים. בעזרת מיקרוסקופיה פלואורסצנטית מתקדמת, החוקרים עקבו אחר קומפלקסים של הגנום הויראלי הבודד, המכונים vRNPs, מרגע כניסתם לתאים. הם גילו שמפעלי הוירוס אינם מופיעים משום מקום; במקום זאת הם מתבססים על vRNPs נכנסים בודדים שגדלים בהדרגה ומתחברים לטיפות גדולות יותר.
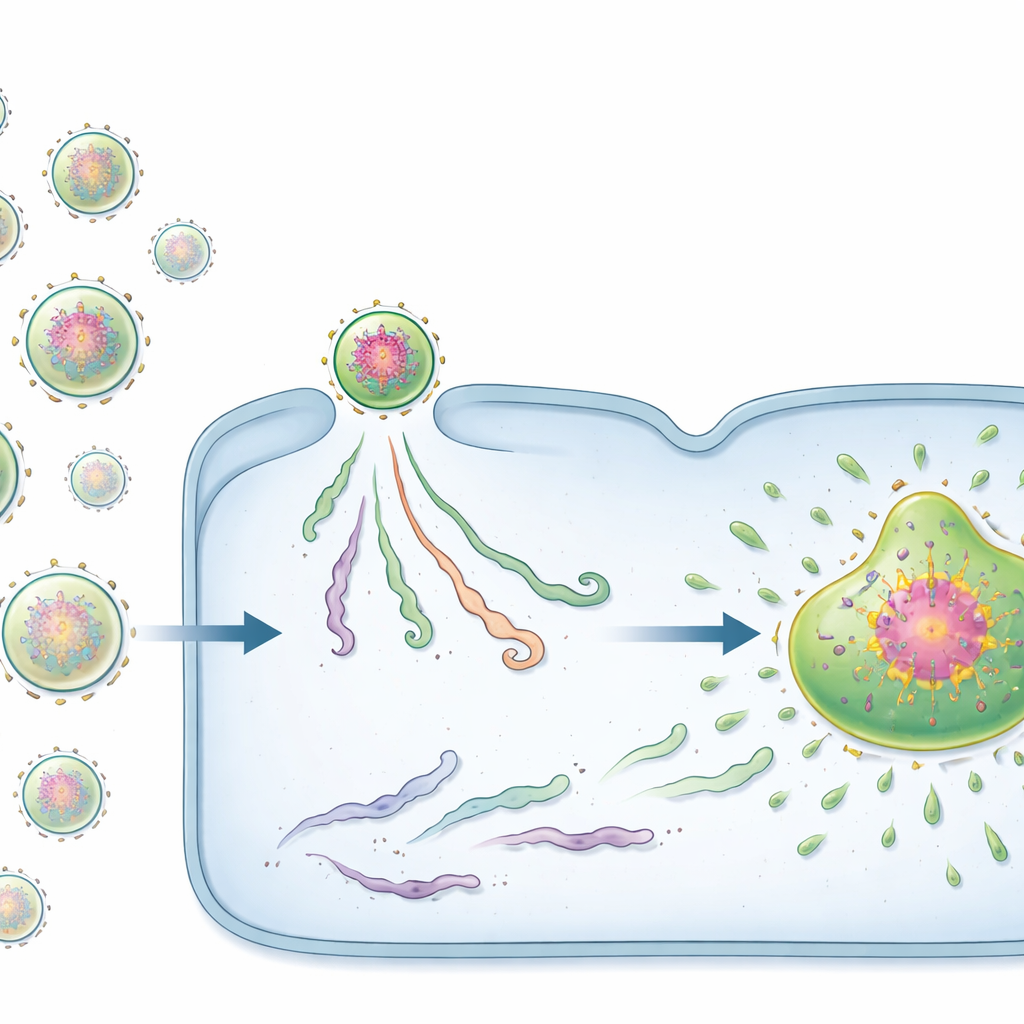
שני סוגי מייצרי הדבקה: זרעים ונוסעים
להפתעתם, לא כל ה‑vRNPs הנכנסים פעלו באותו אופן. בעזרת חיישני פלואורסצנציה מהונדסים במיוחד, הצוות גילה שתי מצבים מובחנים. מיעוט של vRNPs נשאו אשכולות צפופים של חלבונים ויראליים שכבר נבנו סביב הגנום. קומפלקסים עשירים בחלבון אלה, שהמחברים קוראים להם מרכזי קדם‑שכפול (PRCs), פעלו כ"זרעים" עוצמתיים למפעלי הוירוס. תאים שהודבקו אפילו על ידי PRC יחיד כמעט תמיד המשיכו ליצור מפעל ולייצר מספר רב של גנומי־צאצא. בניגוד לכך, רוב ה‑vRNPs חסרו את רשת החלבונים המוכנה וכונו vRNPs פסיביים. הדבקות שמתחילות ב‑vRNPs פסיביים לעתים קרובות נעצרו: החומר הויראלי נשאר קטן ומבודד, ולא הופיעו מפעל ויראלי או גנומי‑צאצא.
מדוע הזרעים מצליחים והנוסעים נכשל
על‑ידי מדידת הפעילות הויראלית בזמן אמת, הראו המחברים כי PRCs מתחילים לתמלל גנים ויראליים במהירות ובקצבים גבוהים בהרבה מאשר vRNPs פסיביים. הדמיה מפורטת וניתוחים ביוכימיים חשפו מדוע. ל‑PRCs יש כמות משמעותית גבוהה יותר של העתקי חלבונים ויראליים מרכזיים — במיוחד הפולימרז והקולבונד שלו — לכל גנום לעומת vRNPs פסיביים, אפילו לפני כניסתם לתא. ברגע שהם בציטופלסמה, חלבונים אלה נשארים קשורים ל‑PRCs אך נובלים מ‑vRNPs פסיביים. PRCs גם מתפקדים כמו שלד דביק שמושך חלבונים ויראליים נוספים ואף vRNPs אחרים. ככל שהחלבונים מצטברים, PRCs חוצים את הסף הנדרש להתעבות לטיפה‑דמוי מפעל ויראלי, שם שכפול הגנום נדלק סופית. זה יוצר לולאת הזנה קדימה: יותר חלבונים הופכים את הזרע ליעיל יותר, מה שלוכד עוד חלבונים וגדל במהירות למפעל.
הבדלים מובנים בין חלקיקי הוירוס
המחקר מראה גם שחלקיקי RSV המשתחררים מתאים מודבקים אינם שווים זה לזה. כמה ויריונים ארזו מספר vRNPs, ורבים מהם הכילו בעיקר PRCs או בעיקר vRNPs פסיביים. ויריונים העשירים ב‑PRCs נוטים בהרבה להתחיל הדבקה פרודוקטיבית בתא חדש. "ההטרוגניות של הויריון" הזו נצפתה בזנים מעבדתיים, מבודדים קליניים ובווירוסים שנלקחו ישירות מאנשים מודבקים, מה שמצביע על כך שמדובר בתכונה טבעית של ביולוגיית RSV. מספר הגנומים בכל חלקיק הוערך כפחות משמעותי מאשר השאלה האם לפחות אחד מהם הוא PRC. לפיכך, תת‑קבוצה קטנה של חלקיקים מצוידים היטב כנראה מייצרת את מרבית ההדבקות המוצלחות, בעוד אחרים משמשים כנוסעים חלשים.
מדוע הדבר חשוב לזיהום ומעבר לו
במלים פשוטות, המחברים מסכמים ש‑RSV פותר בעיה שנראית כמו דילמת העוף והביצה — צורך ברמות חלבון גבוהות כדי לבנות מפעלי וירוס, אך צורך במפעלים כדי לייצר חלבונים — על‑ידי הרכבה מוקדמת של זרעים עשירים בחלבון בתוך חלקיקים מסוימים לפני שאלה עוזבים תא מודבק. כאשר הגנומים המוסעים הללו נכנסים לתא חדש, הם מיד מתחילים לייצר חלבונים ולסלקף סביבם עוד חלבונים, ומגייסים במהירות מפעל ויראלי ומניעים שכפול. גנומים פסיביים, לעומת זאת, לעתים נדירות בורחים ממצב הפעילות הנמוכה הזה אלא אם כן מסופקים חלבונים ויראליים נוספים. עבודה זו לא רק מבהירה מדוע הדבקות RSV יכולות להשתנות כל כך מתא לתא, אלא גם מציעה אסטרטגיות חדשות: תרופות שמפריעות לזרעים אלה או ליכולתם להתעבות עשויות לבלום הדבקה כבר בשלבים הראשונים שלה, ועקרונות דומים עשויים לשלוט באופן שבו טיפות ביומולקולריות רבות הקשורות למחלות מתגבשות בתוך התאים שלנו.
ציטוט: Ratnayake, D., Galloux, M., Boersma, S. et al. Pre-assembly of biomolecular condensate seeds drives RSV replication. Nature 652, 189–200 (2026). https://doi.org/10.1038/s41586-025-10071-5
מילות מפתח: וירוס הסינציטיאלי הנשימתי, מפעלים ויראליים, עיבודים ביומולקולריים, דימות של וירוס יחיד, הטרוגניות בזיהום