Clear Sky Science · ar
التجميع المسبق لبذور المكثفات البيومولكولية يدفع تكاثر فيروس RSV
كيف تحصل بعض جزيئات الفيروس على بداية متقدمة
فيروس الجهاز التنفسي المخلوي (RSV) سبب رئيسي لالتهابات الرئة عند الرضع وكبار السن والأشخاص ذوي المناعة الضعيفة. تطرح هذه الدراسة سؤالاً يبدو بسيطاً لكنه ذو آثار كبيرة: عندما يهبط جسيم RSV مفرد على خلية، ما الذي يحدد ما إذا كانت تلك العدوى ستنطلق أم تتعثر بصمت؟ من خلال متابعة الجينومات الفيروسية الفردية في خلايا حية، يكشف المؤلفون فروقاً مخفية بين جزيئات الفيروس تفسر لماذا تتفجر بعض العدوى بينما تتلاشى أخرى.
قطرات فيروسية خفية داخل الخلايا المصابة
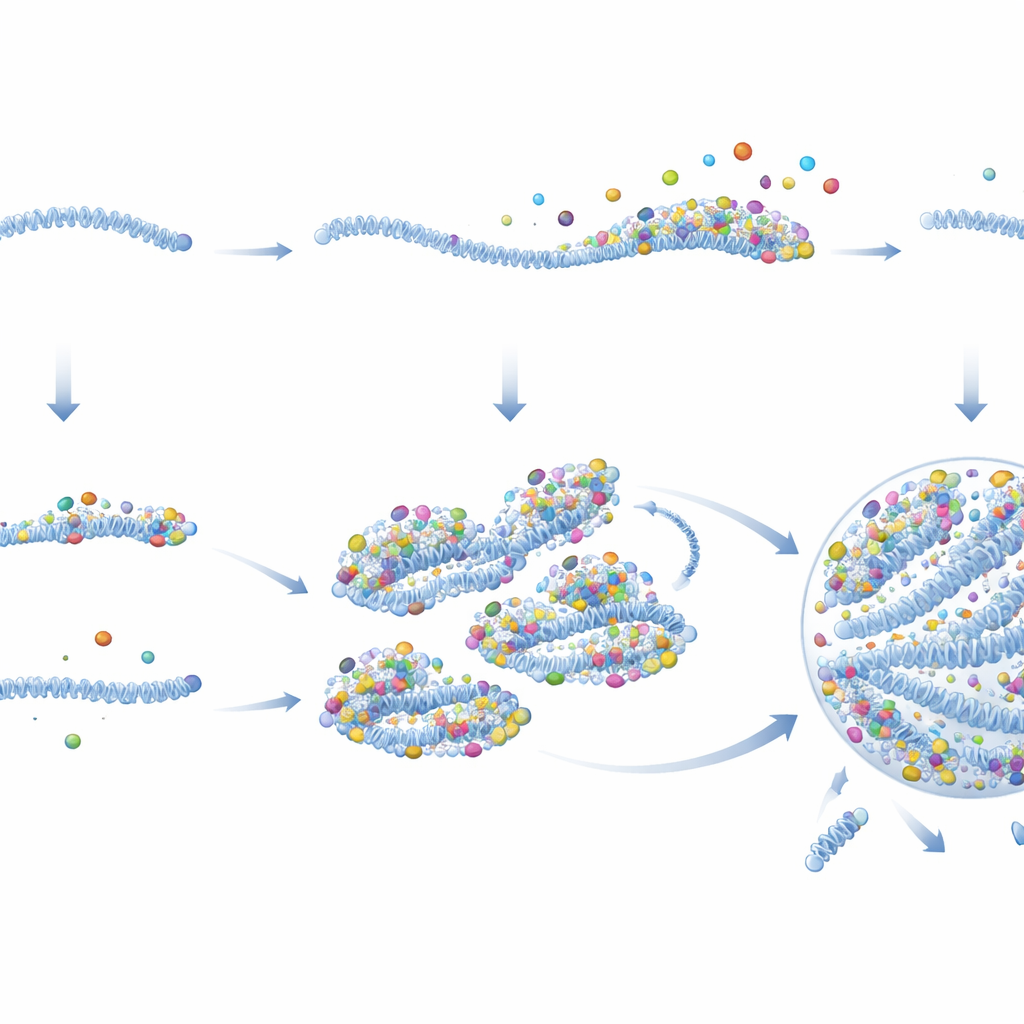
بمجرد دخولها إلى الخلية، تبني العديد من الفيروسات الريبيية، بما في ذلك RSV، «مصانع فيروسية» صغيرة خالية من الغشاء. هذه الهياكل الشبيهة بالقطرات تركز المكونات الفيروسية وتعد المواقع الرئيسية التي تُصنع فيها الجينومات والبروتينات الفيروسية الجديدة. لكن هناك مشكلة: مثل هذه القطرات عادة ما تتشكل فقط عندما تكون مستويات البروتين مرتفعة بالفعل، في حين أن البروتينات الفيروسية نادرة في المراحل المبكرة من العدوى. باستخدام مجهر فلوري متقدم، تعقّب الباحثون مركبات الجينوم الفيروسي المفردة، المسماة vRNPs، منذ لحظة دخولها الخلايا. ووجدوا أن المصانع الفيروسية لا تظهر من فراغ؛ بل تنمو من vRNPs واردة فردية تنتفخ تدريجياً وتندمج لتكوّن قطرات أكبر.
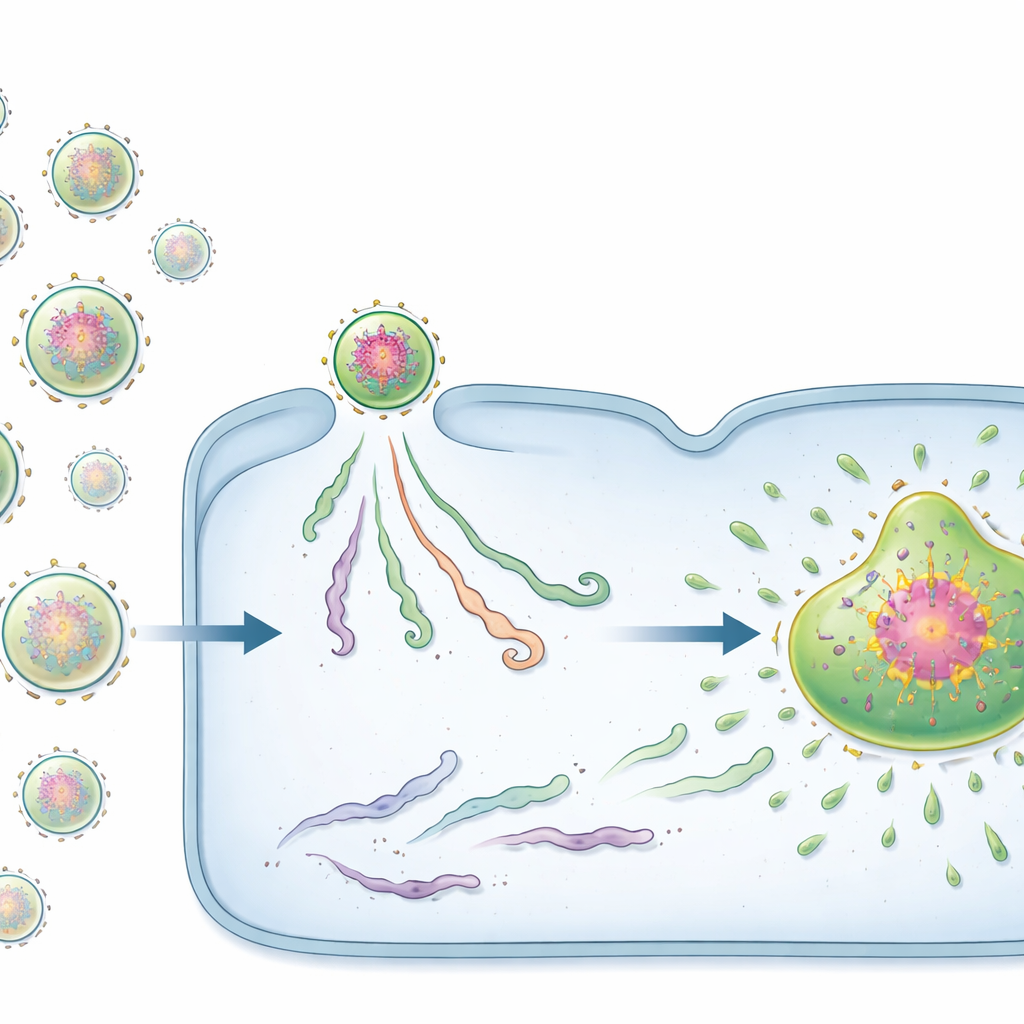
نوعان من بادئات الفيروس: البذور والركاب
بشكل مفاجئ، لم تتصرف كل vRNPs الواردة بالطريقة نفسها. باستخدام مجسات فلورية مصممة خصيصاً، اكتشف الفريق حالتين متميزتين. فئة أقلية من vRNPs كانت تحمل عناقيد كثيفة من البروتينات الفيروسية مُجمَّعة بالفعل حول الجينوم. هذه المعقدات الغنية بالبروتين، التي يسميها المؤلفون مراكز ما قبل التكاثر (PRCs)، عملت كبذور قوية للمصانع الفيروسية. الخلايا المصابة حتى بواسطة PRC واحد نادراً ما فشلت في تكوين مصنع وإنتاج أعداد كبيرة من الجينومات الوليدة. بالمقابل، افتقرت معظم vRNPs إلى هذه الشبكة البروتينية المحمّلة سلفاً وسميت vRNPs سلبية أو خاملة. العدوات التي تبدأ بـ vRNPs خاملة كثيراً ما تتعثر: تبقى المادة الفيروسية صغيرة ومعزولة، ولا يظهر أي مصنع فيروسي أو جينومات وليدة.
لماذا تنجح البذور حيث يفشل الركاب
من خلال قياس النشاط الفيروسي في الزمن الحقيقي، أظهر المؤلفون أن PRCs تبدأ نسخ الجينات الفيروسية بسرعة وبمعدلات أعلى بكثير من vRNPs الخاملة. كشفت التصويرات التفصيلية والتحاليل البيوكيميائية عن السبب. تحمل PRCs نسخاً أكثر بكثير من البروتينات الفيروسية الأساسية —وخاصة البوليميراز والعامل المساعد له— لكل جينوم مقارنةً بـ vRNPs الخاملة، حتى قبل دخول الخلية. بمجرد وجودها في السيتوبلازم، تظل هذه البروتينات مرتبطة بـ PRCs لكنها تتساقط من vRNPs الخاملة. تعمل PRCs أيضاً كهياكل لزجة تسحب بروتينات فيروسية إضافية وحتى vRNPs أخرى. مع تراكم البروتينات، تتجاوز PRCs العتبة اللازمة للتكاثف إلى مصنع فيروسي شبيه بالقطرة، حيث يبدأ تكرار الجينوم أخيراً. هذا يخلق حلقة تغذية أمامية: مزيد من البروتينات يجعل البذرة أفضل، والتي تلتقط مزيداً من البروتينات وتنمو بسرعة لتصبح مصنعاً.
اختلافات مدمجة بين جسيمات الفيروس
تُظهر الدراسة أيضاً أن الجسيمات الفيروسية التي تُطلقها الخلايا المصابة ليست متساوية جميعها. بعض الفيريونات تعبئ عدة vRNPs، ويحتوي كثيرٌ منها إما على أغلبية من PRCs أو أغلبية من vRNPs الخاملة. الفيريونات الغنية بالـ PRCs أكثر احتمالاً بكثير لأن تبدأ عدوى منتجة في خلية جديدة. رُصدت هذه «تغايرية الفيريونات» عبر سلالات مختبرية وعزلات سريرية وفيروسات جمعت مباشرة من أشخاص مصابين، ما يوحي بأنها سمة طبيعية في بيولوجيا RSV. عدد الجينومات في كل جسيم كان ذا أهمية أقل بكثير من وجود ما لا يقل عن واحد منها كـ PRC. هكذا، مجموعة صغيرة من الجسيمات المجهزة جيداً على الأرجح تقف وراء معظم العدوى الناجحة، في حين تعمل البقية كركاب ذوي قدرة منخفضة.
لماذا هذا مهم للعدوى وما بعدها
بعبارة بسيطة، يستنتج المؤلفون أن RSV يحل مشكلة تبدو كالطائر والدجاجة — الحاجة إلى مستويات بروتين عالية لبناء مصانع فيروسية، مع الحاجة إلى المصانع لصنع البروتينات — عن طريق تجميع بذور غنية بالبروتين داخل بعض الفيريونات قبل مغادرتها الخلية المصابة. عندما تدخل هذه الجينومات المزروعة خلية جديدة، تبدأ فوراً في إنتاج البروتينات وجمع المزيد حول نفسها، فتؤسس بسرعة مصنعاً فيروسياً وتطلق التكاثر. أما الجينومات الخاملة فنادراً ما تخرج من حالة النشاط المنخفض هذه ما لم تُزوَّد ببروتينات فيروسية إضافية. لا يوضح هذا العمل فحسب سبب تفاوت العدوى الخلوية بشدة، بل يشير أيضاً إلى استراتيجيات جديدة: قد تُضعف الأدوية التي تعطل هذه البذور أو قدرتها على التكاثف العدوى في خطواتها الأولى، وقد تحكم مبادئ مماثلة تشكيل العديد من المكثفات البيومولكولية المرتبطة بالأمراض داخل خلايانا.
الاستشهاد: Ratnayake, D., Galloux, M., Boersma, S. et al. Pre-assembly of biomolecular condensate seeds drives RSV replication. Nature 652, 189–200 (2026). https://doi.org/10.1038/s41586-025-10071-5
الكلمات المفتاحية: فيروس الجهاز التنفسي المخلوي, مصانع فيروسية, مكثفات بيومولكولية, تصوير فيروس واحد, تغايرية العدوى