Clear Sky Science · it
La pre-assemblaggio dei semi di condensati biomolecolari guida la replicazione di RSV
Perché alcune particelle virali iniziano prima
Il virus respiratorio sinciziale (RSV) è una causa importante di infezioni polmonari nei neonati, negli anziani e nelle persone con sistema immunitario compromesso. Questo studio pone una domanda apparentemente semplice ma dalle grandi implicazioni: quando una singola particella di RSV arriva su una cellula, che cosa determina se quell’infezione decollerà o si spegnerà silenziosamente? Seguendo singoli genomi virali in cellule vive, gli autori hanno scoperto differenze nascoste tra le particelle che spiegano perché alcune infezioni esplodono mentre altre si spengono.
Goccioline virali nascoste all’interno delle cellule infette
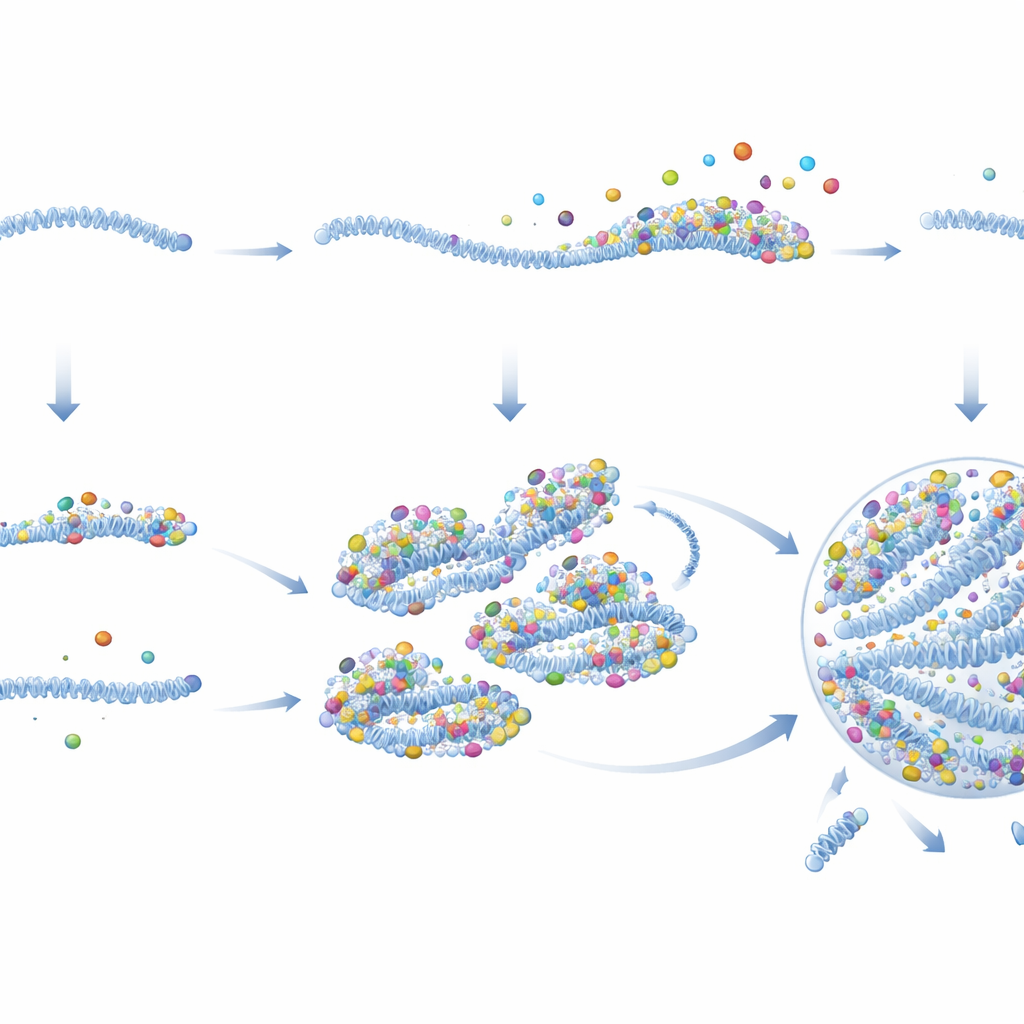
Una volta all’interno della cellula, molti virus a RNA, incluso RSV, costruiscono piccole “fabbriche virali” prive di membrana. Queste strutture a forma di goccia concentrano componenti virali e sono i principali siti in cui si producono nuovi genomi e proteine virali. C’è però un problema: tali goccioline di solito si formano solo quando i livelli proteici sono già elevati, mentre nelle prime fasi dell’infezione le proteine virali sono scarse. Utilizzando microscopia a fluorescenza avanzata, i ricercatori hanno seguito complessi genomici di RSV individuali, detti vRNP, dal momento in cui entravano nelle cellule. Hanno scoperto che le fabbriche virali non compaiono dal nulla; piuttosto, si sviluppano a partire da singoli vRNP in arrivo che gradualmente si ingrossano e si fondono in goccioline più grandi.
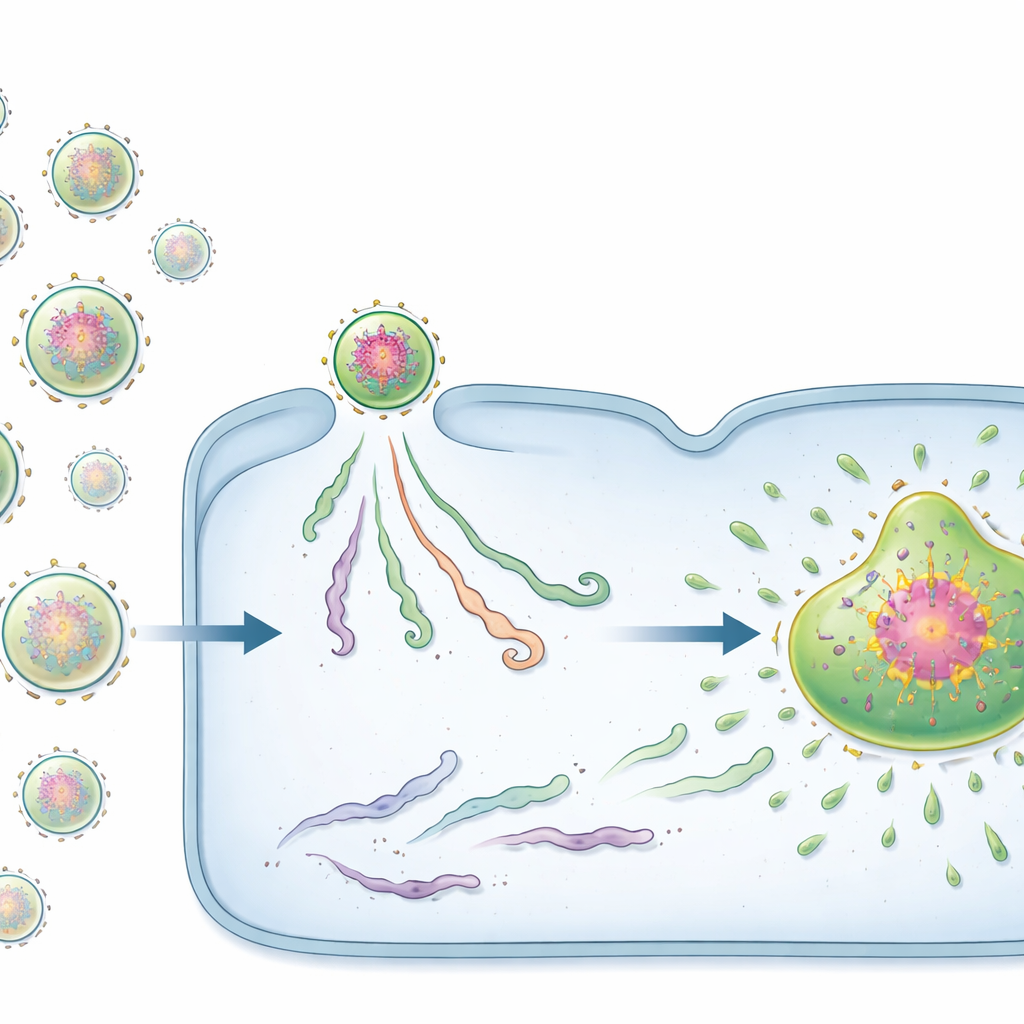
Due tipi di iniziatori virali: semi e passeggeri
Sorprendentemente, non tutti i vRNP in arrivo si comportavano allo stesso modo. Con sonde fluorescenti appositamente ingegnerizzate, il team ha scoperto due stati distinti. Una minoranza di vRNP portava già intorno al genoma ammassi densi di proteine virali assemblate. Questi complessi ricchi di proteine, che gli autori chiamano centri pre‑replicativi (PRC), fungevano da potenti “semi” per le fabbriche virali. Le cellule infettate anche da un solo PRC quasi sempre formavano una fabbrica e producevano un gran numero di genomi progenie. Al contrario, la maggior parte dei vRNP non possedeva questa rete proteica precaricata e veniva definita vRNP passiva. Le infezioni avviate da vRNP passive spesso si bloccavano: il materiale virale rimaneva piccolo e isolato, e non comparivano né fabbriche virali né genomi progenie.
Perché i semi hanno successo dove i passeggeri falliscono
Misurando l’attività virale in tempo reale, gli autori hanno mostrato che i PRC iniziano a trascrivere i geni virali rapidamente e a tassi molto più alti rispetto ai vRNP passivi. Analisi dettagliate di immagini e biochimiche hanno rivelato il perché. I PRC trasportano sostanzialmente più copie di proteine virali chiave—in particolare la polimerasi e il suo co‑fattore—per genoma rispetto ai vRNP passivi, anche prima dell’ingresso nella cellula. Una volta nel citoplasma, queste proteine restano legate ai PRC ma si staccano dai vRNP passivi. I PRC agiscono anche come impalcature adesive che attirano ulteriori proteine virali e perfino altri vRNP. Man mano che le proteine si accumulano, i PRC superano la soglia necessaria per condensarsi in una fabbrica virale di tipo gocciolante, dove la replicazione del genoma si attiva finalmente. Si crea così un ciclo a retroazione positiva: più proteine formano un seme migliore, che cattura ancora più proteine e cresce rapidamente in una fabbrica.
Differenze incorporate tra particelle virali
Lo studio mostra inoltre che le particelle di RSV rilasciate dalle cellule infette non sono tutte uguali. Alcuni virioni imballano più vRNP e molti contengono prevalentemente PRC o prevalentemente vRNP passivi. I virioni arricchiti in PRC hanno molte più probabilità di dare inizio a un’infezione produttiva in una nuova cellula. Questa “eterogeneità dei virioni” è stata osservata in ceppi di laboratorio, isolati clinici e virus raccolti direttamente da persone infette, suggerendo che sia una caratteristica naturale della biologia di RSV. Il numero di genomi per particella contava molto meno rispetto al fatto che almeno uno di essi fosse un PRC. Di conseguenza, un piccolo sottogruppo di particelle ben equipaggiate probabilmente guida la maggior parte delle infezioni riuscite, mentre le altre agiscono come passeggeri sottodimensionati.
Perché questo conta per l’infezione e oltre
In termini semplici, gli autori concludono che RSV risolve un apparente problema della gallina e dell’uovo—avere bisogno di alti livelli proteici per costruire fabbriche virali, ma avere bisogno delle fabbriche per produrre proteine—pre‑assemblando semi ricchi di proteine all’interno di alcuni virioni prima che lascino la cellula infetta. Quando questi genomi seminati entrano in una nuova cellula, iniziano immediatamente a produrre proteine e ad aggregarne altre intorno a sé, nucleando rapidamente una fabbrica virale e avviando la replicazione. I genomi passivi, al contrario, raramente sfuggono a questo stato di bassa attività a meno che non vengano forniti proteine virali aggiuntive. Questo lavoro non solo chiarisce perché le infezioni da RSV possono variare così tanto da cellula a cellula, ma suggerisce anche nuove strategie: farmaci che disturbano questi semi o la loro capacità di condensarsi potrebbero attenuare l’infezione fin dai primissimi passaggi, e principi simili potrebbero regolare la formazione di molti altri condensati biomolecolari legati a malattie all’interno delle nostre cellule.
Citazione: Ratnayake, D., Galloux, M., Boersma, S. et al. Pre-assembly of biomolecular condensate seeds drives RSV replication. Nature 652, 189–200 (2026). https://doi.org/10.1038/s41586-025-10071-5
Parole chiave: virus respiratorio sinciziale, fabbriche virali, condensati biomolecolari, imaging di singoli virus, eterogeneità dell'infezione