Clear Sky Science · fr
Préassemblage de graines de condensats biomoléculaires favorise la réplication du VRS
Comment certaines particules virales prennent de l’avance
Le virus respiratoire syncytial (VRS) est une cause majeure d’infections pulmonaires chez les nourrissons, les personnes âgées et les sujets immunodéprimés. Cette étude pose une question apparemment simple mais aux grandes implications : lorsqu’une seule particule de VRS atteint une cellule, qu’est‑ce qui détermine si l’infection va démarrer ou s’éteindre silencieusement ? En suivant des génomes viraux individuels dans des cellules vivantes, les auteurs font apparaître des différences cachées entre particules virales qui expliquent pourquoi certaines infections explosent tandis que d’autres s’éteignent.
Des gouttelettes virales cachées dans les cellules infectées
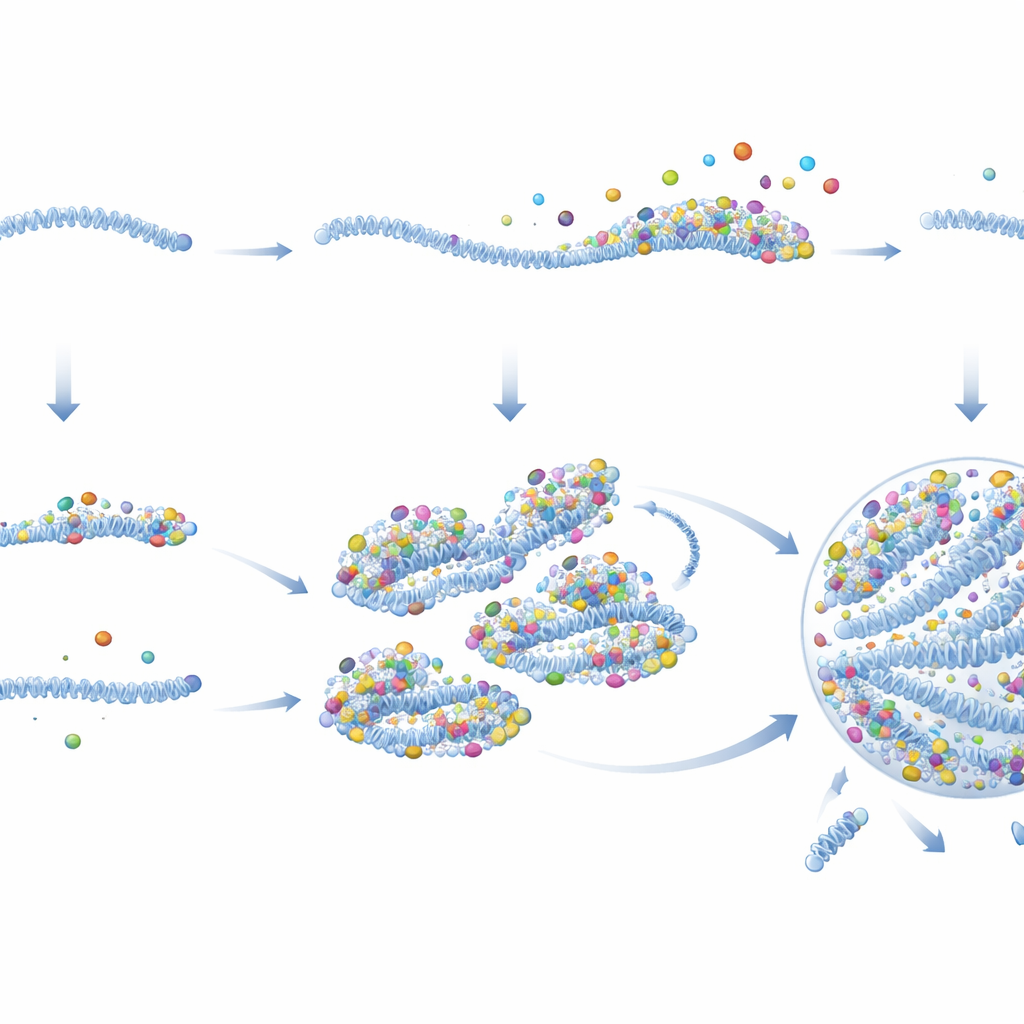
Une fois à l’intérieur d’une cellule, de nombreux virus à ARN, y compris le VRS, construisent de petites « usines virales » sans membrane. Ces structures en forme de goutte concentrent les composants viraux et sont les principaux lieux où de nouveaux génomes et protéines virales sont produits. Mais il y a un problème : ces gouttelettes se forment généralement seulement lorsque les niveaux protéiques sont déjà élevés, alors qu’au début de l’infection les protéines virales sont rares. Grâce à une microscopie de fluorescence avancée, les chercheurs ont suivi des complexes génomiques viraux individuels, appelés vRNP, depuis le moment où ils pénétraient dans les cellules. Ils ont constaté que les usines virales n’apparaissent pas ex nihilo ; elles se développent plutôt à partir de vRNP entrants individuels qui gonflent progressivement et fusionnent en gouttelettes plus grandes.
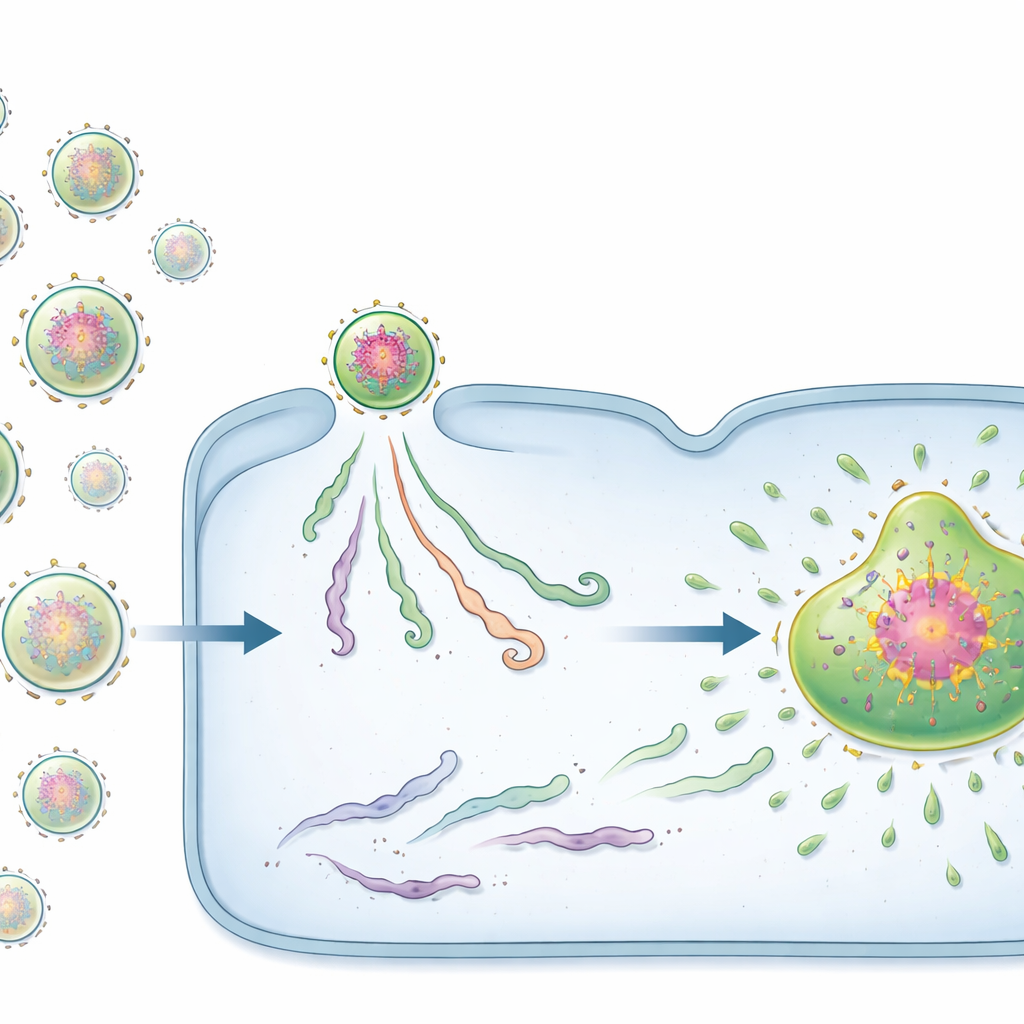
Deux types de démarreurs viraux : graines et passagers
De façon surprenante, tous les vRNP entrants ne se comportaient pas de la même façon. Avec des sondes fluorescentes spécialement conçues, l’équipe a découvert deux états distincts. Une minorité de vRNP portaient déjà des amas denses de protéines virales assemblées autour du génome. Ces complexes riches en protéines, que les auteurs appellent centres de pré‑réplication (CPR), agissaient comme de puissantes « graines » pour les usines virales. Les cellules infectées par ne serait‑ce qu’un seul CPR formaient presque toujours une usine et produisaient un grand nombre de génomes descendants. En revanche, la plupart des vRNP ne possédaient pas ce réseau protéique préchargé et furent qualifiés de vRNP passifs. Les infections initiées par des vRNP passifs s’interrompaient fréquemment : le matériel viral restait petit et isolé, et aucune usine virale ni génome descendant n’apparaissait.
Pourquoi les graines réussissent là où les passagers échouent
En mesurant l’activité virale en temps réel, les auteurs montrent que les CPR commencent à transcrire les gènes viraux rapidement et à des taux beaucoup plus élevés que les vRNP passifs. Des analyses d’imagerie détaillées et biochimiques expliquent pourquoi. Les CPR portent sensiblement plus de copies de protéines virales clés—en particulier la polymérase et son cofacteur—par génome que les vRNP passifs, et ce dès avant l’entrée dans la cellule. Une fois dans le cytoplasme, ces protéines restent liées aux CPR mais se détachent des vRNP passifs. Les CPR agissent également comme des échafaudages collants qui attirent d’autres protéines virales et même d’autres vRNP. À mesure que les protéines s’accumulent, les CPR franchissent le seuil nécessaire pour se condenser en une usine virale de type goutte, où la réplication du génome s’enclenche enfin. Cela crée une boucle d’amplification : davantage de protéines renforcent la graine, qui capture encore plus de protéines et croît rapidement en une usine.
Différences intégrées entre particules virales
L’étude montre en outre que les particules de VRS libérées par des cellules infectées ne sont pas toutes identiques. Certains virions emballent plusieurs vRNP, et beaucoup contiennent soit principalement des CPR, soit principalement des vRNP passifs. Les virions enrichis en CPR ont beaucoup plus de chances d’initier une infection productive dans une nouvelle cellule. Cette « hétérogénéité des virions » a été observée dans des souches de laboratoire, des isolats cliniques et des virus prélevés directement chez des personnes infectées, ce qui suggère qu’il s’agit d’une caractéristique naturelle de la biologie du VRS. Le nombre de génomes par particule importait beaucoup moins que la présence d’au moins un CPR. Ainsi, un petit sous‑ensemble de particules bien équipées pilote probablement la plupart des infections réussies, tandis que d’autres jouent le rôle de passagers sous‑motorisés.
Pourquoi cela compte pour l’infection et au‑delà
En termes simples, les auteurs concluent que le VRS résout un problème apparemment du type « poule et œuf »—avoir besoin de niveaux protéiques élevés pour construire des usines virales, mais avoir besoin d’usines pour produire ces protéines—en préassemblant des graines riches en protéines à l’intérieur de certains virions avant qu’ils ne quittent une cellule infectée. Lorsque ces génomes pré‑équipés pénètrent dans une nouvelle cellule, ils commencent immédiatement à produire des protéines et à en rassembler davantage autour d’eux, nucléant rapidement une usine virale et lançant la réplication. Les génomes passifs, en revanche, échappent rarement à cet état de faible activité à moins qu’un apport supplémentaire de protéines virales ne soit fourni. Ce travail clarifie non seulement pourquoi les infections à VRS peuvent varier d’une cellule à l’autre, mais suggère aussi de nouvelles stratégies : des médicaments qui perturbent ces graines ou leur capacité à se condenser pourraient atténuer l’infection dès ses premiers instants, et des principes similaires peuvent régir la formation de nombreux autres condensats biomoléculaires liés aux maladies dans nos cellules.
Citation: Ratnayake, D., Galloux, M., Boersma, S. et al. Pre-assembly of biomolecular condensate seeds drives RSV replication. Nature 652, 189–200 (2026). https://doi.org/10.1038/s41586-025-10071-5
Mots-clés: virus respiratoire syncytial, usines virales, condensats biomoléculaires, imagerie d’un seul virus, hétérogénéité de l’infection