Clear Sky Science · pt
Pré-montagem de sementes de condensados biomoleculares impulsiona a replicação do RSV
Como algumas partículas virais ganham vantagem inicial
O vírus sincicial respiratório (RSV) é uma causa importante de infecções pulmonares em bebês, idosos e pessoas com o sistema imunológico comprometido. Este estudo investiga uma pergunta aparentemente simples, mas de grande impacto: quando uma única partícula de RSV chega a uma célula, o que determina se essa infecção vai prosperar ou ficar silenciosamente estagnada? Ao observar genomas virais individuais em células vivas, os autores revelam diferenças ocultas entre partículas virais que explicam por que algumas infecções explodem enquanto outras se apagam.
Gotas virais ocultas dentro de células infectadas
Uma vez dentro da célula, muitos vírus de RNA, incluindo o RSV, constroem pequenas “fábricas virais” sem membrana. Essas estruturas semelhantes a gotas concentram componentes virais e são os principais locais onde novos genomas e proteínas virais são produzidos. Mas há uma contradição: tais gotas geralmente se formam apenas quando os níveis de proteína já estão altos, enquanto no início da infecção as proteínas virais são escassas. Usando microscopia de fluorescência avançada, os pesquisadores rastrearam complexos de genoma de RSV individuais, chamados vRNPs, desde o momento em que entraram nas células. Eles descobriram que as fábricas virais não surgem do nada; em vez disso, crescem a partir de vRNPs entrantes individuais que gradualmente incham e se fundem em gotas maiores.
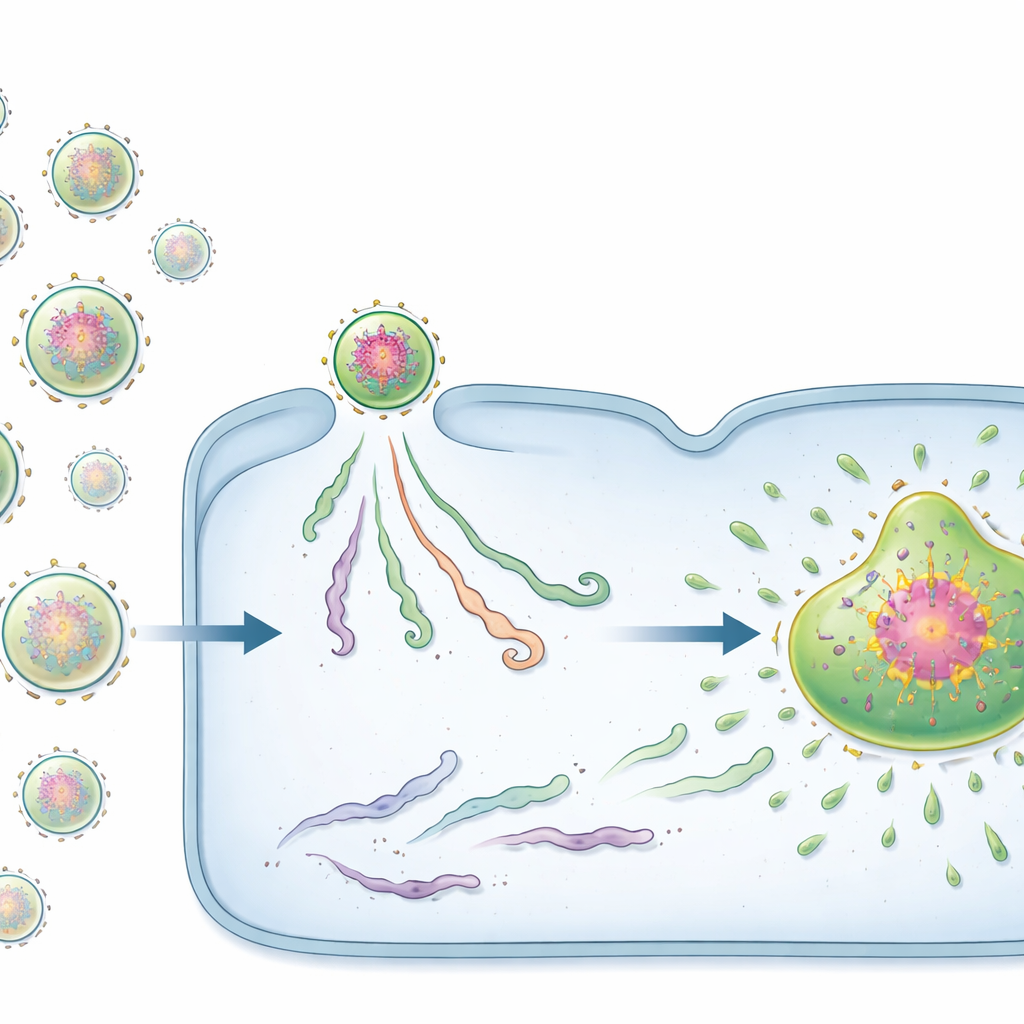
Dois tipos de iniciadores virais: sementes e passageiras
Surpreendentemente, nem todos os vRNPs entrantes se comportaram da mesma forma. Com sondas fluorescentes especialmente projetadas, a equipe identificou dois estados distintos. Uma minoria de vRNPs carregava aglomerados densos de proteínas virais já montadas ao redor do genoma. Esses complexos ricos em proteínas, que os autores chamam de centros pré‑replicativos (PRCs), atuavam como poderosas “sementes” para as fábricas virais. Células infectadas por mesmo um único PRC quase sempre formavam uma fábrica e produziam grande número de genomas progenitores. Em contraste, a maioria dos vRNPs não possuía essa rede proteica pré-carregada e foi classificada como vRNPs passivos. Infecções iniciadas por vRNPs passivos frequentemente estagnavam: o material viral permanecia pequeno e isolado, e nenhuma fábrica viral ou genomas progenitores apareciam.
Por que as sementes têm sucesso onde as passageiras falham
Ao medir a atividade viral em tempo real, os autores mostraram que os PRCs começam a transcrever genes virais rapidamente e em taxas muito maiores do que os vRNPs passivos. Imagens detalhadas e análises bioquímicas revelaram o porquê. Os PRCs carregam substancialmente mais cópias de proteínas virais-chave — especialmente a polimerase e seu cofator — por genoma do que os vRNPs passivos, mesmo antes de entrar na célula. Uma vez no citoplasma, essas proteínas permanecem ligadas aos PRCs, mas se desprendem dos vRNPs passivos. Os PRCs também funcionam como andaimes pegajosos que atraem proteínas virais adicionais e até outros vRNPs. À medida que as proteínas se acumulam, os PRCs ultrapassam o limiar necessário para se condensarem em uma fábrica viral tipo gota, onde a replicação do genoma finalmente é ativada. Isso cria um ciclo de retroalimentação: mais proteínas tornam uma semente melhor, que captura ainda mais proteínas e cresce rapidamente em uma fábrica.
Diferenças incorporadas entre partículas virais
O estudo também mostra que as partículas de RSV liberadas de células infectadas não são todas iguais. Alguns vírions empacotam múltiplos vRNPs, e muitos contêm predominantemente PRCs ou predominantemente vRNPs passivos. Vírions enriquecidos em PRCs têm muito mais probabilidade de iniciar uma infecção produtiva em uma nova célula. Essa “heterogeneidade de vírions” foi observada em cepas de laboratório, isolados clínicos e vírus coletados diretamente de pessoas infectadas, sugerindo que é uma característica natural da biologia do RSV. O número de genomas por partícula importou bem menos do que o fato de pelo menos um deles ser um PRC. Assim, um pequeno subconjunto de partículas bem equipadas provavelmente conduz a maioria das infecções bem‑sucedidas, enquanto outras atuam como passageiras subdimensionadas.
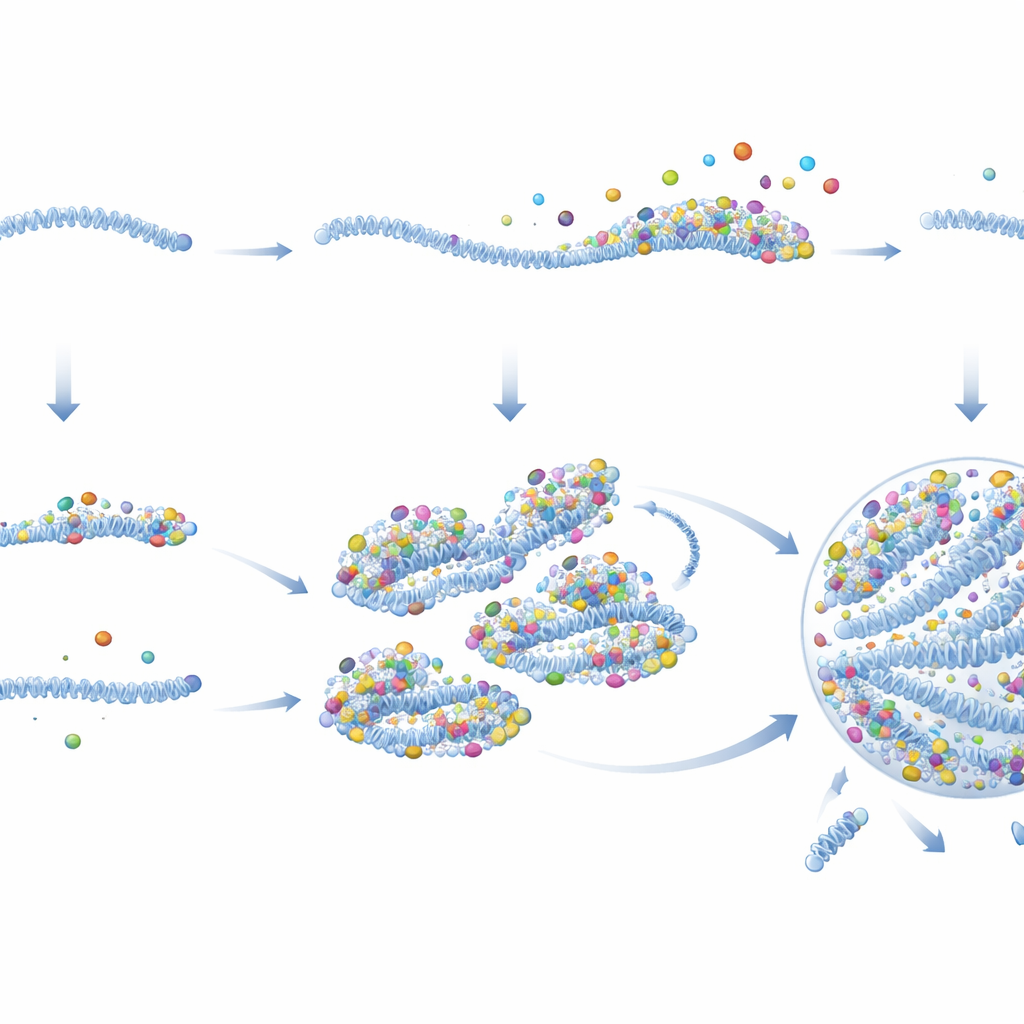
Por que isso importa para a infecção e além
Em termos simples, os autores concluem que o RSV resolve um aparente problema do tipo “ovo e galinha” — precisar de altos níveis de proteína para construir fábricas virais, mas precisar das fábricas para produzir proteínas — pré‑montando sementes ricas em proteínas dentro de alguns vírions antes de saírem da célula infectada. Quando esses genomas semeados entram em uma nova célula, começam imediatamente a produzir proteínas e a reunir mais ao redor de si, rapidamente nucleando uma fábrica viral e lançando a replicação. Genomas passivos, por outro lado, raramente escapam desse estado de baixa atividade, a menos que proteínas virais adicionais sejam fornecidas. Este trabalho não só esclarece por que as infecções por RSV podem variar tanto de célula para célula, mas também sugere novas estratégias: fármacos que perturbem essas sementes ou sua capacidade de condensar poderiam atenuar a infecção em seus primeiros passos, e princípios semelhantes podem governar como muitas outras gotas biomoleculares relacionadas a doenças se formam dentro de nossas células.
Citação: Ratnayake, D., Galloux, M., Boersma, S. et al. Pre-assembly of biomolecular condensate seeds drives RSV replication. Nature 652, 189–200 (2026). https://doi.org/10.1038/s41586-025-10071-5
Palavras-chave: vírus sincicial respiratório, fábricas virais, condensados biomoleculares, imagens de vírus único, heterogeneidade da infecção