Clear Sky Science · es
Preensamblaje de semillas de condensados biomoleculares impulsa la replicación del VSR
Cómo algunas partículas virales obtienen ventaja inicial
El virus respiratorio sincitial (VSR) es una causa principal de infecciones pulmonares en bebés, adultos mayores y personas con el sistema inmune debilitado. Este estudio plantea una pregunta aparentemente simple con grandes implicaciones: cuando una única partícula de VSR llega a una célula, ¿qué determina si esa infección despegará o quedará silenciosamente estancada? Al observar genomas virales individuales en células vivas, los autores descubren diferencias ocultas entre partículas virales que explican por qué algunas infecciones se disparan mientras otras se apagan.
Gotas virales ocultas dentro de células infectadas
Una vez dentro de la célula, muchos virus de ARN, incluido el VSR, construyen diminutas “fábricas virales” sin membrana. Estas estructuras similares a gotas concentran componentes virales y son los principales lugares donde se producen nuevos genomas y proteínas virales. Pero hay un problema: tales gotas suelen formarse solo cuando los niveles de proteína ya son altos, mientras que al inicio de la infección las proteínas virales son escasas. Usando microscopía de fluorescencia avanzada, los investigadores siguieron complejos de genoma viral individuales, llamados vRNPs, desde el momento en que entraron en las células. Encontraron que las fábricas virales no aparecen de la nada; en su lugar, crecen a partir de vRNPs entrantes individuales que se hinchan gradualmente y se fusionan en gotas más grandes.
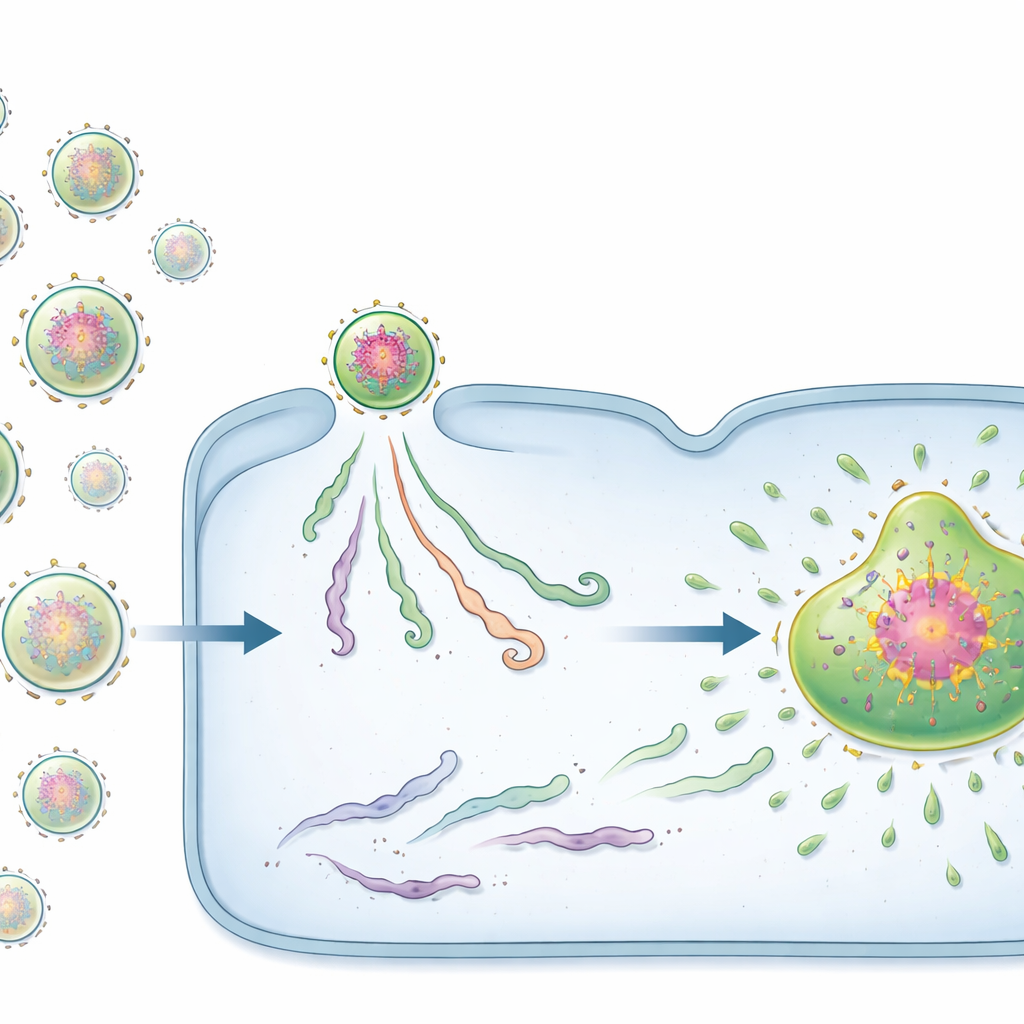
Dos tipos de iniciadores virales: semillas y pasajeras
Sorprendentemente, no todos los vRNPs entrantes se comportaron igual. Con sondas fluorescentes especialmente diseñadas, el equipo identificó dos estados distintos. Una minoría de vRNPs llevaba cúmulos densos de proteínas virales ya ensambladas alrededor del genoma. Estos complejos ricos en proteína, que los autores denominan centros pre‑replicativos (PRC), actuaban como potentes “semillas” para las fábricas virales. Las células infectadas por incluso un solo PRC casi siempre terminaban formando una fábrica y produciendo un gran número de genomas descendientes. En contraste, la mayoría de los vRNPs carecían de esta red proteica precargada y se clasificaron como vRNPs pasivos. Las infecciones iniciadas por vRNPs pasivos con frecuencia se estancaban: el material viral se mantenía pequeño y aislado, y no aparecían fábricas virales ni genomas progenie.
Por qué las semillas triunfan donde las pasajeras fracasan
Midiendo la actividad viral en tiempo real, los autores mostraron que los PRC comienzan a transcribir genes virales rápidamente y a tasas mucho más altas que los vRNPs pasivos. Imágenes detalladas y análisis bioquímicos revelaron el porqué. Los PRC llevan considerablemente más copias de proteínas virales clave —especialmente la polimerasa y su cofactor— por genoma que los vRNPs pasivos, incluso antes de entrar en la célula. Una vez en el citoplasma, estas proteínas permanecen unidas a los PRC pero se desprenden de los vRNPs pasivos. Los PRC también actúan como andamiajes pegajosos que atraen proteínas virales adicionales e incluso otros vRNPs. A medida que se acumulan proteínas, los PRC cruzan el umbral necesario para condensarse en una fábrica viral con apariencia de gota, donde finalmente se enciende la replicación del genoma. Esto crea un bucle de refuerzo: más proteínas hacen una mejor semilla, que captura aún más proteínas y crece rápidamente hasta formar una fábrica.
Diferencias incorporadas entre partículas virales
El estudio muestra además que las partículas de VSR liberadas por células infectadas no son todas iguales. Algunos viriones empaquetan múltiples vRNPs, y muchos contienen mayoritariamente PRC o mayoritariamente vRNPs pasivos. Los viriones enriquecidos en PRC tienen muchas más probabilidades de iniciar una infección productiva en una célula nueva. Esta “heterogeneidad de viriones” se observó en cepas de laboratorio, aislamientos clínicos y virus recogidos directamente de personas infectadas, lo que sugiere que es una característica natural de la biología del VSR. El número de genomas por partícula importó mucho menos que si al menos uno de ellos era un PRC. Así, un pequeño subconjunto de partículas bien equipadas probablemente impulsa la mayoría de las infecciones exitosas, mientras que otras actúan como pasajeras poco potentes.
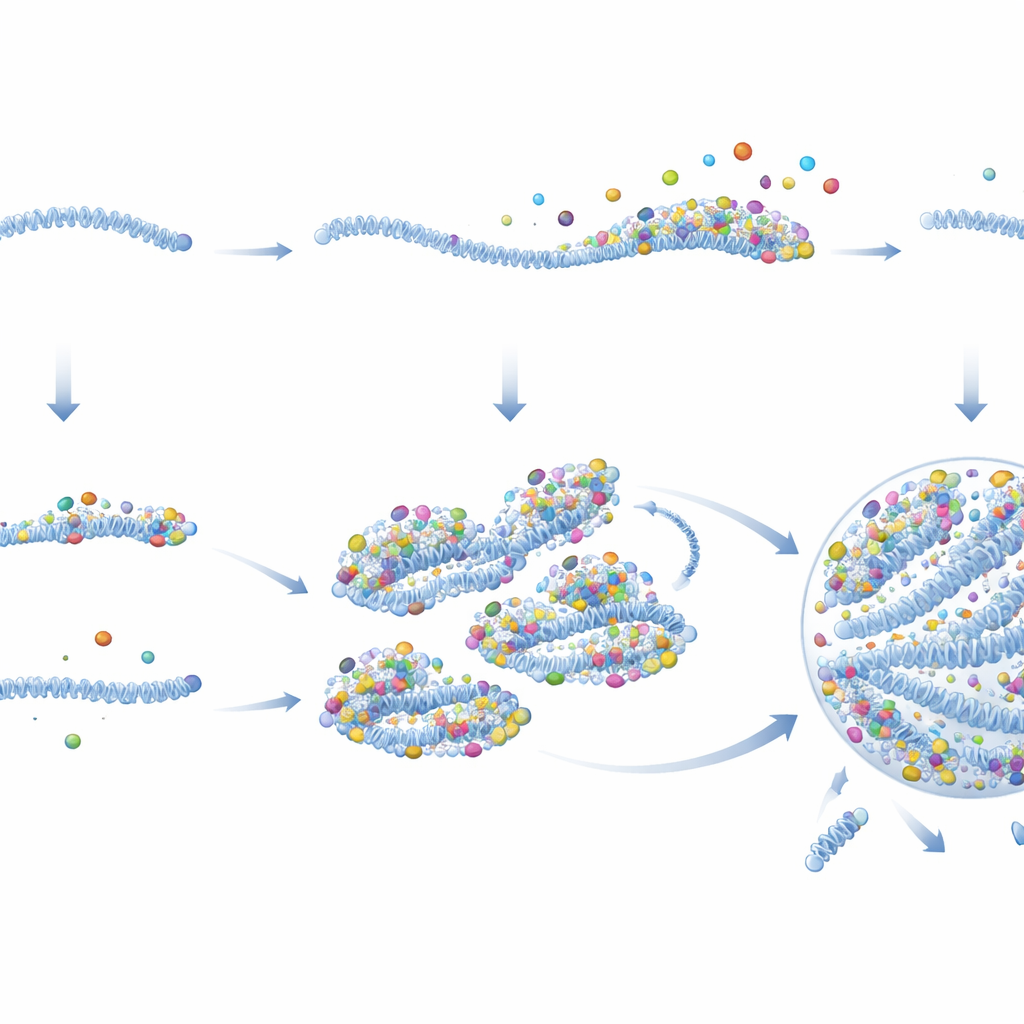
Por qué esto importa para la infección y más allá
En términos sencillos, los autores concluyen que el VSR resuelve un aparente problema del huevo y la gallina —necesitar niveles altos de proteína para construir fábricas virales, pero necesitar fábricas para producir proteínas— preensamblando semillas ricas en proteínas dentro de algunos viriones antes de que salgan de una célula infectada. Cuando estos genomas sembrados entran en una célula nueva, comienzan de inmediato a producir proteínas y a reunir más a su alrededor, nucleando rápidamente una fábrica viral y lanzando la replicación. Los genomas pasivos, en cambio, rara vez escapan a este estado de baja actividad a menos que se suministren proteínas virales adicionales. Este trabajo no solo aclara por qué las infecciones por VSR pueden variar tanto entre células, sino que también sugiere nuevas estrategias: fármacos que interrumpan estas semillas o su capacidad de condensarse podrían debilitar la infección en sus primeros pasos, y principios similares pueden regir cómo se forman muchas otras gotas biomoleculares relacionadas con enfermedades dentro de nuestras células.
Cita: Ratnayake, D., Galloux, M., Boersma, S. et al. Pre-assembly of biomolecular condensate seeds drives RSV replication. Nature 652, 189–200 (2026). https://doi.org/10.1038/s41586-025-10071-5
Palabras clave: virus respiratorio sincitial, fábricas virales, condensados biomoleculares, imagen de virus individual, heterogeneidad de la infección