Clear Sky Science · de
Vorassemblierung von biomolekularen Kondensatsamen treibt die RSV-Replikation an
Wie einige Viruspartikel einen Vorsprung bekommen
Das respiratorische Synzytialvirus (RSV) ist eine Hauptursache für Lungeninfektionen bei Säuglingen, älteren Erwachsenen und immungeschwächten Personen. Diese Studie stellt eine auf den ersten Blick einfache, aber folgenreiche Frage: Wenn ein einzelnes RSV-Partikel auf eine Zelle trifft, was entscheidet darüber, ob die Infektion sich entfaltet oder still ins Stocken gerät? Durch die Beobachtung einzelner viraler Genome in lebenden Zellen decken die Autoren verborgene Unterschiede zwischen Viruspartikeln auf, die erklären, warum manche Infektionen explosionsartig wachsen, während andere verkümmern.
Verborgene virale Tröpfchen in infizierten Zellen
Einmal in der Zelle angekommen, bauen viele RNA‑Viren, darunter RSV, winzige, membranfreie „virale Fabriken“ auf. Diese tropfenähnlichen Strukturen konzentrieren virale Komponenten und sind die Hauptorte, an denen neue virale Genome und Proteine hergestellt werden. Es gibt jedoch einen Haken: Solche Tröpfchen entstehen normalerweise erst, wenn die Proteinmengen bereits hoch sind, während zu Beginn einer Infektion virale Proteine knapp sind. Mit fortschrittlicher Fluoreszenzmikroskopie verfolgten die Forscher einzelne RSV‑Genomkomplexe, sogenannte vRNPs, ab dem Moment ihres Zellzutritts. Sie fanden heraus, dass virale Fabriken nicht aus dem Nichts auftauchen; vielmehr wachsen sie aus einzelnen eingehenden vRNPs, die allmählich anschwellen und zu größeren Tröpfchen verschmelzen.
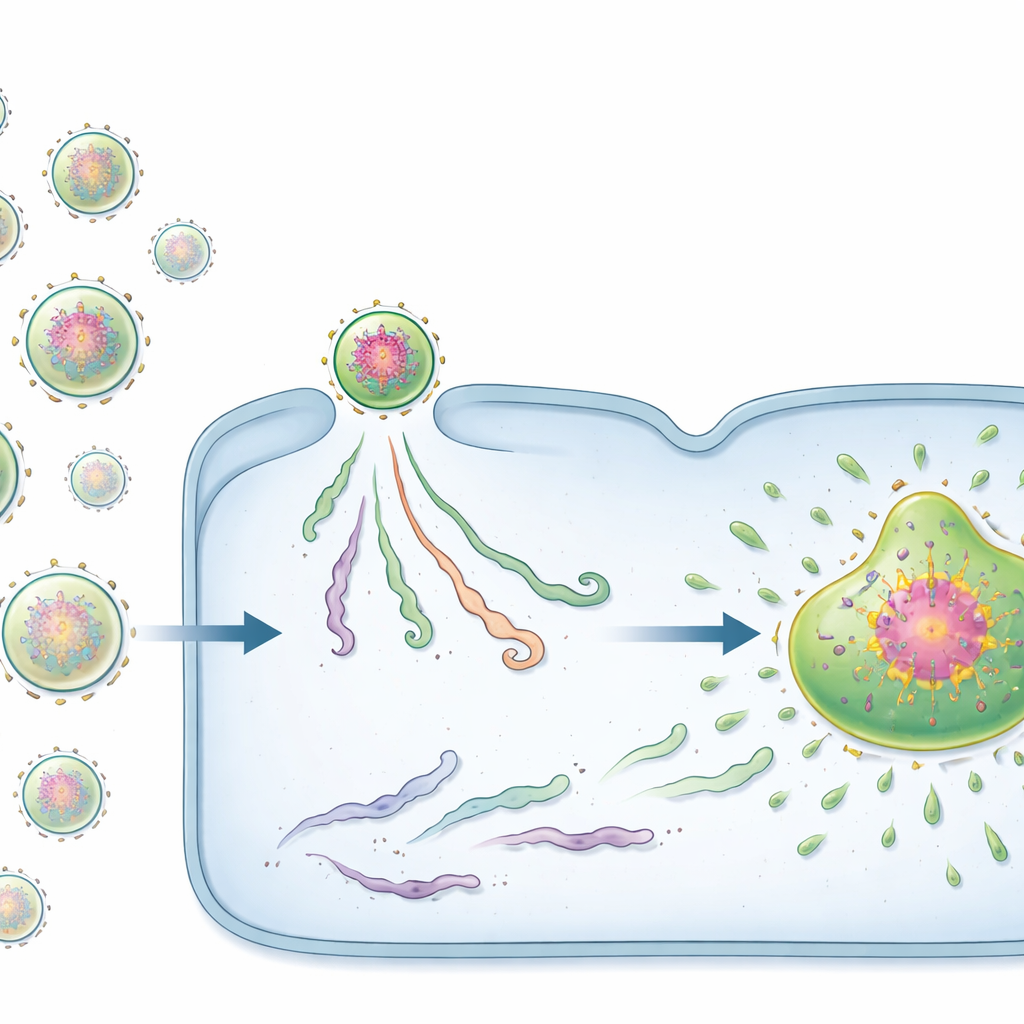
Zwei Arten viraler Starter: Samen und Passagiere
Überraschenderweise verhielten sich nicht alle eingehenden vRNPs gleich. Mit speziell entwickelten fluoreszierenden Sonden entdeckte das Team zwei verschiedene Zustände. Eine Minderheit der vRNPs trug bereits dichte Cluster viraler Proteine um das Genom herum. Diese proteinreichen Komplexe, die die Autoren als Prä‑Replikationszentren (PRCs) bezeichnen, fungierten als potente „Samen“ für virale Fabriken. Zellen, die von schon einem einzigen PRC infiziert wurden, bildeten fast immer eine Fabrik und produzierten zahlreiche Nachkommen‑Genome. Im Gegensatz dazu fehlte den meisten vRNPs dieses vorbeladene Proteinnetzwerk; sie wurden als passive vRNPs bezeichnet. Von passiven vRNPs initiierte Infektionen gerieten häufig ins Stocken: das virale Material blieb klein und isoliert, und es erschienen weder virale Fabriken noch Nachkommen‑Genome.
Warum Samen dort Erfolg haben, wo Passagiere scheitern
Durch Messung viraler Aktivität in Echtzeit zeigten die Autoren, dass PRCs sehr schnell und in deutlich höherer Rate virale Gene transkribieren als passive vRNPs. Detaillierte Bildgebung und biochemische Analysen erklärten warum. PRCs tragen erheblich mehr Kopien zentraler viraler Proteine—insbesondere der Polymerase und ihres Co‑Faktors—pro Genom als passive vRNPs, bereits bevor sie in die Zelle eintreten. Im Zytoplasma bleiben diese Proteine an PRCs gebunden, während sie von passiven vRNPs abfallen. PRCs wirken außerdem wie klebrige Gerüste, die zusätzliche virale Proteine und sogar andere vRNPs anziehen. Wenn Proteine akkumulieren, überschreiten PRCs die Schwelle zur Kondensation in ein tropfenartiges virales Fabrikat, wo die Genomreplikation schließlich eingeschaltet wird. Das schafft eine Vorwärtsverstärkung: mehr Proteine machen einen besseren Samen, der noch mehr Proteine einfängt und rasch zur Fabrik heranwächst.
Eingebaute Unterschiede zwischen Viruspartikeln
Die Studie zeigt ferner, dass von infizierten Zellen freigesetzte RSV‑Partikel nicht alle gleich sind. Einige Virionen verpacken mehrere vRNPs, und viele enthalten entweder überwiegend PRCs oder überwiegend passive vRNPs. Virionen, die an PRCs reich sind, führen deutlich häufiger zu einer produktiven Infektion in einer neuen Zelle. Diese „Virion‑Heterogenität“ wurde bei Laborstämmen, klinischen Isolaten und direkt aus infizierten Personen gesammelten Viren beobachtet, was darauf hindeutet, dass es sich um ein natürliches Merkmal der RSV‑Biologie handelt. Die Anzahl der Genome pro Partikel war weniger entscheidend als die Frage, ob wenigstens eines davon ein PRC war. Somit treibt wahrscheinlich eine kleine Untergruppe gut ausgestatteter Partikel die meisten erfolgreichen Infektionen an, während andere als unterlegene Passagiere wirken.
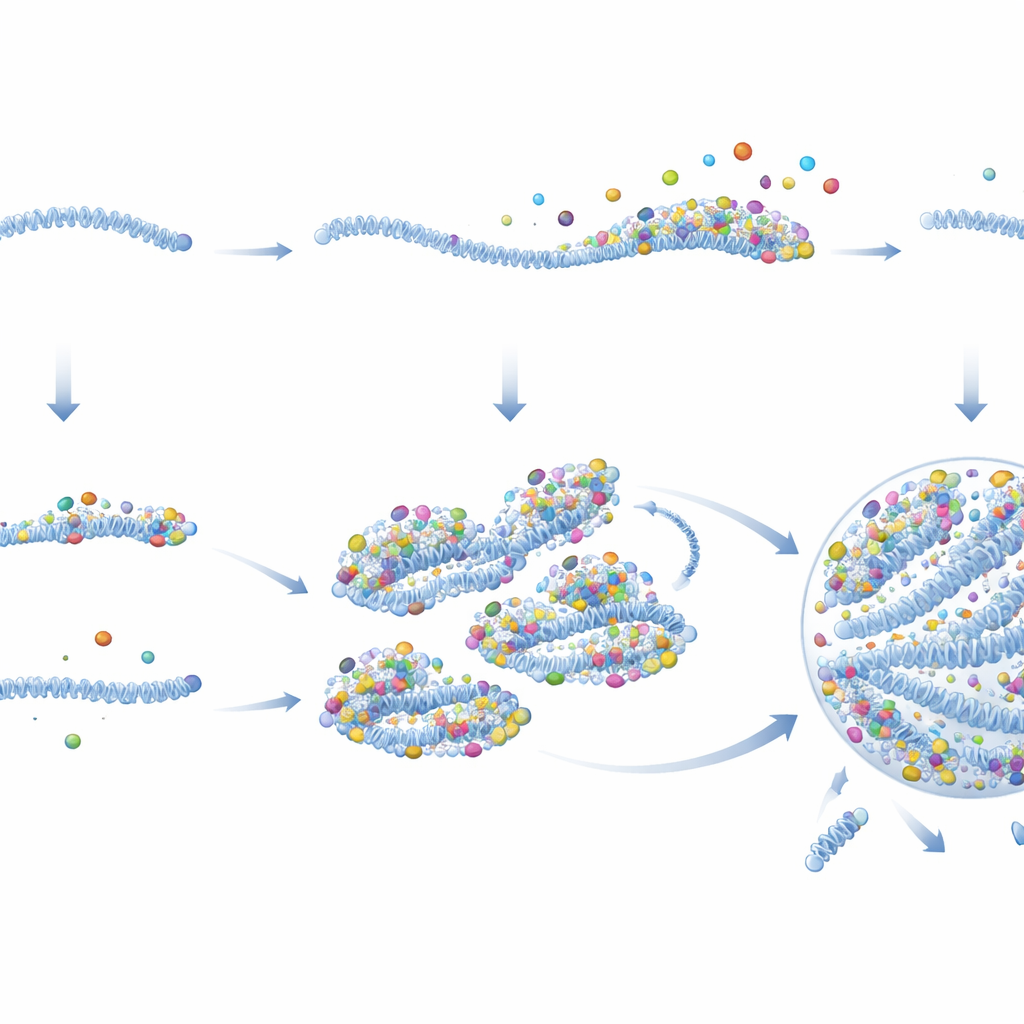
Warum das für Infektionen und darüber hinaus wichtig ist
Einfache gesagt kommen die Autoren zu dem Schluss, dass RSV ein scheinbares Henne‑und‑Ei‑Problem löst—es braucht hohe Proteinmengen, um virale Fabriken zu bauen, braucht aber Fabriken, um Proteine zu produzieren—indem es proteinreiche Samen bereits in einigen Virionen zusammenbaut, bevor diese eine infizierte Zelle verlassen. Wenn diese vorgeprägten Genome in eine neue Zelle eintreten, beginnen sie sofort mit der Proteinsynthese und sammeln weitere Proteine um sich, wobei sie schnell ein virales Fabrikat nukleieren und die Replikation starten. Passive Genome hingegen entkommen diesem Niedrigaktivitäts‑Zustand selten, es sei denn, es werden zusätzliche virale Proteine zugeführt. Diese Arbeit erklärt nicht nur, warum RSV‑Infektionen von Zelle zu Zelle so unterschiedlich verlaufen können, sondern schlägt auch neue Strategien vor: Wirkstoffe, die diese Samen oder deren Kondensationsfähigkeit stören, könnten die Infektion in ihren allerersten Schritten abschwächen, und ähnliche Prinzipien könnten steuern, wie viele andere krankheitsrelevante biomolekulare Tröpfchen in unseren Zellen entstehen.
Zitation: Ratnayake, D., Galloux, M., Boersma, S. et al. Pre-assembly of biomolecular condensate seeds drives RSV replication. Nature 652, 189–200 (2026). https://doi.org/10.1038/s41586-025-10071-5
Schlüsselwörter: respiratorisches Synzytialvirus, virale Fabriken, biomolekulare Kondensate, Einzelvirus-Bildgebung, Heterogenität der Infektion