Clear Sky Science · tr
Biomoleküler kondensat çekirdeklerinin önceden monte edilmesi RSV replikasyonunu tetikliyor
Bazı virüs partikülleri nasıl öne geçiyor
Respiratuar sinsityal virüs (RSV), bebeklerde, yaşlı yetişkinlerde ve bağışıklığı zayıf kişilerde akciğer enfeksiyonlarının başlıca nedenlerinden biridir. Bu çalışma, basit görünüp büyük sonuçları olan bir soruyu gündeme getiriyor: tek bir RSV partikülü bir hücreye yerleştiğinde, o enfeksiyonun yayılıp yayılmayacağını veya sessizce durup kalacağını ne belirler? Yazarlar, canlı hücrelerde bireysel viral genomları izleyerek, bazı enfeksiyonların patlamasına diğerlerinin sönmesine neden olan gizli farklılıkları ortaya koyuyor.
Enfekte hücrelerdeki gizli viral damlacıklar
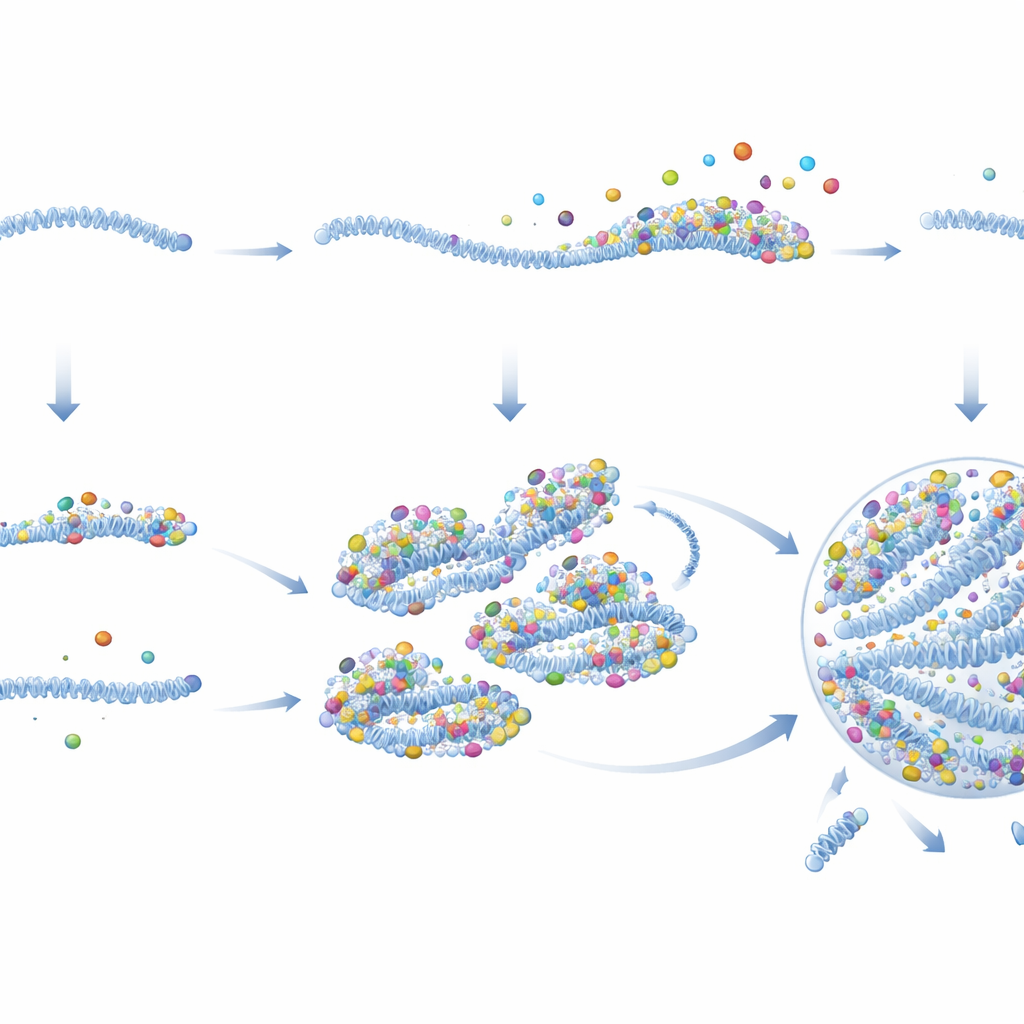
Bir hücreye girdikten sonra, RSV de dahil birçok RNA virüsü, küçük, membransız “viral fabrikalar” oluşturur. Bu damlacık benzeri yapılar viral bileşenleri yoğunlaştırır ve yeni viral genomlar ile proteinlerin üretildiği ana yerlerdir. Ama bir sorun vardır: bu tür damlacıklar genellikle protein seviyeleri zaten yüksek olduğunda oluşur; oysa enfeksiyonun erken döneminde viral proteinler nadirdir. Gelişmiş floresan mikroskopisi kullanarak araştırmacılar, hücrelere girdikleri andan itibaren vRNP adı verilen tek RSV genom komplekslerini izlediler. Viral fabrikaların hiçbir yerden aniden ortaya çıkmadığını; bunun yerine gelen tekil vRNP’lerin kademeli olarak şişip birbirleriyle kaynaşarak daha büyük damlacıklar hâline geldiğini buldular.
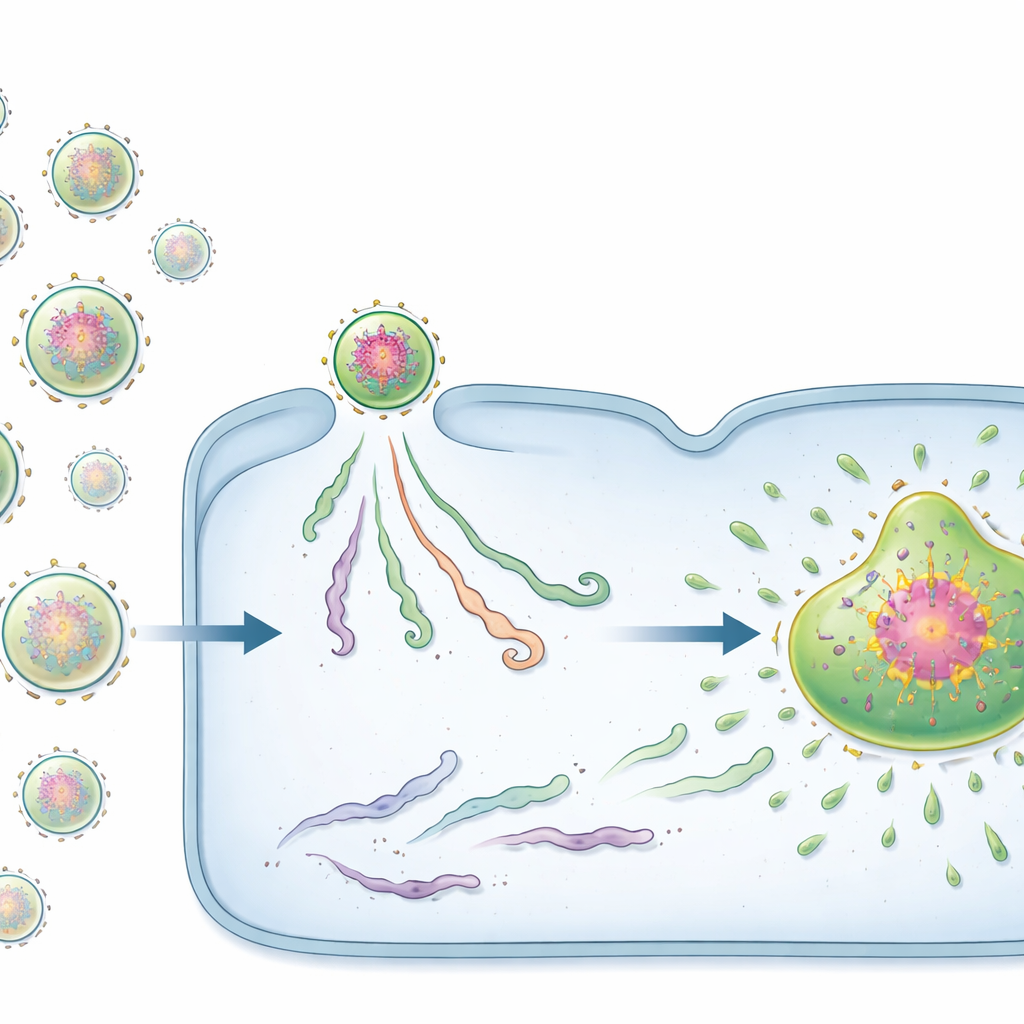
İki tür viral başlatıcı: çekirdekler ve yolcular
Şaşırtıcı şekilde, gelen tüm vRNP’ler aynı davranmadı. Özelleştirilmiş floresan problarla ekip, iki ayrı durum keşfetti. Azınlıkta olan bazı vRNP’ler genom etrafında zaten toplanmış yoğun viral protein kümeleri taşıyordu. Yazarların ön‑replikasyon merkezleri (ÖRM) diye adlandırdığı bu protein açısından zengin kompleksler, viral fabrikalar için güçlü “çekirdekler” gibi davrandı. Bir hücre tek bir ÖRM ile enfekte olduğunda neredeyse her zaman bir fabrika oluştu ve bol sayıda yeni genom üretildi. Buna karşılık, çoğu vRNP bu önceden yüklü protein ağından yoksundu ve pasif vRNP’ler olarak adlandırıldı. Pasif vRNP’lerin başlattığı enfeksiyonlar sıklıkla durakladı: viral materyal küçük ve izole kaldı, ne viral fabrika ne de türetilmiş genomlar ortaya çıktı.
Çekirdeklerin yolculardan üstün olmasının nedeni
Viral aktiviteyi gerçek zamanlı ölçerek yazarlar, ÖRM’lerin viral genleri hızla ve pasif vRNP’lere göre çok daha yüksek oranlarda transkribe etmeye başladığını gösterdi. Ayrıntılı görüntüleme ve biyokimyasal analizler bunun nedenini açıkladı. ÖRM’ler, özellikle polimeraz ve onun yardımcı faktörü olmak üzere, pasif vRNP’lere göre her genom başına önemli ölçüde daha fazla anahtar viral protein kopyası taşıyordu—hâlâ hücreye girmeden önce bile. Sitoplazmaya girdiklerinde bu proteinler ÖRM’lere bağlı kalırken, pasif vRNP’lerden kopuyordu. ÖRM’ler ayrıca ek viral proteinleri ve hatta diğer vRNP’leri çekebilen yapışkan iskeletler gibi davranıyordu. Proteinler biriktikçe ÖRM’ler damlacık‑benzeri bir viral fabrikaya yoğunlaşmak için gerekli eşik değeri aşıyor ve burada genome replike edilmeye başlanıyordu. Bu, besleme‑ileri döngüsü yaratıyordu: daha fazla protein daha iyi bir çekirdek yapıyor, bu çekirdek daha fazla proteini yakalıyor ve hızla bir fabrikaya dönüşüyordu.
Virüs partikülleri arasında yerleşik farklılıklar
Çalışma ayrıca enfekte hücrelerden salınan RSV partiküllerinin hepsinin eşit olmadığını gösteriyor. Bazı virionlar birden fazla vRNP paketler ve pek çoğu ağırlıklı olarak ya ÖRM ya da pasif vRNP içerir. ÖRM bakımından zengin virionlar yeni bir hücrede ürünü enfeksiyon başlatma olasılığı çok daha yüksek. Bu “virion heterojenitesi” laboratuvar suşlarında, klinik izolatlarda ve doğrudan enfekte kişilerden toplanan virüslerde görüldü; bu da bunun RSV biyolojisinin doğal bir özelliği olduğunu düşündürüyor. Partikül başına düşen genom sayısı, en az birinin ÖRM olup olmadığı kadar önemli değildi. Böylece iyi donanımlı küçük bir parçacık alt grubu muhtemelen çoğu başarılı enfeksiyonu yönlendiriyor, diğerleri ise yetersiz güçte yolcu olarak görev yapıyor.
Bu bulgunun enfeksiyon ve ötesi için önemi
Basitçe söylemek gerekirse yazarlar, RSV’nin görünürdeki tavuk‑yumurta sorununu—viral fabrikalar kurmak için yüksek protein seviyelerine ihtiyaç duyması ama protein yapmak için fabrikalara ihtiyaç duyması—çözümlediğini öne sürüyor: Enfekte bir hücreden ayrılmadan önce bazı virionların içinde protein açısından zengin çekirdekleri önceden monte ediyor. Bu çekirdeklenmiş genomlar yeni bir hücreye girdiklerinde derhal protein üretmeye başlıyor ve etraflarında daha fazla protein biriktirerek hızla bir viral fabrika nucleate ediyor ve replikasyonu başlatıyor. Buna karşın pasif genomlar, ek viral protein sağlanmadıkça nadiren bu düşük‑aktiflik durumundan kurtuluyor. Bu çalışma yalnızca RSV enfeksiyonlarının hücreden hücreye neden bu kadar değişken olduğunu açıklamakla kalmıyor, aynı zamanda yeni stratejiler de öneriyor: bu çekirdekleri veya onların yoğunlaşma yeteneğini bozan ilaçlar, enfeksiyonu daha ilk adımlarında zayıflatabilir ve benzer ilkelerin hücrelerimizde oluşan diğer hastalıkla ilişkili biomoleküler damlacıkların oluşumunu da yönlendirebileceğini düşündürüyor.
Atıf: Ratnayake, D., Galloux, M., Boersma, S. et al. Pre-assembly of biomolecular condensate seeds drives RSV replication. Nature 652, 189–200 (2026). https://doi.org/10.1038/s41586-025-10071-5
Anahtar kelimeler: respiratuar sinsityal virüs, viral fabrikalar, biomoleküler kondensatlar, tek virüs görüntüleme, enfeksiyon heterojenitesi