Clear Sky Science · sv
Förmontering av biomolekylära kondensatfrön driver RSV-replikation
Hur vissa viruspartiklar får ett försprång
Respiratoriskt syncytialvirus (RSV) är en huvudorsak till lunginfektioner hos spädbarn, äldre och personer med försvagat immunförsvar. Denna studie ställer en till synes enkel fråga med stora konsekvenser: när en enskild RSV-partikel landar på en cell, vad avgör om den infektionen tar fart eller tyst dör ut? Genom att följa individuella virala genom i levande celler avslöjar författarna dolda skillnader mellan partklar som förklarar varför vissa infektioner exploderar medan andra slocknar.
Dolda virala droppar inne i infekterade celler
När de väl är inne i en cell bygger många RNA-virus, inklusive RSV, små membranfria ”virala fabriker”. Dessa dropp-liknande strukturer koncentrerar virala komponenter och är huvudplatserna där nya virala genom och proteiner tillverkas. Men det finns en hake: sådana droppar bildas vanligtvis först när proteinnivåerna redan är höga, medan virusproteiner är sällsynta tidigt i infektionen. Med avancerad fluorescensmikroskopi följde forskarna enskilda RSV-genomkomplex, kallade vRNPs, från det ögonblick de trädde in i cellerna. De fann att virala fabriker inte uppstår ur intet; i stället växer de utifrån individuella inkommande vRNPs som gradvis sväller och smälter samman till större droppar.
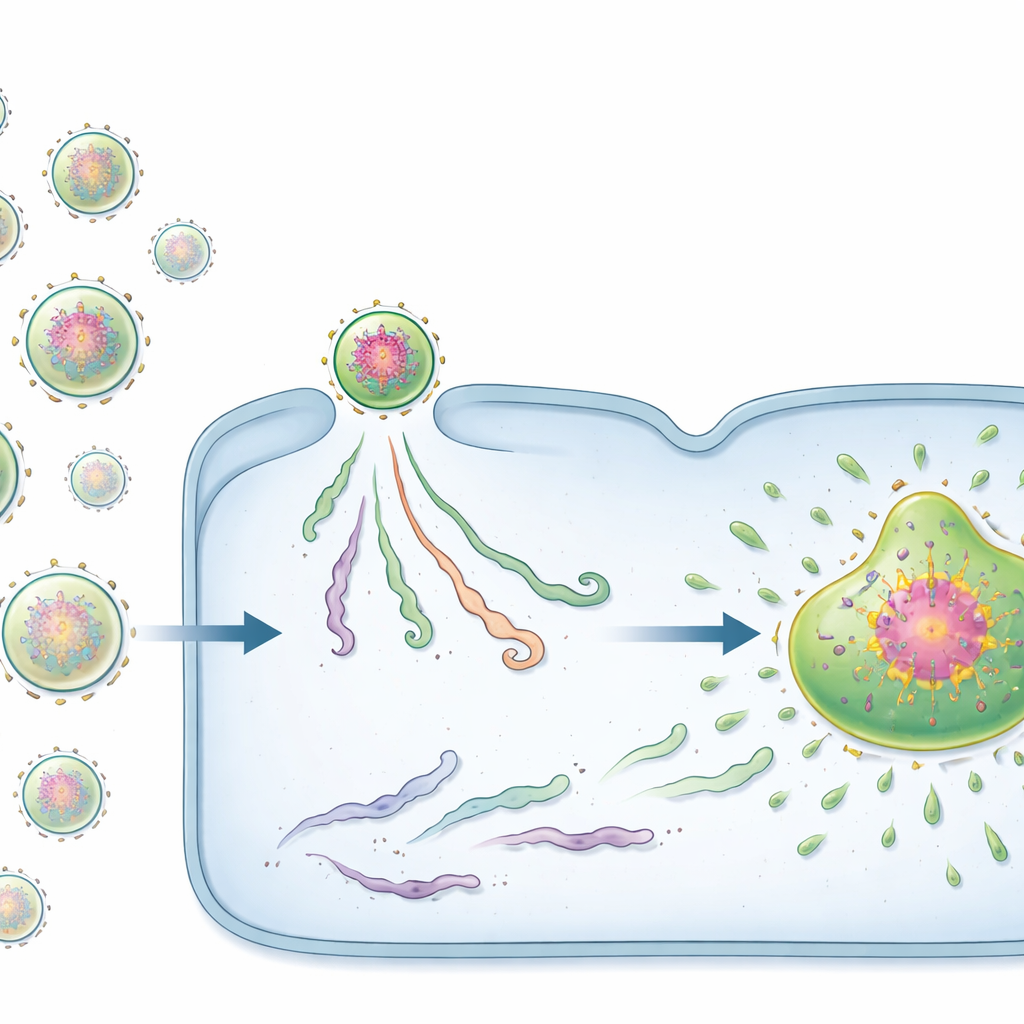
Två typer av virala startare: frön och passagerare
Överraskande nog uppträdde inte alla inkommande vRNPs likadant. Med särskilt konstruerade fluorescerande prober upptäckte teamet två distinkta tillstånd. En minoritet av vRNPs bar täta kluster av virala proteiner redan monterade runt genomet. Dessa proteinrika komplex, som författarna kallar för pre‑replikationscentra (PRC), fungerade som kraftfulla ”frön” för virala fabriker. Celler som infekterades av även ett enda PRC bildade nästan alltid en fabrik och producerade stora mängder avkommegenom. I kontrast saknade de flesta vRNPs detta förladdade proteinnätverk och betecknades som passiva vRNPs. Infektioner som startade från passiva vRNPs stannade ofta av: det virala materialet förblev litet och isolerat, och ingen viral fabrik eller avkommegenom uppträdde.
Varför frön lyckas där passagerare misslyckas
Genom att mäta viral aktivitet i realtid visade författarna att PRC snabbt börjar transkribera virusgener och i mycket högre takt än passiva vRNPs. Detaljerad avbildning och biokemiska analyser förklarade varför. PRC bär avsevärt fler kopior av nyckelvirusproteiner—särskilt polymeraset och dess cofaktor—per genom än passiva vRNPs, redan innan de kommer in i cellen. Väl i cytoplasman förblir dessa proteiner bundna till PRC men lossnar från passiva vRNPs. PRC fungerar också som kletiga ställningar som drar till sig ytterligare virala proteiner och till och med andra vRNPs. När proteiner ackumuleras korsar PRC tröskeln som krävs för att kondensera till en dropp‑liknande viral fabrik, där genomreplikation slutligen slås på. Detta skapar en framåtriktad loop: fler proteiner gör ett bättre frö, som fångar ännu fler proteiner och snabbt växer till en fabrik.
Inbyggda skillnader mellan viruspartiklar
Studien visar vidare att RSV-partiklar som släpps från infekterade celler inte är likadana. Vissa virioner packar flera vRNPs, och många innehåller antingen mestadels PRC eller mestadels passiva vRNPs. Virioner som är rika på PRC är mycket mer benägna att initiera en produktiv infektion i en ny cell. Denna ”virion‑heterogenitet” observerades hos laboratoriestammar, kliniska isolat och virus samlade direkt från infekterade människor, vilket tyder på att det är en naturlig egenskap hos RSV‑biologin. Antalet genom per partikel spelade mindre roll än om minst ett av dem var ett PRC. Således driver sannolikt en liten undergrupp av välutrustade partiklar de flesta lyckade infektionerna, medan andra fungerar som underutrustade passagerare.
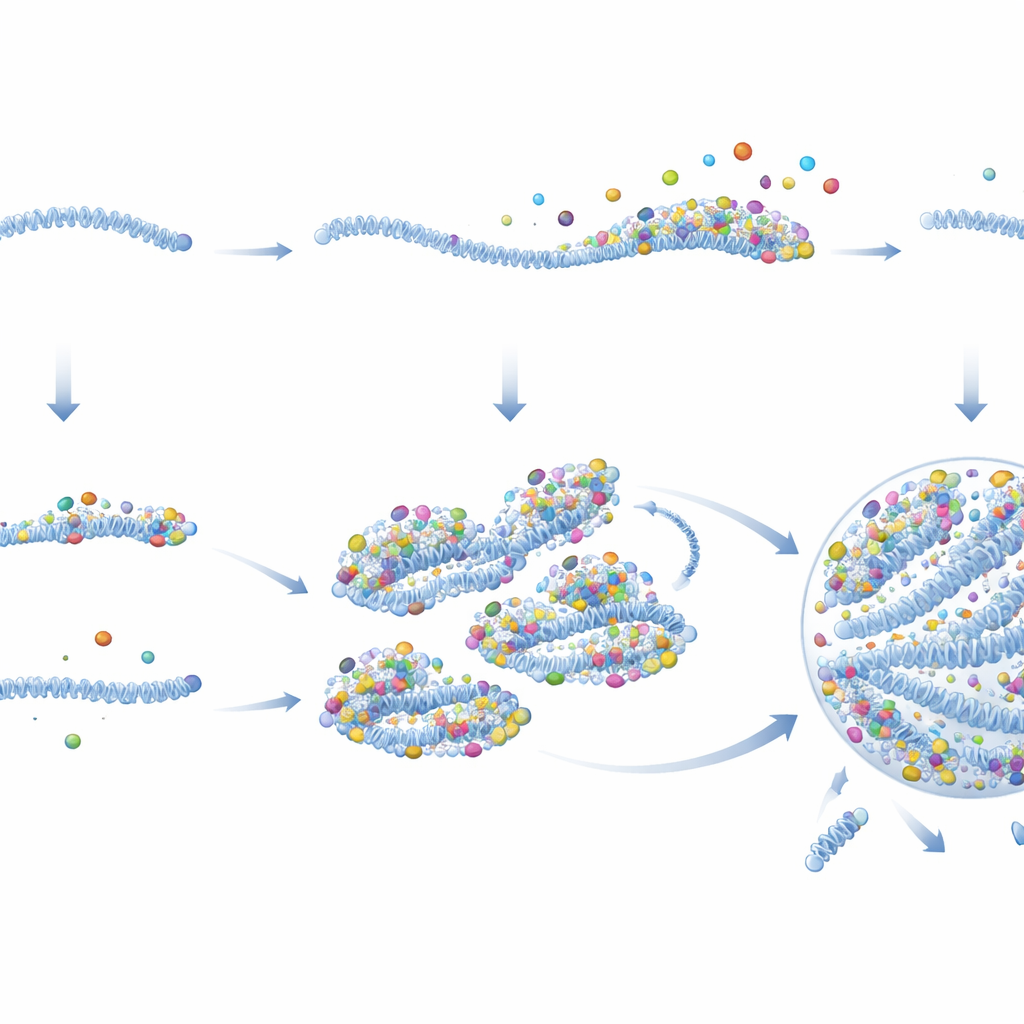
Varför detta är viktigt för infektion och vidare
Enklare uttryckt drar författarna slutsatsen att RSV löser ett till synes hönan‑och‑ägget‑problem—att behöva höga proteinnivåer för att bygga virala fabriker, men behöva fabriker för att göra proteiner—genom att förmontera proteinrika frön inuti vissa virioner innan de lämnar en infekterad cell. När dessa försedda genom kommer in i en ny cell börjar de omedelbart producera proteiner och samla fler runt sig, snabbt nukleera en viral fabrik och starta replikation. Passiva genom hamnar däremot sällan ur detta låga‑aktivitetstillstånd om inte extra virala proteiner tillförs. Detta arbete klargör inte bara varför RSV‑infektioner kan variera så mycket från cell till cell, utan pekar också på nya strategier: läkemedel som stör dessa frön eller deras förmåga att kondensera skulle kunna dämpa infektionen i dess allra första steg, och liknande principer kan styra hur många andra sjukdomsrelaterade biomolekylära droppar bildas inom våra celler.
Citering: Ratnayake, D., Galloux, M., Boersma, S. et al. Pre-assembly of biomolecular condensate seeds drives RSV replication. Nature 652, 189–200 (2026). https://doi.org/10.1038/s41586-025-10071-5
Nyckelord: respiratoriskt syncytialvirus, virala fabriker, biomolekylära kondensat, avbildning av enskilda virus, heterogenitet i infektion