Clear Sky Science · ja
バイオ分子凝縮体のシードの事前組み立てがRSV複製を促進する
ウイルス粒子の一部が先手を取る仕組み
呼吸器合胞体ウイルス(RSV)は、乳児、高齢者、免疫力が低下した人々における肺感染症の主要な原因です。本研究は一見単純だが重要な問いを投げかけます:単一のRSV粒子が細胞に着地したとき、どの要因がその感染が拡大するか、あるいは静かに停滞するかを決めるのか?生細胞内で個々のウイルスゲノムを観察することで、著者らはウイルス粒子間の隠れた差異を明らかにし、なぜ一部の感染が爆発的に増えるのに対し他はしぼんでしまうのかを説明しています。
感染細胞内部に隠れたウイルス性ドロップレット
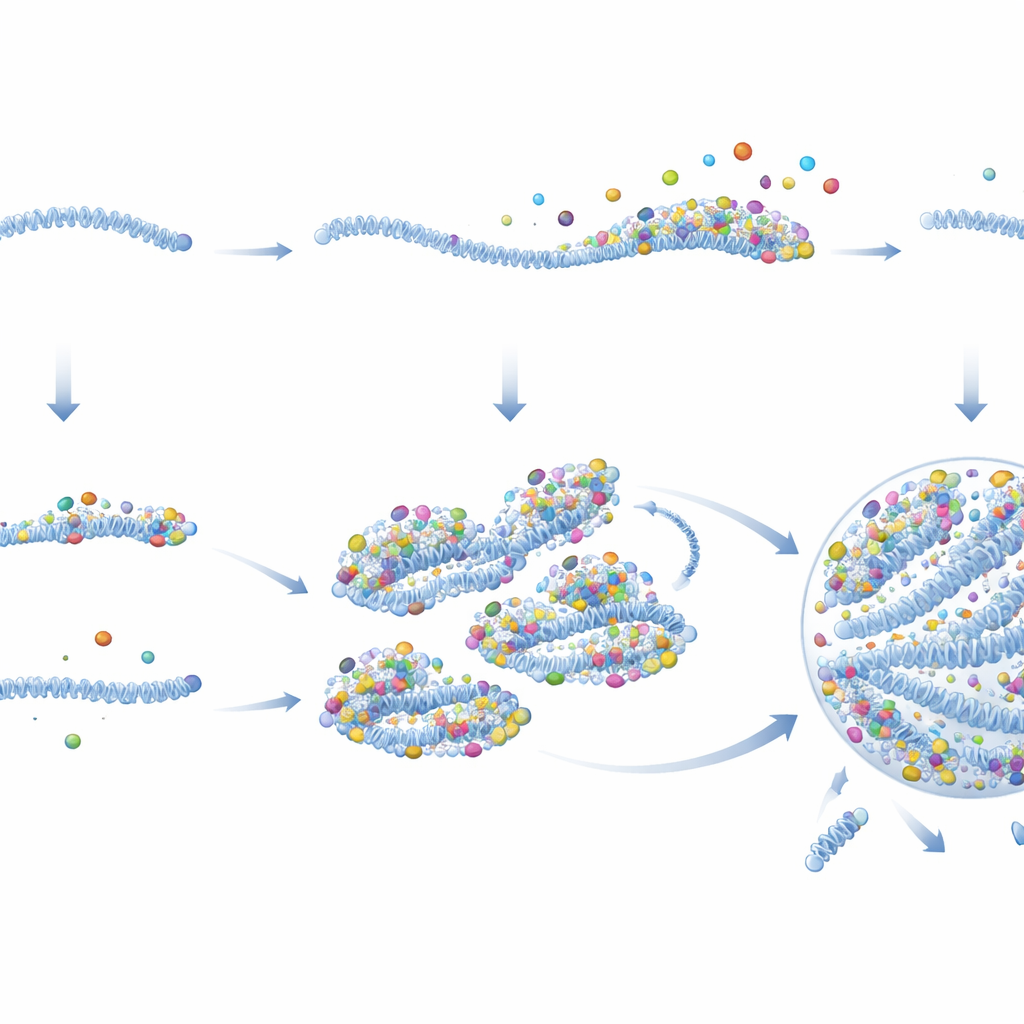
細胞内に入ると、多くのRNAウイルス(RSVを含む)は小さな膜を持たない「ウイルスファクトリー」を作ります。これらの液滴状構造はウイルス成分を濃縮し、新しいウイルスゲノムやタンパク質が主に作られる場所です。しかし問題があります:こうした液滴は通常タンパク質量がある程度高くなってから形成される一方で、感染初期にはウイルスタンパク質は稀です。高性能蛍光顕微鏡を用いて、研究者らは細胞に入った瞬間から単一のRSVゲノム複合体(vRNP)を追跡しました。彼らはウイルスファクトリーが突然出現するのではなく、個々の侵入vRNPが徐々に膨張し融合してより大きな液滴へと成長していくことを見出しました。
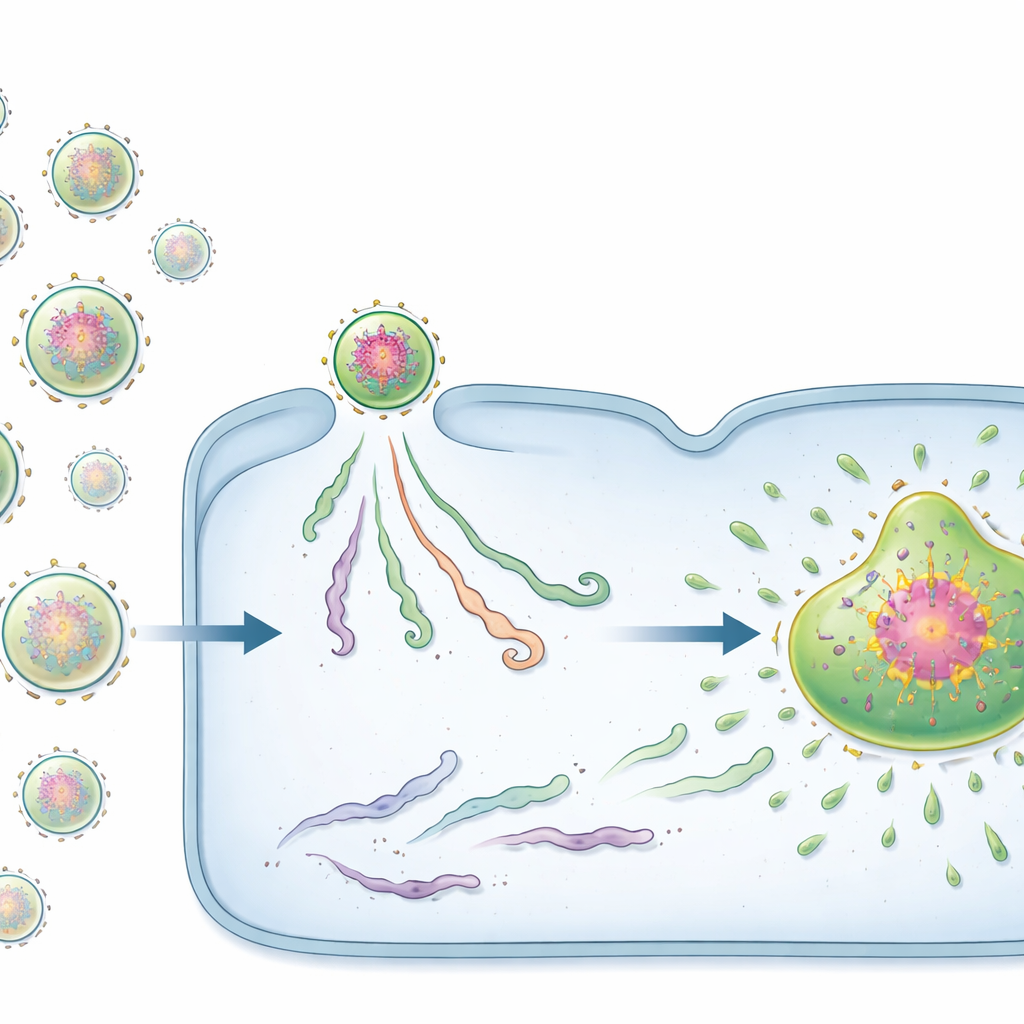
二種類のウイルス起動子:シードとパッセンジャー
驚くべきことに、すべての侵入vRNPが同じ振る舞いをするわけではありませんでした。特別に設計した蛍光プローブを用いて、チームは二つの明確な状態を発見しました。少数のvRNPはすでにゲノムの周りに密なウイルスタンパク質クラスターを備えていました。著者らはこれらのタンパク質に富む複合体をプレ複製中心(PRC)と呼び、強力な“シード”としてウイルスファクトリーの核となりました。たとえ単一のPRCによって感染が始まっても、細胞はほとんど確実にファクトリーを形成し、多数の子孫ゲノムを生産しました。対照的に、大多数のvRNPはこの予め装填されたタンパク質ネットワークを欠いており、受動的vRNPと名付けられました。受動的vRNPによって始まった感染は頻繁に停滞しました:ウイルス性物質は小さく孤立したままで、ウイルスファクトリーも子孫ゲノムも出現しませんでした。
なぜシードは成功しパッセンジャーは失敗するのか
ウイルス活動をリアルタイムで計測することで、著者らはPRCが受動的vRNPよりも速やかに、かつはるかに高いレートで遺伝子転写を開始することを示しました。詳細なイメージングと生化学的解析がその理由を明らかにしました。PRCは、特にポリメラーゼとその補因子など、重要なウイルスタンパク質をゲノム当たりかなり多く保持しており、受動的vRNPよりも多くのタンパク質を保持していました。細胞質に入ると、これらのタンパク質はPRCに結合したままですが、受動的vRNPからは外れてしまいます。PRCはさらに粘着性のある足場のように振る舞い、追加のウイルスタンパク質や他のvRNPさえも引き寄せます。タンパク質が蓄積すると、PRCは液滴状のウイルスファクトリーに凝縮するために必要な閾値を超え、そこでゲノム複製がようやくオンになります。これがフィードフォワードループを生み出します:より多くのタンパク質がより良いシードを作り、それがさらに多くのタンパク質を取り込み急速にファクトリーへと成長するのです。
ウイルス粒子間の生来の違い
さらに研究は、感染細胞から放出されるRSV粒子が均一ではないことを示しています。いくつかのビリオンは複数のvRNPをパッケージし、多くは主にPRCを含むか主に受動的vRNPを含んでいます。PRCに富むビリオンは新たな細胞で生産的な感染を開始する可能性がはるかに高いです。この「ビリオンの不均一性」は、実験室株、臨床分離株、そして感染者から直接採取したウイルス群にわたって観察され、RSV生物学の自然な特徴であることを示唆します。粒子当たりのゲノム数は、少なくともそのうちの1つがPRCであるかどうかほど重要ではありませんでした。したがって、装備の整った少数の粒子がおそらく大多数の成功した感染を駆動し、他は十分な力を持たないパッセンジャーとして作用する可能性が高いのです。
感染とそれを超えてなぜ重要か
簡潔に言えば、著者らはRSVが一見するとニワトリと卵の問題を解決していると結論づけています——ウイルスファクトリーを作るのに高いタンパク質量が必要だが、タンパク質を作るにはファクトリーが必要である、という問題です。RSVは感染細胞を離れる前に一部のビリオン内部でタンパク質に富むシードを事前に組み立てることでこれを回避します。こうしたシード化されたゲノムが新しい細胞に入ると、即座にタンパク質を生産し周囲にさらにタンパク質を集め、迅速にウイルスファクトリーを核形成して複製を開始します。これに対して受動的なゲノムは、追加のウイルスタンパク質が供給されない限り、この低活動状態から脱することはまれです。本研究はRSV感染が細胞ごとに大きく異なる理由を明らかにするだけでなく、新たな戦略を示唆します:これらのシードやそれらの凝縮能を阻害する薬剤は、感染のごく初期段階で作用して感染を鈍らせる可能性があり、同様の原理が多くの他の疾患関連バイオ分子ドロップレットが細胞内で形成される仕組みを支配しているかもしれません。
引用: Ratnayake, D., Galloux, M., Boersma, S. et al. Pre-assembly of biomolecular condensate seeds drives RSV replication. Nature 652, 189–200 (2026). https://doi.org/10.1038/s41586-025-10071-5
キーワード: 呼吸器合胞体ウイルス, ウイルスファクトリー, バイオ分子凝縮体, 単一ウイルスイメージング, 感染の不均一性