Clear Sky Science · zh
释放计算表型药物发现的潜力:方法、挑战与未来方向
为何这种新药物发现方式至关重要
大多数新药在从实验室到临床的过程中失败,即便投入多年时间和巨额成本仍难奏效。本文介绍了一种日益兴起的替代方案——表型药物发现,它关注化合物如何改变整个细胞或有机体的行为,而不是仅针对预先选定的单一分子。在人工智能和大型生物学数据集的帮助下,这一方法有望发现传统方法难以攻克的复杂疾病的治疗途径。
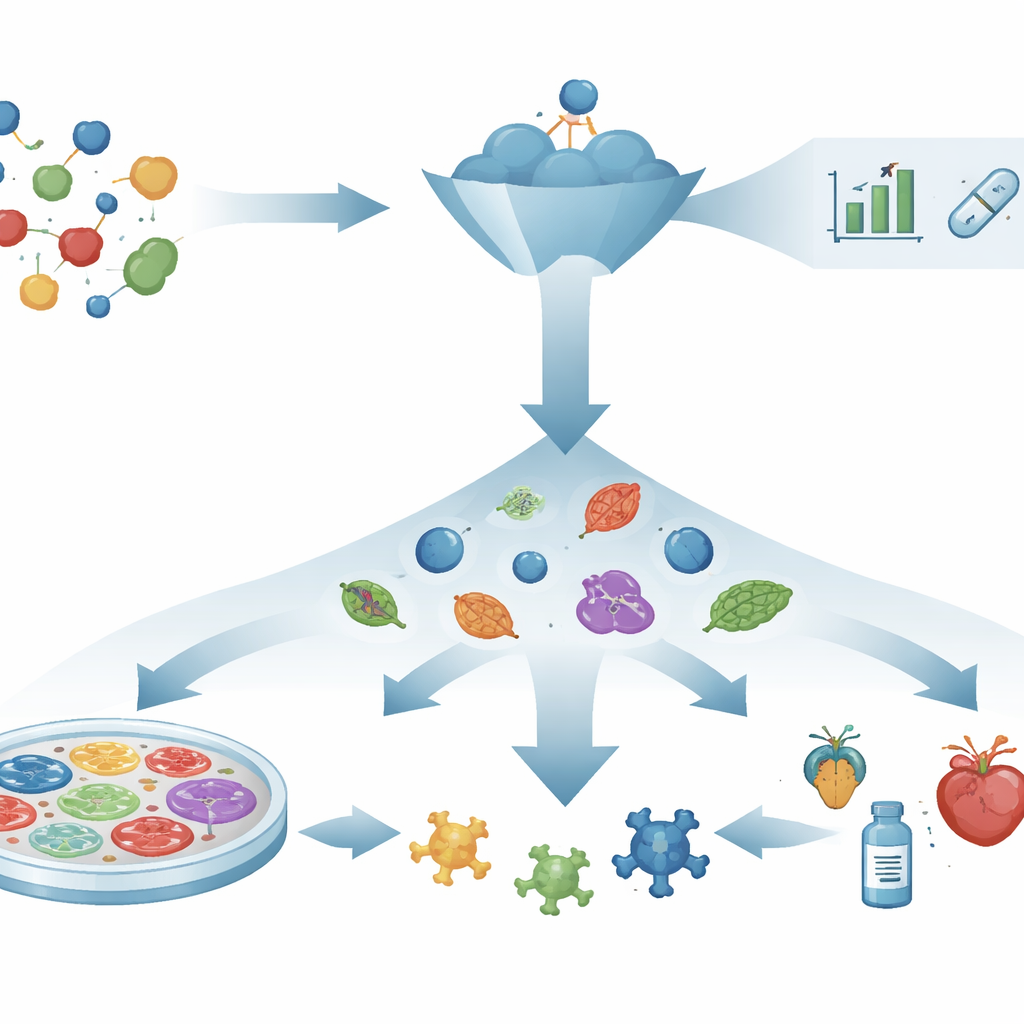
从“锁与钥匙”思维到观察生命系统
几十年来,药物发现遵循一种“机制优先”剧本:选择被认为驱动疾病的单一蛋白,设计或筛选与之结合的化学物质,然后期望这些相互作用能转化为真实的健康收益。蛋白质结构预测、计算辅助设计和虚拟筛选等强大工具加速了这一过程。然而,许多精心挑选的靶点和有前景的分子仍未能帮助患者,因为仅改变一个分子并不总能修复复杂交织的疾病网络。试管内成功与人体疗效之间的这一差距促使人们重新关注那些着眼于生命系统中实际发生情况的策略。
以化合物为先来发现有益变化
表型药物发现颠覆了传统思路。它不是从已知靶点出发,而是直接问一个问题:化合物是否能将病态系统推回健康状态?研究者将细胞、组织或小型生物暴露于大量化合物,寻找可见或可测量的变化,例如细胞形态恢复、脆弱细胞存活或行为恢复正常。只有在观察到有前景的效应后,科学家才进一步研究化合物在细胞内的作用机制。这种不依赖特定靶点的方法已促成若干药物的发现,例如用于囊性纤维化和脊髓性肌萎缩症的治疗,且其详细机制是在之后才被阐明。对于由多条通路共同驱动的疾病,单一“主”靶点不可行时,这一方法尤为有用。
将丰富的生物读数转化为数字
现代表型筛选产生海量数据:染色细胞的高分辨率图像、基因活性读数、蛋白质变化图谱,甚至模型生物的行为记录。为了理解这种复杂性,该领域依赖于“嵌入”技术——将化学、图像、基因表达和相互作用网络转换为紧凑的数值指纹。这些指纹捕捉药物外观、对细胞的改变以及与基因和疾病之间联系的模式。随后,从经典算法到深度神经网络和图形方法的机器学习模型学习将这些指纹与毒性、潜在疗效或与已知药物的相似性等结果关联起来。在某些情况下,它们甚至能建议新化合物或现有药物的新用途。
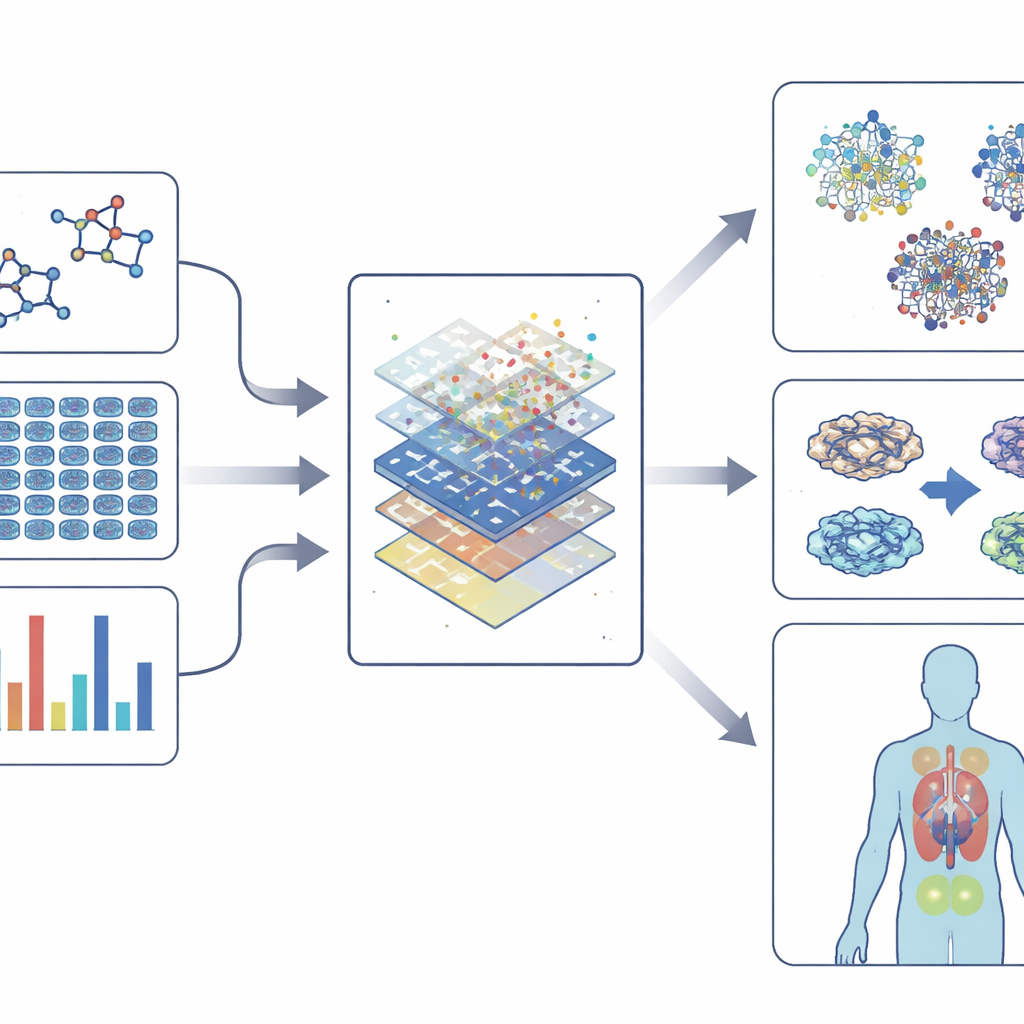
使用更智能的模型同时保持可解释性
随着模型变得更强大,它们也可能变得更不透明。可解释的人工智能工具旨在打开这个黑箱,突出哪些特征——例如特定的基因变化或分子结构片段——推动了某项预测。这种透明性帮助研究人员信任模型、设计更安全的化合物,并理解表型效应发生的原因,而不仅仅是知道它发生了。同时,单细胞和多组学技术使科学家能够看到组织中不同细胞类型对药物的响应,从而使该领域更接近个体化治疗选择。
通往更好药物的道路上的障碍
尽管前景可观,表型药物发现面临重大挑战。高质量数据集仍然零散且不同实验室间不一致,这使得训练出具有良好泛化能力的模型变得困难。复杂的表型实验难以复现,而从细胞或动物中的命中转向对人类安全有效的治疗常常暴露出隐藏的缺陷。弄清表型命中的作用机制——即所谓的靶点去卷积——可能既缓慢又不确定,尤其是在化合物同时作用于多条通路时。失败或被重新定位的药物个案研究强调了缺失或误解机制如何导致试验浪费或意外副作用。
这一方法的下一个发展方向
文章总结认为,表型药物发现的真正力量将来自将丰富的生物学模型与先进计算相结合。来源于患者的干细胞、三维微型器官和精细成像可以提供更接近人体的测试系统,而生成式人工智能可能提出针对特定疾病特征量身定制的分子,即使在数据有限的罕见病情况下亦然。如果能够解决数据质量、验证和机制发现等问题,这种以化合物为先、具有系统意识的策略有望使药物发现更快、更高效,并更贴近疾病在真实患者中的表现。
引用: Kumar, S., Pal, A. & Chatterjee, S. Unlocking the potential of computational phenotypic drug discovery: methods, challenges, and future directions. npj Syst Biol Appl 12, 46 (2026). https://doi.org/10.1038/s41540-026-00676-5
关键词: 表型药物发现, 药物发现中的机器学习, 药物重定位, 高内涵筛选, 计算药理学