Clear Sky Science · he
שחרור הפוטנציאל של גילוי תרופות פנוטיפי חישובי: שיטות, אתגרים וכיוונים עתידיים
מדוע השיטה החדשה הזאת לגילוי תרופות חשובה
רוב התרופות החדשות נופלות בשלב כלשהו בין המבחנה לקליניקה, גם אחרי שנים של עבודה ועלויות עצומות. מאמר זה מסביר אלטרנטיבה מתפתחת שנקראת גילוי תרופות פנוטיפי, המתמקדת בשינויי התנהגות בתאים או באורגניזמים שלמים במקום ביעד מולקולרי שנבחר מראש. בעזרת בינה מלאכותית ומאגרי נתונים ביולוגיים נרחבים, גישה זו עשויה לחשוף טיפולים למחלות מורכבות שהתנגדו לשיטות המסורתיות.
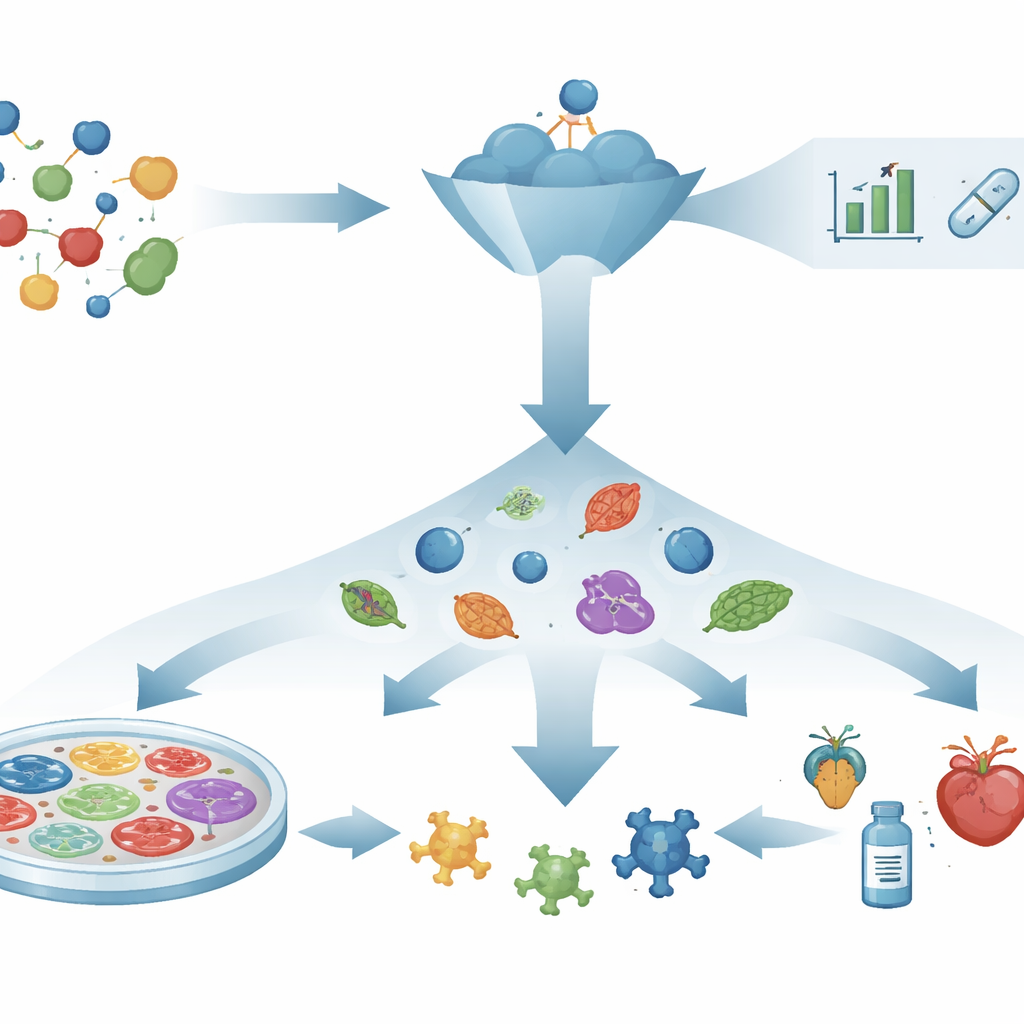
מחשבת המנעול והמפתח לצפייה במערכות חיות
בעשרות השנים האחרונות, גילוי תרופות התנהל לפי תסריט של "מנגנון קודם": בוחרים חלבון אחד שמאמינים שהוא מניע את המחלה, מעצבים או מחפשים חומרים שמתחברים אליו, ומקווים שאינטראקציות אלו יתורגמו להטבות רפואיות. כלים חזקים כמו חיזוי מבנה חלבון, תכנון בעזרת מחשב וסריקה וירטואלית האיצו את החיפוש הזה. עם זאת, מטרות שנבחרו בקפידה ומולקולות מבטיחות רבות עדיין לא עזרו לחולים, כי שינוי של מולקולה אחת לא תמיד פותר רשת מחלתית מסובכת. הפער בין הצלחה בצינוריות להצלחה באנשים עורר עניין מחודש באסטרטגיות המתמקדות במה שקורה בפועל במערכות חיות.
גישה שמתחילה בחיבור — לזהות שינויים מועילים
גילוי תרופות פנוטיפי הופך את התסריט: במקום להתחיל ביעד ידוע, נשאלת שאלה ישירה יותר: האם חומר מסוים דוחף מערכת חולה חזרה לכיוון בריאות? חוקרים חושפים תאים, רקמות או אורגניזמים קטנים להרבה חומרים ומחפשים שינויים נראים או נמדדים, כמו שחזור צורת תא, הישרדות של תאים רגישים או שחזור התנהגות נורמלית. רק אחרי שנראה אפקט מבטיח חוקרים בודקים איך החומר פועל בתוך התא. גישה שאינה תלויה ביעד זו כבר הובילה לתרופות, כמו טיפולים לציסטיק פיברוזיס ולניוון שרירים ספינלי, שמנגנוניהם המפורטים הורחבו מאוחר יותר. היא שימושית במיוחד למחלות שמונעות על ידי מסלולים רבים בו‑זמנית, שבהן בחירת "יעד ראשי" בודד היא לא ריאליסטית.
הפיכת קריאות ביולוגיות עשירות למספרים
מסכי פנוטיפ מודרניים מייצרים כמות עצומה של נתונים: תמונות ברזולוציה גבוהה של תאים מוכתמים, קריאות של פעילות גנים, מפות של שינויים בחלבונים ואף התנהגות של אורגניזמים מודליים. כדי לפענח את המורכבות הזו, התחום נשען על "הטמעות" — דרכים להמיר כימיה, תמונות, ביטוי גנים ורשתות אינטראקציות לטביעות אצבע נומריות דחוסות. טביעות אלה קולקות דפוסים באופן שבו תרופות נראות, כיצד הן משנות תאים ואיך הן מתקשרות עם גנים ומחלות. מודלים של למידת מכונה, מאלגוריתמים קלאסיים ועד רשתות עצביות עמוקות ושיטות גרפ‑מבוססות, לומדים לקשר טביעות אלה לתוצאות כמו רעילות, תועלת צפויה או דמיון לתרופות ידועות. במקרים מסוימים הם אף יכולים להציע מולקולות חדשות או שימושים חדשים לחומרים קיימים.
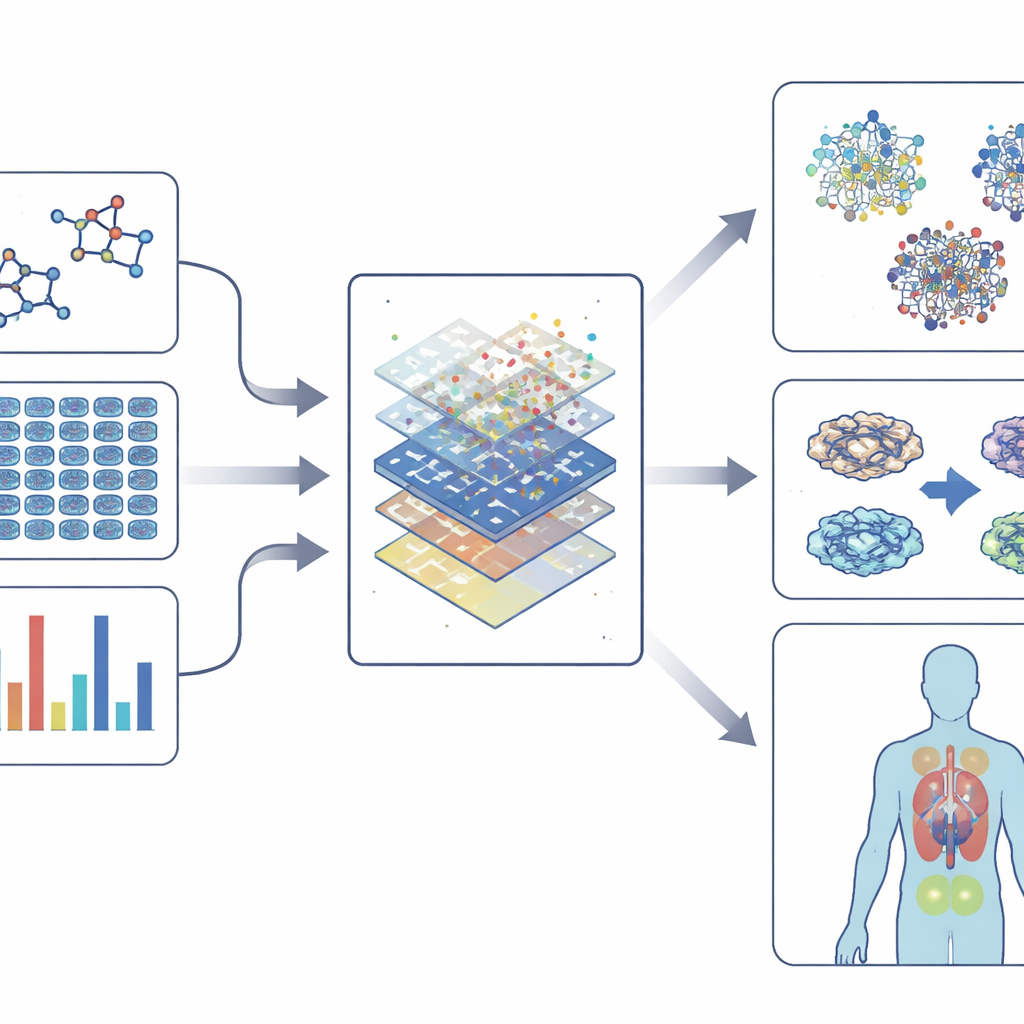
שימוש במודלים חכמים תוך שמירה על הבהירות שלהם
ככל שהמודלים מתעצמים, הם גם עלולים להפוך לאפלים יותר. כלים של בינה מוסברת שואפים לפתוח את התיבה השחורה הזו על‑ידי הדגשת תכונות — כמו שינויים בגנים מסוימים או חלקים מבניים של מולקולה — שמניעות את התחזית. השקיפות הזו עוזרת לחוקרים להסתמך על המודלים, לעצב תרכובות בטוחות יותר ולהבין מדוע מתרחש אפקט פנוטיפי, לא רק שהוא קורה. במקביל, טכנולוגיות של תא יחיד ורב‑אומיקס מאפשרות למדענים לראות כיצד סוגי תאים שונים ברקמה מגיבים לתרופה, ובכך לקרב את התחום להחלטות טיפול מותאמות אישית.
מכשולים בדרך לתרופות טובות יותר
למרות ההבטחה, גילוי תרופות פנוטיפי עומד בפני אתגרים משמעותיים. מערכי נתונים איכותיים עדיין מפוזרים וחסרים עקביות בין מעבדות, מה שמקשה על אימון מודלים שמכלילים היטב. ניסויי פנוטיפ מורכבים עלולים להיות קשים לשכפל, וממעבר מממצא בתאים או בחיות לטיפול אנושי בטוח ויעיל חושף לעתים ליקויים נסתר��ים. לפענח איך זיהוי פנוטיפי עובד — התהליך הידוע כדה‑קונבולוציית היעד (target deconvolution) — יכול להיות איטי ומלא חוסר ודאות, במיוחד כאשר חומר פועל על מספר מסלולים בבת אחת. מקרי בוחן של תרופות שנכשלו או שוּנוּ שימושם מדגישים כיצד מנגנונים חסרים או מוכרים שלא כהלכה עלולים להוביל לניסויים מבוזבזים או לתופעות לוואי בלתי צפויות.
לאן הגישה הזאת פונה בהמשך
המסקנה היא שעוצמתו האמיתית של גילוי תרופות פנוטיפי תבוא משילוב של מודלים ביולוגיים עשירים עם חישוב מתקדם. תאים גזעיים ממטופלים, איברים‑מיניאטוריים תלת‑ממדיים ודימות מפורט יכולים לספק מערכות בדיקה בעלות דמיון אנושי גבוה יותר, בעוד שבינה גנרטיבית עשויה להציע מולקולות המותאמות לתיקון חתימות מחלה ספציפיות, גם במצבים נדירים עם נתונים מוגבלים. אם ניתנים מענה לאיכות הנתונים, לאימות ולמציאת מנגנונים, אסטרטגיה שמתחילה בחומר ומתחשבת במערכת יכולה להפוך את גילוי התרופות למהיר יותר, יעיל יותר ובהתאמה טובה יותר לאופן שבו מחלות מתנהגות בחולים אמיתיים.
ציטוט: Kumar, S., Pal, A. & Chatterjee, S. Unlocking the potential of computational phenotypic drug discovery: methods, challenges, and future directions. npj Syst Biol Appl 12, 46 (2026). https://doi.org/10.1038/s41540-026-00676-5
מילות מפתח: גילוי תרופות פנוטיפי, למידת מכונה בגילוי תרופות, שימוש מחודש בתרופות, מסך תוכן‑גבוה, פראמקולוגיה חישובית