Clear Sky Science · pt
Desbloqueando o potencial da descoberta fenotípica de medicamentos por computador: métodos, desafios e direções futuras
Por que essa nova forma de encontrar medicamentos importa
A maioria dos novos medicamentos falha em algum ponto entre o laboratório e a clínica, mesmo após anos de trabalho e custos enormes. Este artigo explica uma alternativa em ascensão chamada descoberta fenotípica de medicamentos, que observa como compostos alteram o comportamento de células ou organismos inteiros, em vez de mirar um único alvo pré‑selecionado. Com a ajuda da inteligência artificial e de grandes conjuntos de dados biológicos, essa abordagem pode revelar tratamentos para doenças complexas que resistiram aos métodos tradicionais.
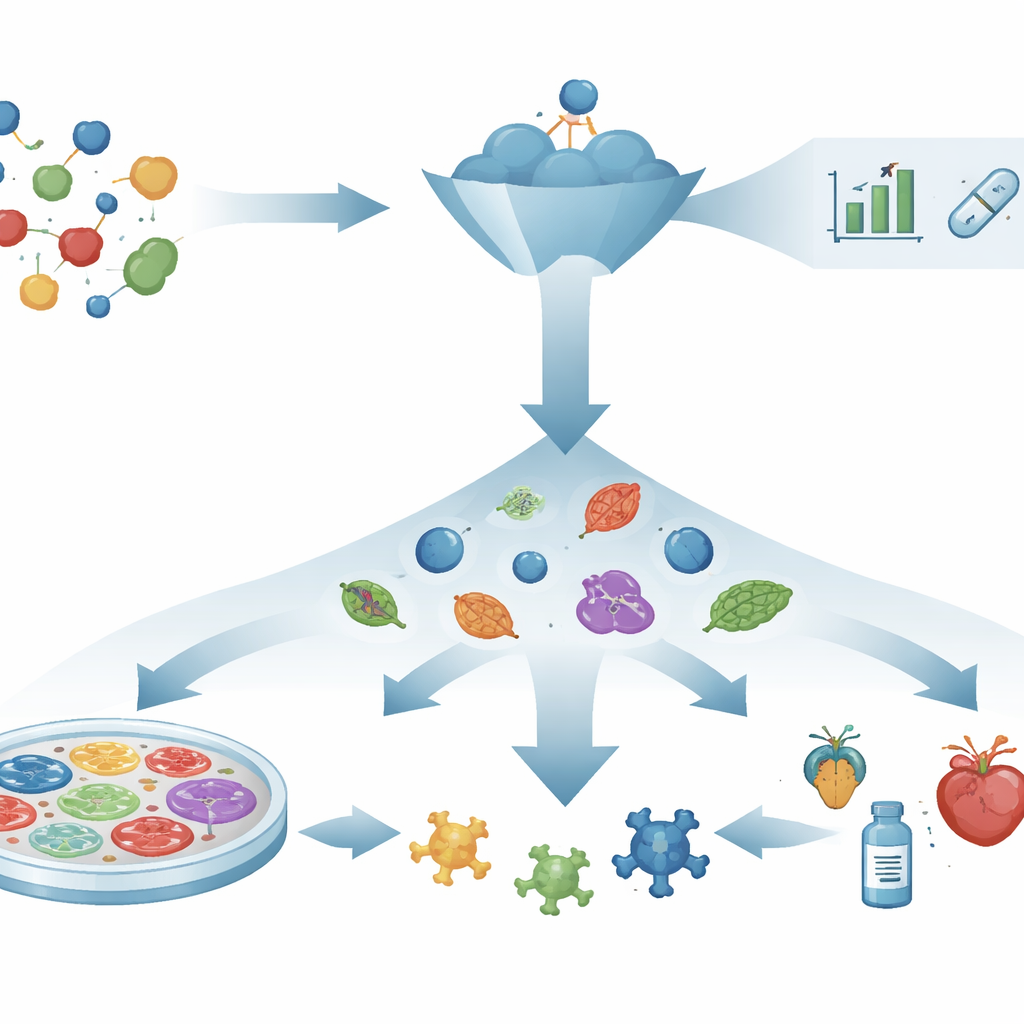
Do pensamento fechadura‑e‑chave para observar sistemas vivos
Durante décadas, a descoberta de fármacos seguiu um roteiro ‘‘mecanismo‑em‑primeiro’': escolher uma proteína única considerada responsável pela doença, projetar ou procurar químicos que se liguem a ela e então esperar que essas interações se traduzam em benefícios reais à saúde. Ferramentas poderosas como previsão de estruturas proteicas, design assistido por computador e triagem virtual aceleraram essa busca. Ainda assim, muitos alvos cuidadosamente escolhidos e moléculas promissoras deixam de ajudar os pacientes, porque alterar uma única molécula nem sempre corrige uma rede de doença emaranhada. Essa lacuna entre o sucesso em tubos de ensaio e o sucesso em pessoas suscitou um renovado interesse em estratégias que se concentram no que realmente acontece em sistemas vivos.
Uma abordagem que começa pelo composto para identificar mudanças úteis
A descoberta fenotípica de medicamentos inverte o roteiro. Em vez de começar com um alvo conhecido, ela faz uma pergunta mais direta: um composto empurra um sistema doente de volta à saúde? Pesquisadores expõem células, tecidos ou pequenos organismos a muitos compostos e procuram mudanças visíveis ou mensuráveis, como restauração da forma celular, sobrevivência de células frágeis ou recuperação de comportamento normal. Só depois que um efeito promissor é observado é que os cientistas investigam como o composto age dentro da célula. Essa abordagem agnóstica ao alvo já levou a medicamentos, como tratamentos para fibrose cística e atrofia muscular espinhal, cujos mecanismos detalhados foram esclarecidos posteriormente. É especialmente útil para doenças impulsionadas por múltiplas vias ao mesmo tempo, em que escolher um único ‘‘alvo mestre’’ é pouco realista.
Transformando leituras biológicas ricas em números
Triagens fenotípicas modernas geram enormes quantidades de dados: imagens de alta resolução de células coradas, leituras de atividade gênica, mapas de alterações proteicas e até comportamento de organismos modelo. Para entender essa complexidade, o campo recorre a ‘‘embeddings’’ — formas de converter química, imagens, expressão gênica e redes de interação em impressões digitais numéricas compactas. Essas impressões capturam padrões de como os fármacos se apresentam, como alteram células e como se conectam a genes e doenças. Modelos de aprendizado de máquina, desde algoritmos clássicos até redes neurais profundas e métodos baseados em grafos, então aprendem a vincular essas impressões a desfechos como toxicidade, benefício provável ou similaridade com fármacos conhecidos. Em alguns casos, podem até sugerir novos compostos ou novos usos para os já existentes.
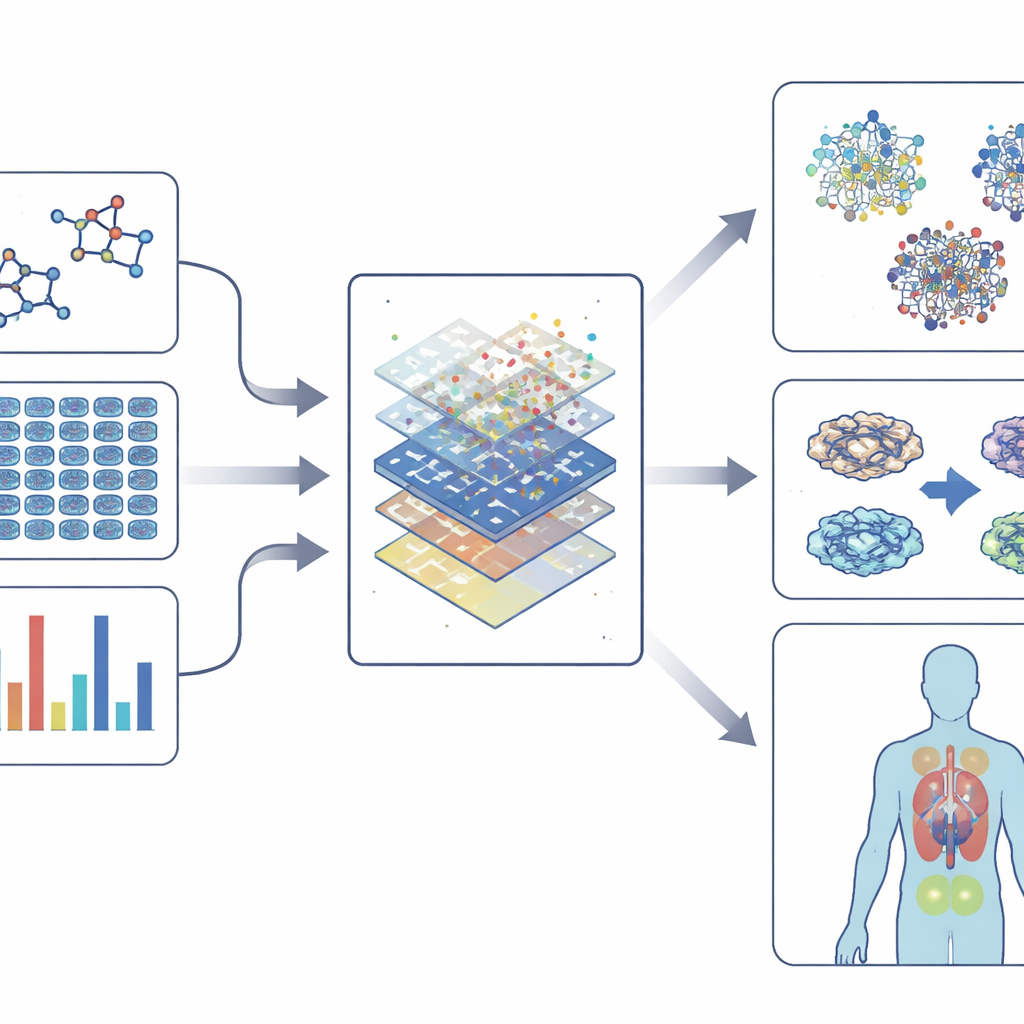
Usando modelos mais inteligentes mantendo‑os compreensíveis
À medida que os modelos se tornam mais poderosos, também correm o risco de ficar mais opacos. Ferramentas de IA explicável visam abrir essa caixa‑preta ao destacar quais características — como mudanças em genes específicos ou partes estruturais de uma molécula — conduzem uma predição. Essa transparência ajuda pesquisadores a confiar nos modelos, projetar compostos mais seguros e entender por que um efeito fenotípico ocorre, não apenas que ele ocorre. Ao mesmo tempo, tecnologias de célula única e multiômicas permitem ver como diferentes tipos celulares em um tecido respondem a um fármaco, aproximando o campo de escolhas de tratamento mais personalizadas.
Obstáculos no caminho para melhores medicamentos
Apesar de sua promessa, a descoberta fenotípica de medicamentos enfrenta desafios importantes. Conjuntos de dados de alta qualidade ainda são esparsos e inconsistentes entre laboratórios, dificultando treinar modelos que generalizem bem. Ensaios fenotípicos complexos podem ser difíceis de reproduzir, e a transição de um hit em células ou animais para uma terapia humana segura e eficaz frequentemente expõe falhas ocultas. Desvendar como um hit fenotípico funciona — o processo conhecido como desconvolução de alvo — pode ser lento e incerto, especialmente quando um composto atua em várias vias ao mesmo tempo. Estudos de caso de medicamentos fracassados ou reposicionados destacam como mecanismos ausentes ou mal compreendidos podem levar a ensaios desperdiçados ou efeitos colaterais inesperados.
Para onde essa abordagem está caminhando
O artigo conclui que o verdadeiro poder da descoberta fenotípica virá da combinação de modelos biológicos ricos com computação avançada. Células‑tronco derivadas de pacientes, mini‑órgãos tridimensionais e imagens detalhadas podem fornecer sistemas de teste mais parecidos com humanos, enquanto a IA generativa pode propor moléculas adaptadas para corrigir assinaturas específicas de doença, mesmo em condições raras com dados limitados. Se questões de qualidade de dados, validação e identificação de mecanismos puderem ser resolvidas, essa estratégia que começa pelo composto e é consciente dos sistemas pode tornar a descoberta de medicamentos mais rápida, mais eficiente e mais alinhada com o comportamento das doenças em pacientes reais.
Citação: Kumar, S., Pal, A. & Chatterjee, S. Unlocking the potential of computational phenotypic drug discovery: methods, challenges, and future directions. npj Syst Biol Appl 12, 46 (2026). https://doi.org/10.1038/s41540-026-00676-5
Palavras-chave: descoberta fenotípica de medicamentos, aprendizado de máquina na descoberta de medicamentos, reposicionamento de medicamentos, triagem de alto conteúdo, farmacologia computacional