Clear Sky Science · de
Das Potenzial der computergestützten phänotypischen Wirkstoffforschung freisetzen: Methoden, Herausforderungen und zukünftige Richtungen
Warum diese neue Art, Medikamente zu finden, wichtig ist
Die meisten neuen Medikamente scheitern irgendwo zwischen Labor und Klinik, selbst nach jahrelanger Arbeit und enormen Kosten. Dieser Artikel erläutert eine aufkommende Alternative namens phänotypische Wirkstoffforschung, die darauf schaut, wie Verbindungen das Verhalten ganzer Zellen oder Organismen verändern, statt ein zuvor ausgewähltes Molekül anzustreben. Mit Hilfe künstlicher Intelligenz und großer biologischer Datensätze könnte dieser Ansatz Behandlungen für komplexe Krankheiten entdecken, die traditionellen Methoden widerstanden haben.
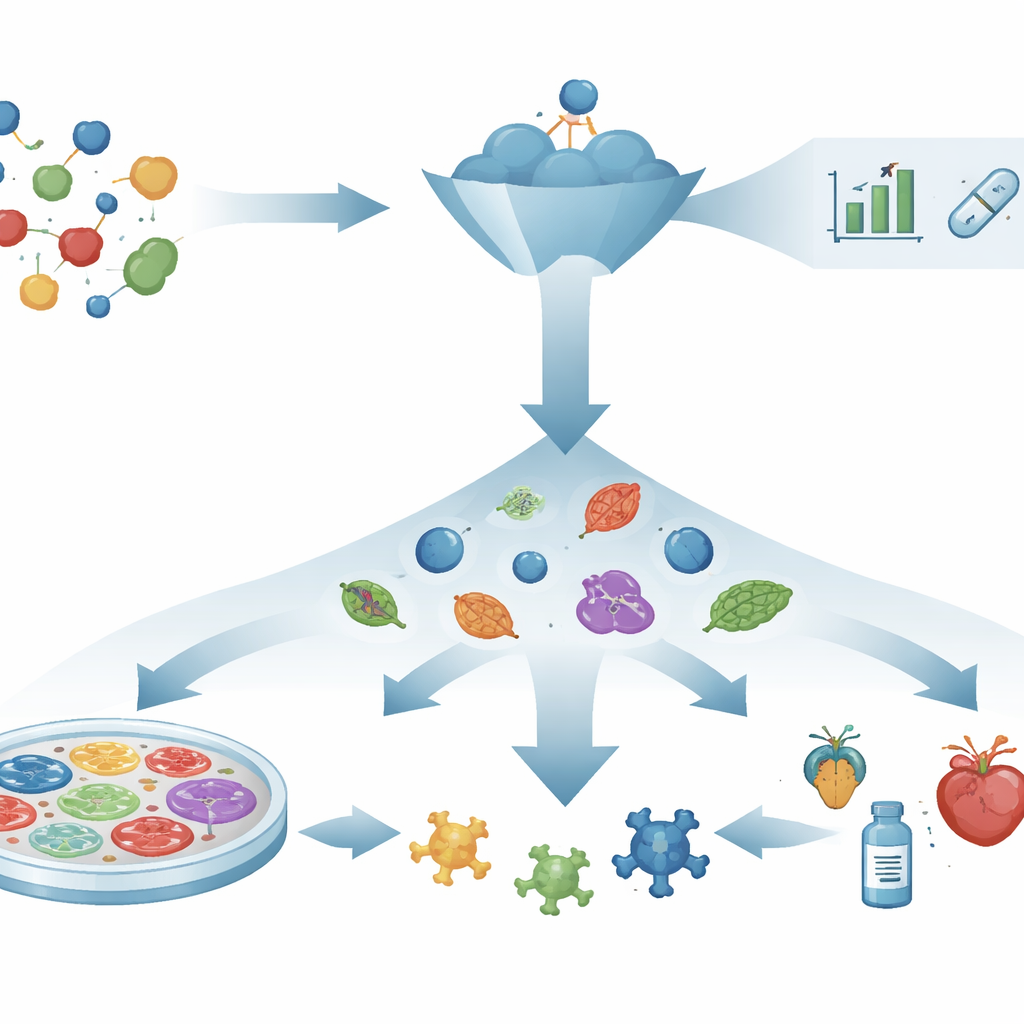
Vom Schloss‑und‑Schlüssel‑Denken zum Beobachten lebender Systeme
Jahrzehntelang folgte die Wirkstoffforschung einem „Mechanismus‑zuerst“-Skript: Man wählt ein einzelnes Protein, von dem man annimmt, dass es die Krankheit antreibt, entwirft oder sucht nach Chemikalien, die daran binden, und hofft dann, dass diese Wechselwirkungen in echte gesundheitliche Vorteile übersetzt werden. Leistungsfähige Werkzeuge wie Vorhersage von Proteinstrukturen, computerunterstützte Gestaltung und virtuelle Screening haben diese Suche beschleunigt. Dennoch helfen viele wohlüberlegte Targets und vielversprechende Moleküle den Patienten nicht, weil die Veränderung eines einzelnen Moleküls nicht notwendigerweise ein vernetztes Krankheitsgeschehen behebt. Diese Lücke zwischen Erfolg im Reagenzglas und Erfolg beim Menschen hat das Interesse an Strategien erneuert, die sich darauf konzentrieren, was tatsächlich in lebenden Systemen geschieht.
Ein verbindungszentrierter Weg, nützliche Veränderungen zu erkennen
Phänotypische Wirkstoffforschung kehrt die Reihenfolge um. Anstatt mit einem bekannten Target zu beginnen, stellt sie eine direktere Frage: Bringt eine Verbindung ein krankes System zurück in Richtung Gesundheit? Forscher setzen Zellen, Gewebe oder kleine Organismen vielen Verbindungen aus und suchen nach sichtbaren oder messbaren Veränderungen, wie der Wiederherstellung der Zellform, dem Überleben empfindlicher Zellen oder der Rückkehr zu normalem Verhalten. Erst nachdem ein vielversprechender Effekt beobachtet wurde, untersuchen Wissenschaftler, wie die Verbindung innerhalb der Zelle wirkt. Dieser target‑agnostische Ansatz hat bereits zu Medikamenten geführt, etwa zu Behandlungen für Mukoviszidose und spinale Muskelatrophie, deren detaillierte Wirkmechanismen später aufgeklärt wurden. Er ist besonders nützlich bei Krankheiten, die von vielen gleichzeitig wirkenden Signalwegen getrieben werden, wo die Wahl eines einzelnen „Master“‑Targets unrealistisch ist.
Reiche biologische Messwerte in Zahlen verwandeln
Moderne phänotypische Screenings erzeugen enorme Datenmengen: hochauflösende Bilder gefärbter Zellen, Messwerte der Genaktivität, Karten von Proteinveränderungen und sogar Verhaltensdaten von Modellorganismen. Um diese Komplexität zu verstehen, stützt sich das Feld auf „Embeddings“ — Methoden, die Chemie, Bilder, Genexpressionsdaten und Interaktionsnetzwerke in kompakte numerische Fingerabdrücke umwandeln. Diese Fingerabdrücke erfassen Muster darin, wie Medikamente wirken, wie sie Zellen verändern und wie sie mit Genen und Krankheiten verknüpft sind. Maschinelle Lernmodelle, von klassischen Algorithmen bis zu tiefen neuronalen Netzen und graphbasierten Methoden, lernen dann, diese Fingerabdrücke mit Ergebnissen wie Toxizität, wahrscheinlichem Nutzen oder Ähnlichkeit zu bekannten Wirkstoffen zu verknüpfen. In manchen Fällen können sie sogar neue Verbindungen oder neue Anwendungen für bestehende Wirkstoffe vorschlagen.
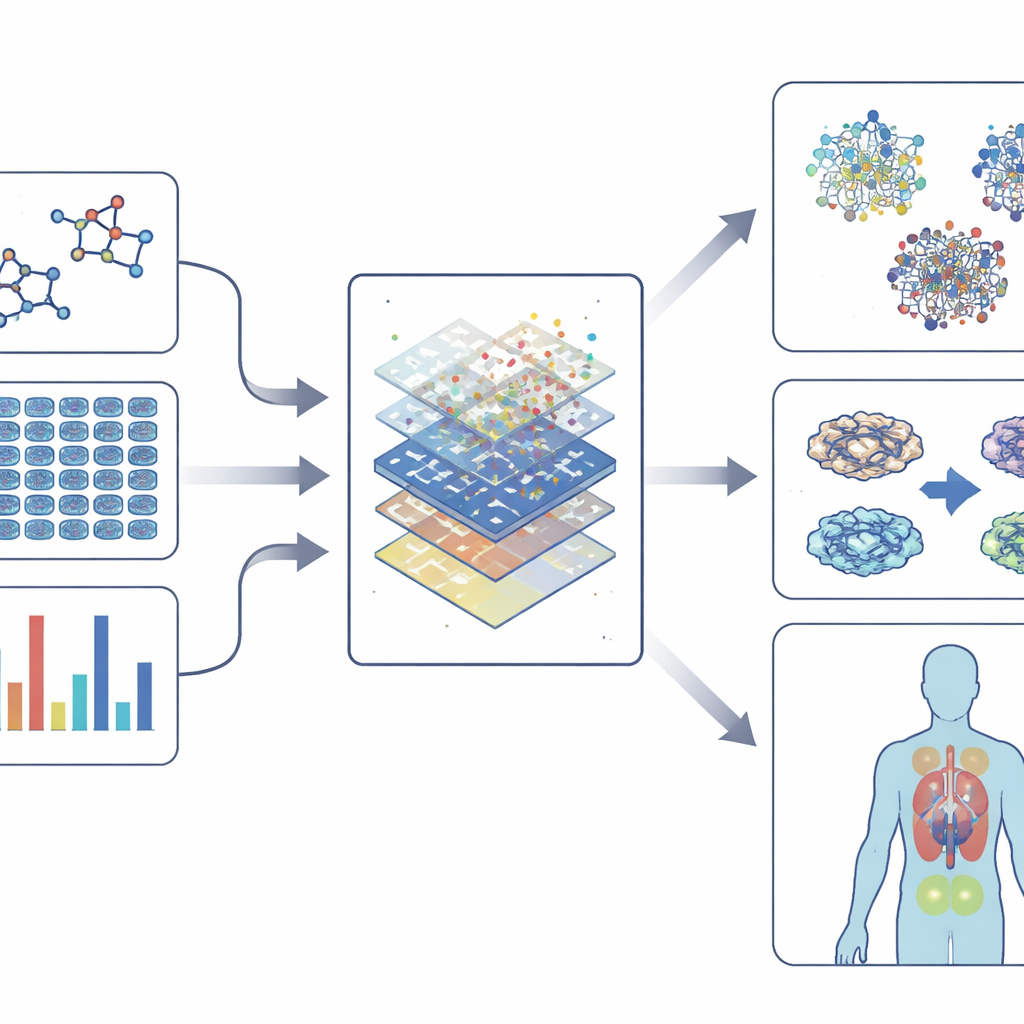
Intelligentere Modelle nutzen und gleichzeitig verständlich halten
Mit zunehmender Leistungsfähigkeit der Modelle wächst auch das Risiko, dass sie undurchsichtig werden. Erklärbare KI‑Werkzeuge zielen darauf ab, diese Blackbox zu öffnen, indem sie hervorheben, welche Merkmale — etwa bestimmte Genveränderungen oder strukturelle Teile eines Moleküls — eine Vorhersage antreiben. Diese Transparenz hilft Forschern, den Modellen zu vertrauen, sicherere Verbindungen zu entwerfen und zu verstehen, warum ein phänotypischer Effekt auftritt, nicht nur dass er auftritt. Gleichzeitig ermöglichen Einzelzell‑ und Multi‑Omics‑Technologien, zu sehen, wie verschiedene Zelltypen in einem Gewebe auf ein Medikament reagieren, und bringen das Feld damit näher an personalisierte Behandlungsentscheidungen.
Hürden auf dem Weg zu besseren Medikamenten
Trotz seines Versprechens steht die phänotypische Wirkstoffforschung vor großen Herausforderungen. Hochwertige Datensätze sind nach wie vor lückenhaft und inkonsistent zwischen Laboren, was es schwierig macht, Modelle zu trainieren, die gut generalisieren. Komplexe phänotypische Assays sind oft schwer reproduzierbar, und der Übergang von einem Treffer in Zellen oder Tieren zu einer sicheren, wirksamen Therapie beim Menschen offenbart häufig versteckte Schwächen. Das Entwirren, wie ein phänotypischer Treffer wirkt — der Prozess der Target‑Dekonvolution — kann langsam und unsicher sein, besonders wenn eine Verbindung auf mehrere Signalwege gleichzeitig wirkt. Fallstudien zu fehlgeschlagenen oder repositionierten Medikamenten zeigen, wie fehlende oder missverstandene Mechanismen zu verschwendeten Studien oder unerwarteten Nebenwirkungen führen können.
Wohin sich dieser Ansatz als Nächstes entwickelt
Der Artikel schließt mit der Einschätzung, dass die eigentliche Stärke der phänotypischen Wirkstoffforschung aus der Kombination reicher biologischer Modelle mit fortschrittlicher Computation entstehen wird. Patientengewonnene Stammzellen, dreidimensionale Mini‑Organe und detaillierte Bildgebung können menschenähnlichere Testsysteme liefern, während generative KI Moleküle vorschlagen könnte, die darauf zugeschnitten sind, spezifische Krankheitsprofile zu korrigieren — sogar bei seltenen Erkrankungen mit begrenzten Daten. Gelängen Verbesserungen bei Datenqualität, Validierung und Mechanismenaufklärung, könnte diese verbindungszentrierte, systembewusste Strategie die Wirkstoffforschung schneller, effizienter und besser an das Krankheitsgeschehen in echten Patienten angepasst machen.
Zitation: Kumar, S., Pal, A. & Chatterjee, S. Unlocking the potential of computational phenotypic drug discovery: methods, challenges, and future directions. npj Syst Biol Appl 12, 46 (2026). https://doi.org/10.1038/s41540-026-00676-5
Schlüsselwörter: phänotypische Wirkstoffforschung, maschinelles Lernen in der Wirkstoffforschung, Wirkstoffrepositionierung, High‑Content‑Screening, computationale Pharmakologie