Clear Sky Science · ar
فتح إمكانات اكتشاف الأدوية الفينوتيبية الحاسوبية: الطرق والتحديات والاتجاهات المستقبلية
لماذا تكتسب هذه الطريقة الجديدة للعثور على الأدوية أهمية
تفشل معظم الأدوية الجديدة في مكان ما بين المختبر والعيادة، حتى بعد سنوات من العمل وتكاليف ضخمة. يشرح هذا المقال نهجًا متصاعدًا يُدعى اكتشاف الأدوية الفينوتيبية، الذي ينظر إلى كيفية تغيير المركبات لسلوك الخلايا أو الكائنات الحية بأكملها بدلاً من استهداف جزيء واحد مُحدد مسبقًا. بمساعدة الذكاء الاصطناعي ومجموعات بيانات بيولوجية كبيرة، قد يكشف هذا النهج عن علاجات لأمراض معقدة قاومت الأساليب التقليدية.
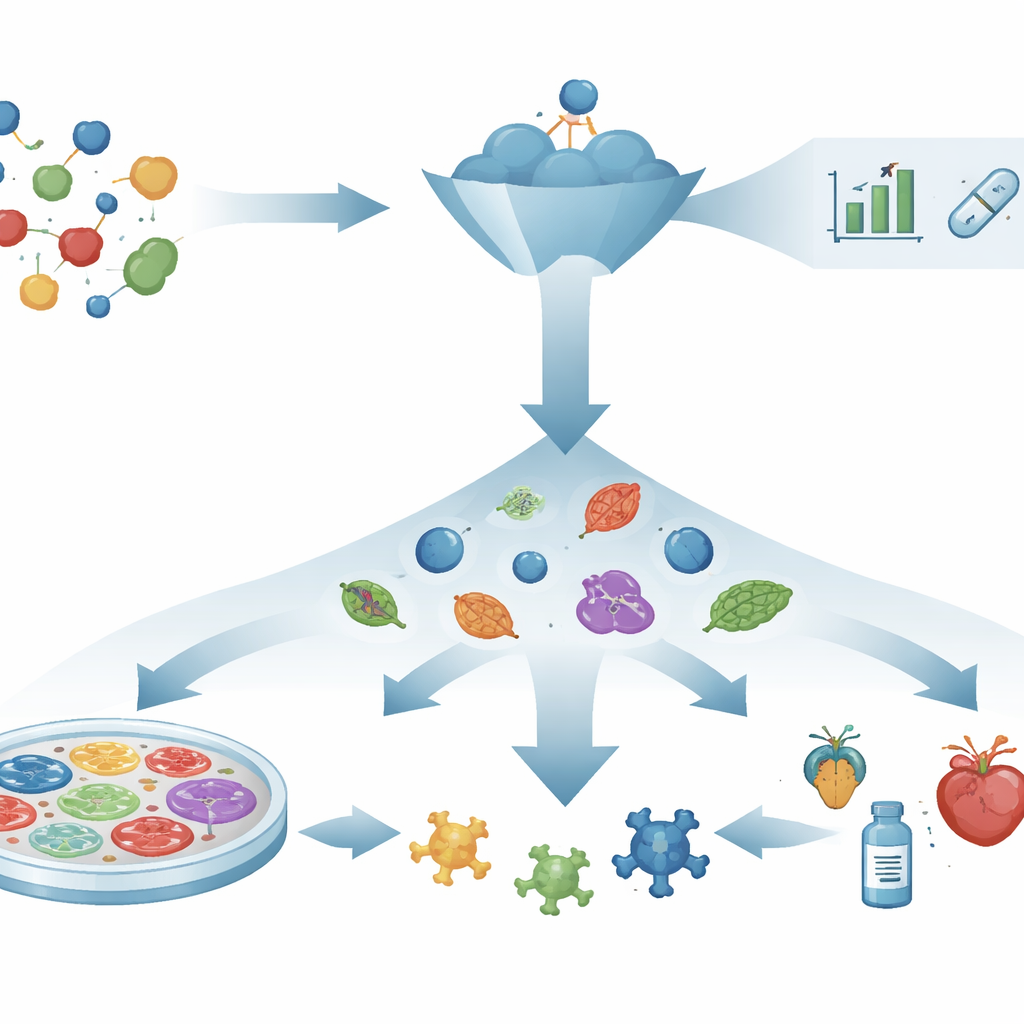
من تفكير القفل والمفتاح إلى مراقبة الأنظمة الحية
لمدة عقود، اتبع اكتشاف الأدوية نصًا «الآلية أولًا»: اختر بروتينًا واحدًا يُعتقد أنه يقود المرض، صمّم أو ابحث عن مركبات ترتبط به، ثم تأمل أن تترجم تلك التفاعلات إلى فوائد صحية حقيقية. أدوات قوية مثل التنبؤ ببنية البروتين، والتصميم المعاون بالحاسوب، والفحص الافتراضي سرّعت هذا البحث. ومع ذلك، تفشل كثير من الأهداف المختارة بعناية والجزيئات الواعدة في مساعدة المرضى، لأن تغيير جزيء واحد لا يصلح دائمًا شبكة المرض المعقدة. هذا الفراغ بين النجاح في أنبوبات الاختبار والنجاح في البشر أثار تجدد الاهتمام باستراتيجيات تركز على ما يحدث فعليًا في الأنظمة الحية.
نهج يبدأ بالمركب لرصد التغييرات المفيدة
يقلب اكتشاف الأدوية الفينوتيبية السيناريو. بدلاً من البدء بهدف معروف، يطرح سؤالًا أكثر مباشرة: هل يدفع مركب ما نظامًا مريضًا نحو الصحة؟ يعرض الباحثون خلايا أو أنسجة أو كائنات صغيرة لعدة مركبات ويبحثون عن تغييرات مرئية أو قابلة للقياس، مثل استعادة شكل الخلية، بقاء خلايا هشة، أو استعادة السلوك الطبيعي. فقط بعد رؤية تأثير واعد يحقق العلماء كيف يعمل المركب داخل الخلية. لقد أدى هذا النهج المستقل عن الهدف بالفعل إلى أدوية مثل علاجات التليف الكيسي والضمور العضلي الشوكي، التي فُهمت آلياتها التفصيلية لاحقًا. وهو مفيد بشكل خاص للأمراض التي تقودها عدة مسارات في الوقت ذاته، حيث يكون اختيار هدف «رئيسي» واحد غير واقعي.
تحويل قراءات بيولوجية غنية إلى أرقام
تولد الفحوصات الفينوتيبية الحديثة كميات هائلة من البيانات: صور عالية الدقة لخلايا مصبوغة، قراءات نشاط الجينات، خرائط تغييرات البروتينات، وحتى سلوك نماذج الكائنات. لفهم هذه التعقيدات، يعتمد المجال على «التضمينات» — طرق لتحويل الكيمياء، الصور، تعبير الجينات، وشبكات التفاعلات إلى بصمات عددية مضغوطة. تلتقط هذه البصمات أنماط كيفية ظهور الأدوية، وكيف تغير الخلايا، وكيف ترتبط بالجينات والأمراض. تتعلم نماذج التعلم الآلي، من الخوارزميات الكلاسيكية إلى الشبكات العصبية العميقة والأساليب القائمة على الرسوم البيانية، ربط هذه البصمات بنتائج مثل السمية، الفائدة المحتملة، أو الشبه بالأدوية المعروفة. وفي بعض الحالات، يمكنها حتى اقتراح مركبات جديدة أو استخدامات جديدة للمركبات القائمة.
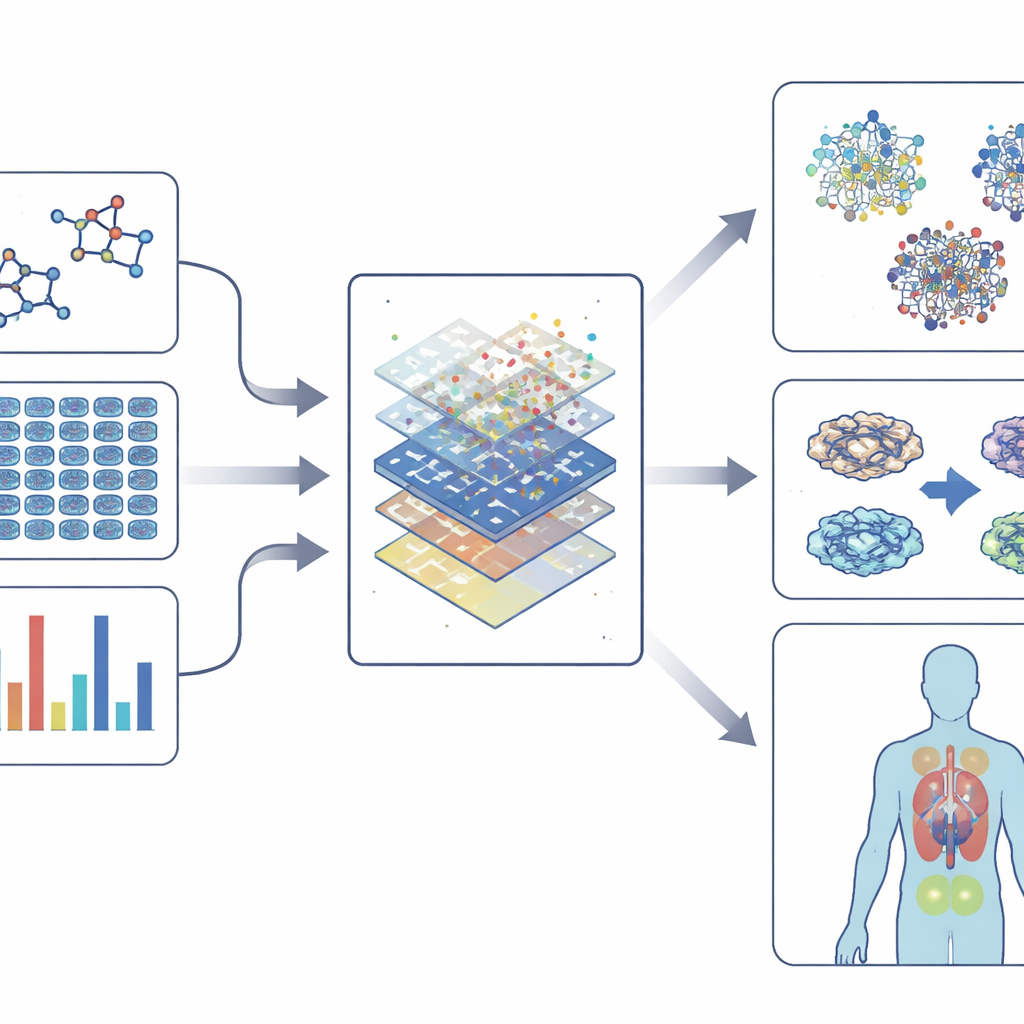
استخدام نماذج أذكى مع الحفاظ على قابليتها للفهم
مع تزايد قوة النماذج، يتزايد معها خطر غموضها. تهدف أدوات الذكاء الاصطناعي القابلة للتفسير إلى فتح هذا الصندوق الأسود من خلال إبراز الميزات — مثل تغييرات جينية معينة أو أجزاء تركيبية في جزيء — التي تقود التنبؤ. تساعد هذه الشفافية الباحثين على الوثوق بالنماذج، تصميم مركبات أكثر أمانًا، وفهم سبب حدوث تأثير فينوتيبي وليس مجرد حدوثه. في الوقت نفسه، تتيح تقنيات الخلية الواحدة وتعدد الأومية للعلماء رؤية كيفية استجابة أنواع الخلايا المختلفة في نسيج لدواء ما، مما يقرب المجال من خيارات علاجية مخصصة.
العقبات في طريق الحصول على أدوية أفضل
رغم وعودها، يواجه اكتشاف الأدوية الفينوتيبية تحديات كبيرة. لا تزال مجموعات البيانات عالية الجودة متقطعة وغير متسقة بين المختبرات، مما يصعّب تدريب نماذج تعمم جيدًا. قد تكون المقاييس الفينوتيبية المعقدة صعبة التكرار، والانتقال من ضربة فعالة في خلايا أو حيوانات إلى علاج بشري آمن وفعال غالبًا ما يكشف عن عيوب مخفية. فك شيفرة كيفية عمل ضربة فينوتيبية — العملية المعروفة بفك إلغاء الهدف — قد يكون بطيئًا وغير مؤكد، خاصة عندما يؤثر المركب على عدة مسارات في آنٍ واحد. تسلط دراسات حالات الأدوية الفاشلة أو المعاد توظيفها الضوء على كيفية أن الآليات المفقودة أو غير المفهومة يمكن أن تؤدي إلى تجارب سريرية مهدورة أو آثار جانبية غير متوقعة.
إلى أين يتجه هذا النهج بعد ذلك
يخلص المقال إلى أن القوة الحقيقية لاكتشاف الأدوية الفينوتيبية ستأتي من الجمع بين نماذج بيولوجية غنية وحوسبة متقدمة. يمكن للخلايا الجذعية المأخوذة من المرضى، والأعضاء المصغرة ثلاثية الأبعاد، والتصوير التفصيلي أن توفر أنظمة اختبار أكثر شبهاً بالبشر، بينما قد يقترح الذكاء الاصطناعي التوليدي جزيئات مصممة لتصحيح تواقيع مرضية محددة، حتى في الحالات النادرة ذات البيانات المحدودة. إذا أمكن معالجة قضايا جودة البيانات، والتحقق، واكتشاف الآليات، فقد يجعل هذا النهج القائم على المركبات والواعٍ بالنظام اكتشاف الأدوية أسرع وأكثر كفاءة وأكثر انسجامًا مع كيفية تصرف الأمراض في المرضى الحقيقيين.
الاستشهاد: Kumar, S., Pal, A. & Chatterjee, S. Unlocking the potential of computational phenotypic drug discovery: methods, challenges, and future directions. npj Syst Biol Appl 12, 46 (2026). https://doi.org/10.1038/s41540-026-00676-5
الكلمات المفتاحية: اكتشاف الأدوية الفينوتيبية, التعلم الآلي في اكتشاف الأدوية, إعادة توظيف الأدوية, الفحص عالي المحتوى, الصيدلة الحاسوبية