Clear Sky Science · ru
Раскрытие потенциала вычислительной фенотипической разработки лекарств: методы, проблемы и перспективы
Почему этот новый подход к поиску лекарств важен
Большинство новых лекарств терпят неудачу на пути от лаборатории к клинике, даже после многих лет работы и огромных затрат. В этой статье объясняется растущая альтернатива — фенотипическая разработка лекарств, которая изучает, как соединения меняют поведение целых клеток или организмов, вместо того чтобы нацеливаться на заранее выбранную молекулу. С помощью искусственного интеллекта и больших биологических наборов данных этот подход может выявить лечения для сложных заболеваний, которые сопротивлялись традиционным методам.
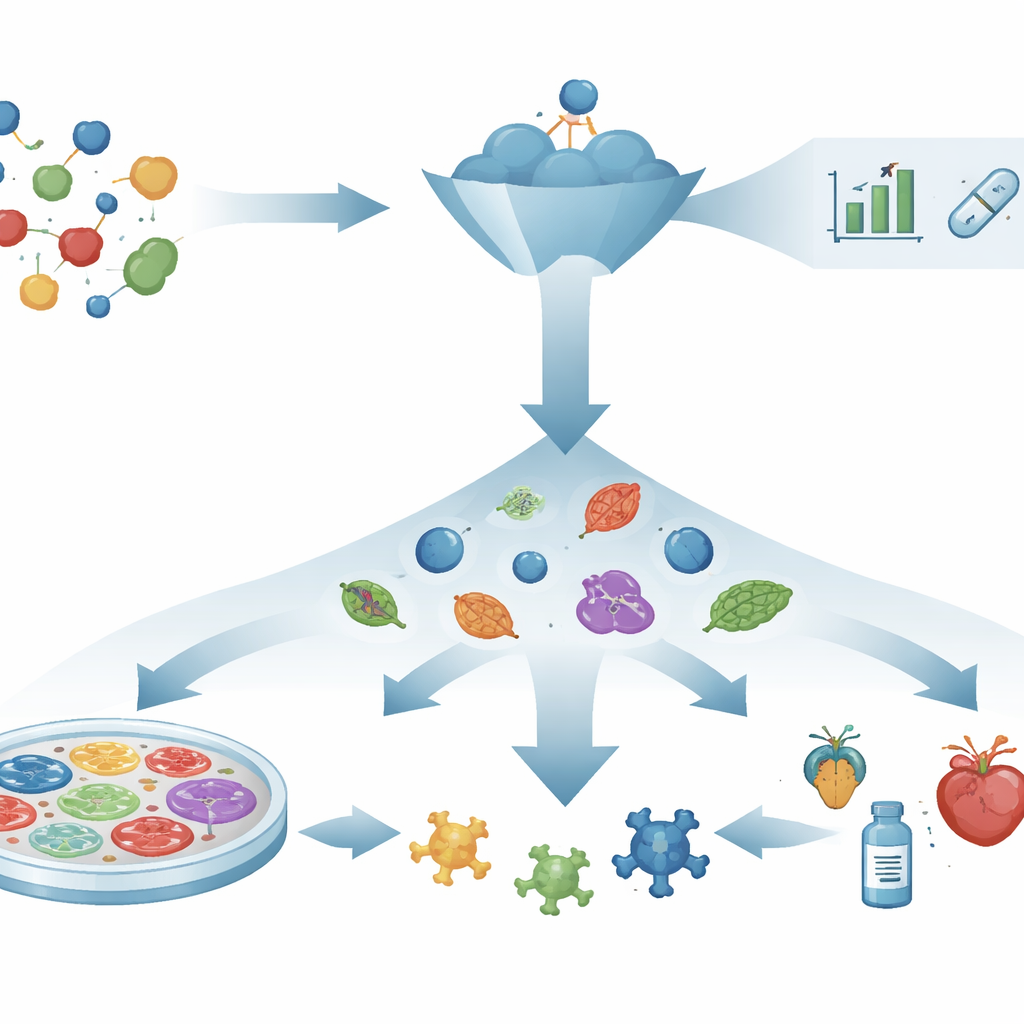
От мышления «замок‑и‑ключ» к наблюдению за живыми системами
Десятилетиями разработка лекарств следовала «сценарию сначала механизм»: выбирали один белок, считающийся причиной болезни, разрабатывали или искали молекулы, связывающиеся с ним, и надеялись, что эти взаимодействия принесут реальную пользу людям. Мощные инструменты, такие как предсказание структуры белков, компьютерное проектирование и виртуальный скрининг, ускорили этот поиск. Тем не менее многие тщательно выбранные мишени и многообещающие молекулы по‑прежнему не помогают пациентам, потому что изменение одной молекулы не всегда исправляет запутанную сеть заболеваний. Этот разрыв между успехами в пробирке и успехами у людей вызвал возобновлённый интерес к стратегиям, сосредоточенным на том, что действительно происходит в живых системах.
Подход «сначала соединение», чтобы заметить полезные изменения
Фенотипическая разработка лекарств переворачивает сценарий. Вместо того чтобы начинать с известной мишени, она задаёт более прямой вопрос: возвращает ли соединение больную систему к здоровому состоянию? Исследователи воздействуют на клетки, ткани или небольшие организмы множеством соединений и отслеживают видимые или измеримые изменения, такие как восстановление формы клетки, выживание уязвимых клеток или восстановление нормального поведения. Только после того, как обнаружен многообещающий эффект, учёные выясняют, как соединение действует внутри клетки. Этот подход, не зависящий от заранее выбранной мишени, уже привёл к лекарствам, например для муковисцидоза и спинальной мышечной атрофии, механизмы которых были подробно изучены позднее. Он особенно полезен при заболеваниях, вызванных множеством путей одновременно, когда выбор одной «главной» мишени нереалистичен.
Преобразование богатых биологических данных в числа
Современные фенотипические скрининги генерируют огромные объёмы данных: высокоразрешающие изображения окрашенных клеток, показатели активности генов, карты изменений белков и даже поведение модельных организмов. Чтобы разобраться в этой сложности, область опирается на «встраивания» (embeddings) — способы преобразования химии, изображений, экспрессии генов и сетей взаимодействий в компактные числовые отпечатки. Эти отпечатки фиксируют закономерности в том, как выглядят лекарства, как они изменяют клетки и как они связаны с генами и заболеваниями. Модели машинного обучения — от классических алгоритмов до глубоких нейронных сетей и методов на графах — затем учатся связывать эти отпечатки с результатами, такими как токсичность, ожидаемая польза или сходство с известными препаратами. В некоторых случаях они даже могут предложить новые соединения или новые применения для существующих препаратов.
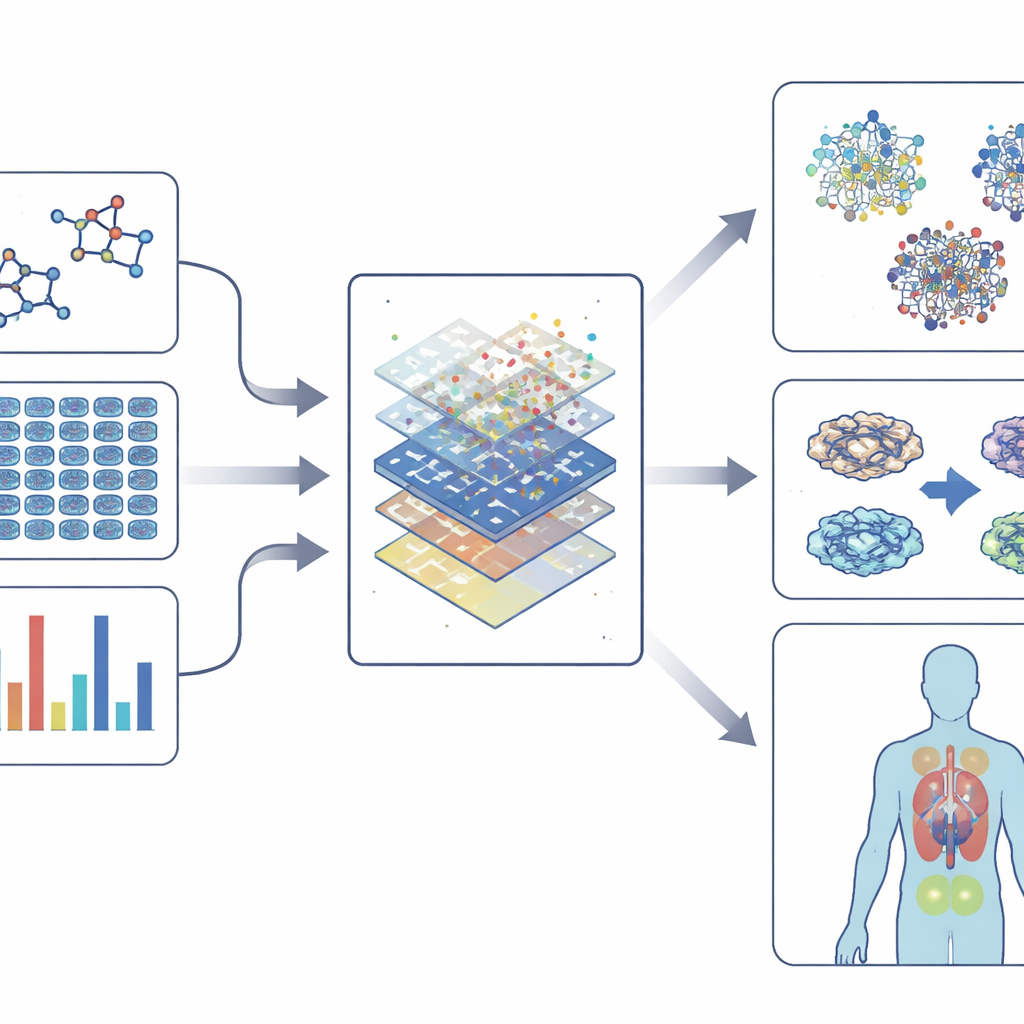
Использование более умных моделей при сохранении их понятности
По мере того как модели становятся мощнее, они также рискуют становиться более непрозрачными. Инструменты объяснимого ИИ стремятся открыть эту «чёрную коробку», выделяя те признаки — например отдельные изменения генов или структурные фрагменты молекулы — которые определяют предсказание. Такая прозрачность помогает исследователям доверять моделям, разрабатывать более безопасные соединения и понимать, почему возникает фенотипический эффект, а не только факт его наличия. Одновременно технологии одиночных клеток и мультиомные подходы позволяют учёным видеть, как разные типы клеток в ткани реагируют на препарат, приближая область к персонализированному выбору терапии.
Препятствия на пути к лучшим лекарствам
Несмотря на потенциал, фенотипическая разработка лекарств сталкивается с серьёзными трудностями. Наборы данных высокого качества по‑прежнему фрагментарны и непоследовательны между лабораториями, что затрудняет обучение моделей, которые хорошо обобщают. Сложные фенотипические тесты могут быть трудновоспроизводимы, а переход от «хита» в клетках или животных к безопасной и эффективной терапии у людей часто выявляет скрытые недостатки. Распутывание механизма действия фенотипического хита — процесс, известный как деконволюция мишеней — может быть медленным и неопределённым, особенно когда соединение действует через несколько путей одновременно. Разбор конкретных случаев неудавшихся или репозиционированных препаратов подчёркивает, как отсутствующие или неправильно понятые механизмы могут привести к напрасной трате ресурсов или неожиданным побочным эффектам.
Куда движется этот подход дальше
В статье делается вывод, что настоящая сила фенотипической разработки лекарств возникнет из сочетания богатых биологических моделей с продвинутыми вычислениями. Клетки, полученные от пациентов, трёхмерные мини‑органы и детальная визуализация могут предоставить более приближённые к человеку тестовые системы, в то время как генеративный ИИ может предлагать молекулы, нацеленные на исправление специфических сигнатур заболевания, даже для редких состояний с ограниченными данными. Если удастся решить проблемы качества данных, валидации и поиска механизмов, этот подход «сначала соединение», учитывающий систему в целом, может сделать разработку лекарств быстрее, эффективнее и более согласованной с тем, как заболевания проявляются у реальных пациентов.
Цитирование: Kumar, S., Pal, A. & Chatterjee, S. Unlocking the potential of computational phenotypic drug discovery: methods, challenges, and future directions. npj Syst Biol Appl 12, 46 (2026). https://doi.org/10.1038/s41540-026-00676-5
Ключевые слова: фенотипическая разработка лекарств, машинное обучение в разработке лекарств, репозиционирование лекарств, скрининг с высоким информационным содержанием, вычислительная фармакология