Clear Sky Science · ja
計算的フェノタイプ薬物探索の可能性を解き放つ:方法、課題、今後の方向性
なぜこの新しい創薬法が重要なのか
多くの新薬は、長年の研究と巨額の費用を経ても、実験室から臨床へ進む過程で失敗します。本稿は「フェノタイプ薬物探索」と呼ばれる台頭する代替手法を解説します。これは特定の分子を狙うのではなく、化合物が細胞や生体の全体的な振る舞いをどのように変えるかに着目します。人工知能と大規模な生物学的データセットを活用することで、従来の手法では見出せなかった複雑な疾患への治療法を明らかにする可能性があります。
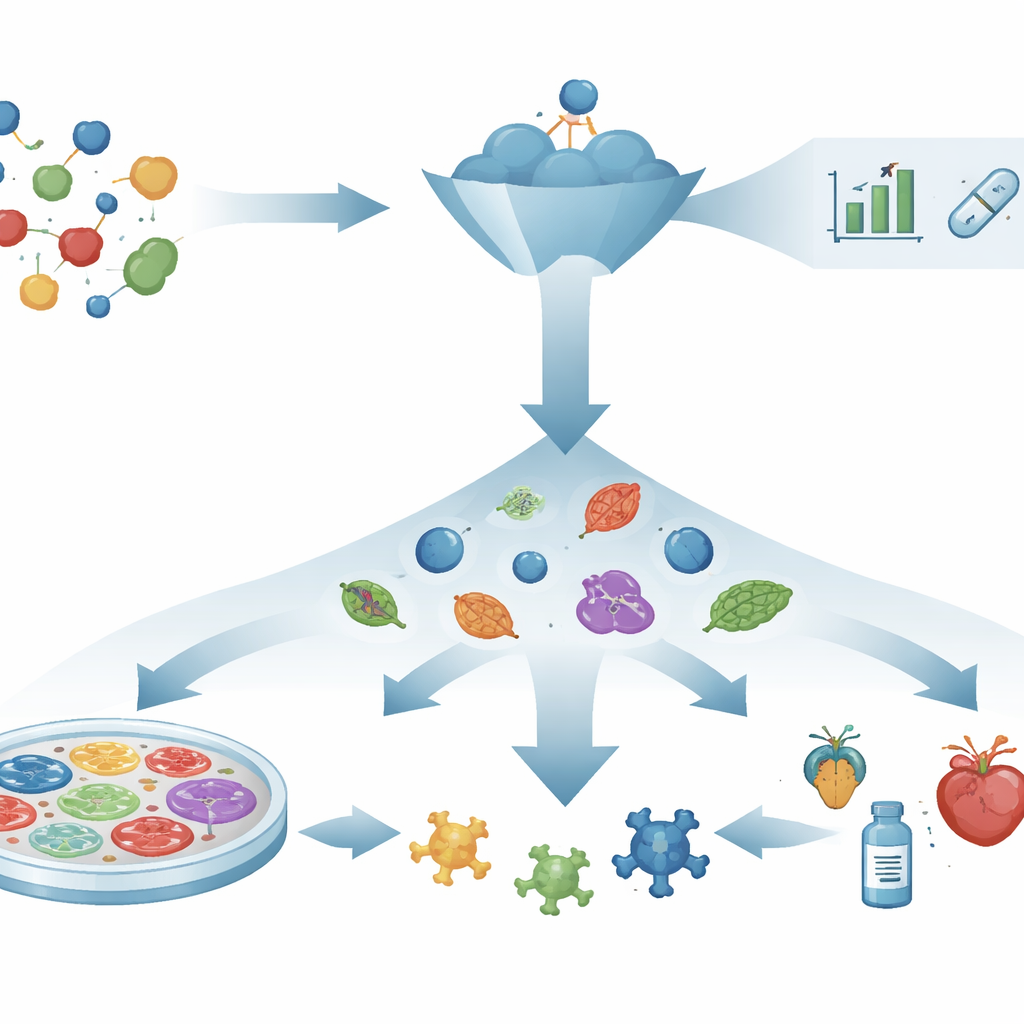
鍵と鍵穴の発想から生きた系の観察へ
何十年にもわたり、創薬は「機構優先」の筋書きに従ってきました。病気を引き起こすと考えられる単一のタンパク質を選び、それに結合する化合物を設計または探索し、その相互作用が実際の治療効果につながることを期待する、という流れです。タンパク質構造予測、コンピュータ支援設計、仮想スクリーニングといった強力なツールがこの探索を加速しました。それでも、慎重に選ばれた標的や有望な分子が患者に効かないことが多いのは、単一の分子を変えても複雑に絡み合った疾患ネットワークが修復されるとは限らないためです。試験管内での成功と人での成功の間にあるこのギャップが、生体で実際に何が起きるかに着目する戦略への関心を再燃させています。
有用な変化を見つける化合物優先の方法
フェノタイプ薬物探索は発想を逆転させます。既知の標的から始める代わりに、より直接的な問いを投げかけます:化合物は病的な系を健康に近づけるか?研究者は細胞、組織、あるいは小型モデル生物に多数の化合物を露呈させ、形態の回復、脆弱な細胞の生存、正常な行動の回復といった可視化・測定可能な変化を探します。有望な効果が観察された後で初めて、科学者はその化合物が細胞内でどのように働くかを調べます。この標的非依存的アプローチは、嚢胞性線維症や脊髄性筋萎縮症の治療薬のように、後に詳細な作用機序が解明された薬を生み出してきました。複数の経路が同時に関与する疾患では、単一の「支配的」標的を選ぶことが現実的でないため、特に有用です。
豊富な生物学的リードアウトを数値に変える
現代のフェノタイプスクリーニングは膨大なデータを生み出します:染色された細胞の高解像度画像、遺伝子発現のリードアウト、タンパク質変化のマップ、さらにはモデル生物の挙動まで。これらの複雑さを理解するために、この分野は「埋め込み(エンベディング)」に依存しています。化学情報、画像、遺伝子発現、相互作用ネットワークをコンパクトな数値的フィンガープリントに変換する手法です。これらのフィンガープリントは、薬物の見た目、細胞に与える変化、遺伝子や疾患とのつながりに関するパターンを捉えます。古典的なアルゴリズムから深層ニューラルネットワークやグラフベースの手法までの機械学習モデルが、これらのフィンガープリントと毒性、想定される有益性、既知薬との類似性といったアウトカムを結びつけることを学びます。場合によっては、新しい化合物や既存薬の新用途を提案することさえあります。
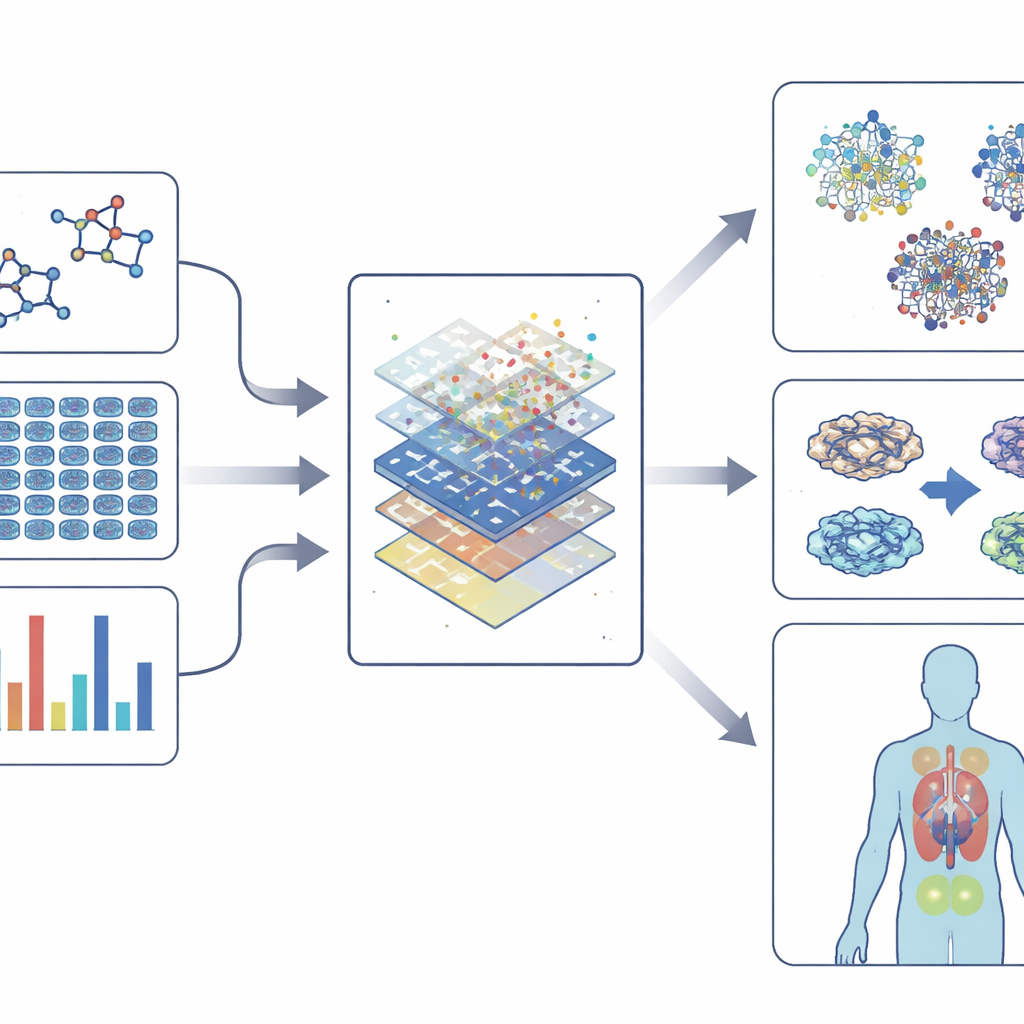
より賢いモデルを使いつつ可解性を保つ
モデルが強力になるにつれて、不透明さが増すリスクも生じます。説明可能なAIツールは、どの特徴—特定の遺伝子変化や分子の構造部分など—が予測を駆動しているかを強調することでこのブラックボックスを開こうとします。この透明性は研究者がモデルを信頼し、安全な化合物を設計し、フェノタイプ効果がなぜ生じるのかを理解するのに役立ちます。同時に、単一細胞解析やマルチオミクス技術は、組織内の異なる細胞型が薬にどう応答するかを可視化し、個別化された治療選択に近づけます。
より良い薬へ向かう道の障壁
有望性にもかかわらず、フェノタイプ薬物探索は重大な課題に直面しています。高品質なデータセットは依然として断片的でラボ間で一貫性が乏しく、汎化性の高いモデルを訓練することが難しいです。複雑なフェノタイプアッセイは再現が困難であり、細胞や動物でのヒットから安全で有効なヒト治療へ移行する過程で隠れた欠陥が露呈することが多いです。フェノタイプヒットの作用機序を解きほぐす、いわゆる標的解剖(ターゲットデコンボリューション)は、特に化合物が複数の経路に作用する場合、遅く不確実になりがちです。失敗例やリポジショニングされた薬の事例は、機序の欠落や誤解が試験の浪費や予期せぬ副作用につながり得ることを示しています。
このアプローチの今後の向かう先
記事は、フェノタイプ薬物探索の真の力は豊富な生物学的モデルと高度な計算を結びつけることにあると結論付けます。患者由来の幹細胞、三次元ミニ臓器、詳細なイメージングはよりヒトに近い試験系を提供し、生成系AIは限られたデータしかない希少疾患においても特定の疾患シグネチャを是正する分子を提案するかもしれません。データ品質、検証、機序解明の問題に対処できれば、この化合物優先でシステムを意識した戦略は、創薬をより迅速に、より効率的に、そして疾患が実際の患者内で振る舞う様子により密接に一致させる可能性があります。
引用: Kumar, S., Pal, A. & Chatterjee, S. Unlocking the potential of computational phenotypic drug discovery: methods, challenges, and future directions. npj Syst Biol Appl 12, 46 (2026). https://doi.org/10.1038/s41540-026-00676-5
キーワード: フェノタイプ薬物探索, 創薬における機械学習, 薬のリポジショニング, ハイコンテントスクリーニング, 計算薬理学