Clear Sky Science · sv
Låsa upp potentialen i beräkningsbaserad fenotypisk läkemedelsupptäckt: metoder, utmaningar och framtida riktningar
Varför detta nya sätt att hitta läkemedel spelar roll
De flesta nya läkemedel misslyckas någonstans mellan labbet och kliniken, trots år av arbete och stora kostnader. Denna artikel förklarar ett växande alternativ kallat fenotypisk läkemedelsupptäckt, som studerar hur föreningar förändrar beteendet hos hela celler eller organismer istället för att rikta in sig på en förutvald molekyl. Med hjälp av artificiell intelligens och stora biologiska dataset kan detta tillvägagångssätt avslöja behandlingar för komplexa sjukdomar som stått emot traditionella metoder.
Från lås‑och‑nyckel‑tänkande till att observera levande system
I årtionden har läkemedelsupptäckt följt ett "mekanism‑först"‑schema: välj ett enskilt protein som antas driva sjukdomen, designa eller sök efter kemikalier som binder till det, och hoppas sedan att dessa interaktioner leder till verkliga hälsofördelar. Kraftfulla verktyg som proteinstrukturförutsägelse, datorstödd design och virtuell screening har påskyndat denna sökning. Ändå misslyckas många noggrant utvalda mål och lovande molekyler fortfarande med att hjälpa patienter, eftersom förändring av en molekyl inte alltid rättar till ett invecklat sjukdomsnätverk. Detta gap mellan framgång i provrör och framgång hos människor har återväckt intresset för strategier som fokuserar på vad som faktiskt händer i levande system.
En förenings‑först‑metod för att upptäcka hjälpsamma förändringar
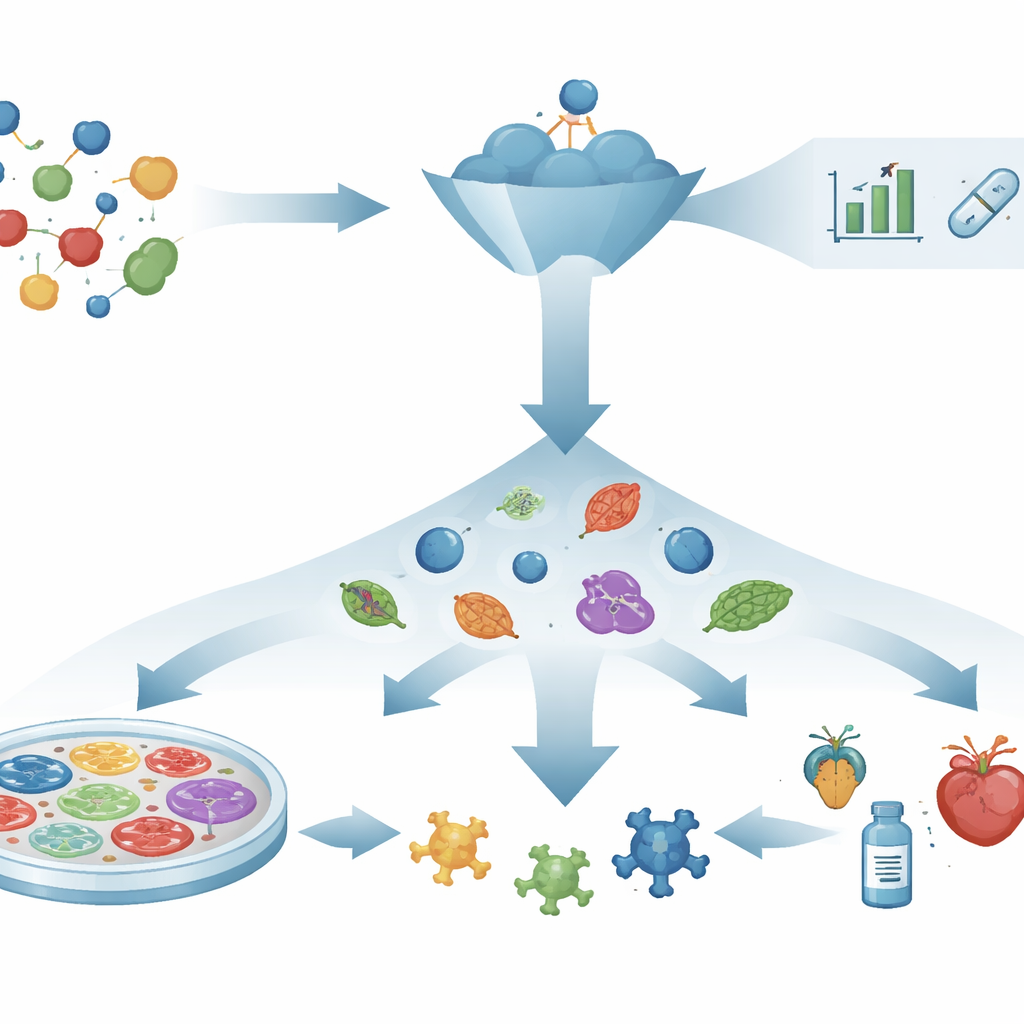
Fenotypisk läkemedelsupptäckt vänder på berättelsen. Istället för att börja med ett känt mål ställer den en mer direkt fråga: driver en förening ett sjukt system tillbaka mot hälsa? Forskare exponerar celler, vävnader eller små organismer för många föreningar och letar efter synliga eller mätbara förändringar, såsom återställd cellform, överlevnad hos sköra celler eller återkomst av normalt beteende. Först efter att en lovande effekt observerats undersöker forskarna hur föreningen verkar inne i cellen. Detta mål‑agnostiska tillvägagångssätt har redan lett till läkemedel, exempelvis behandlingar för cystisk fibros och spinal muskelatrofi, vars detaljerade mekanismer fastställdes i efterhand. Det är särskilt användbart för sjukdomar som drivs av många vägar samtidigt, där det är orealistiskt att välja ett enskilt "huvud"‑mål.
Omvandla rika biologiska avläsningar till siffror
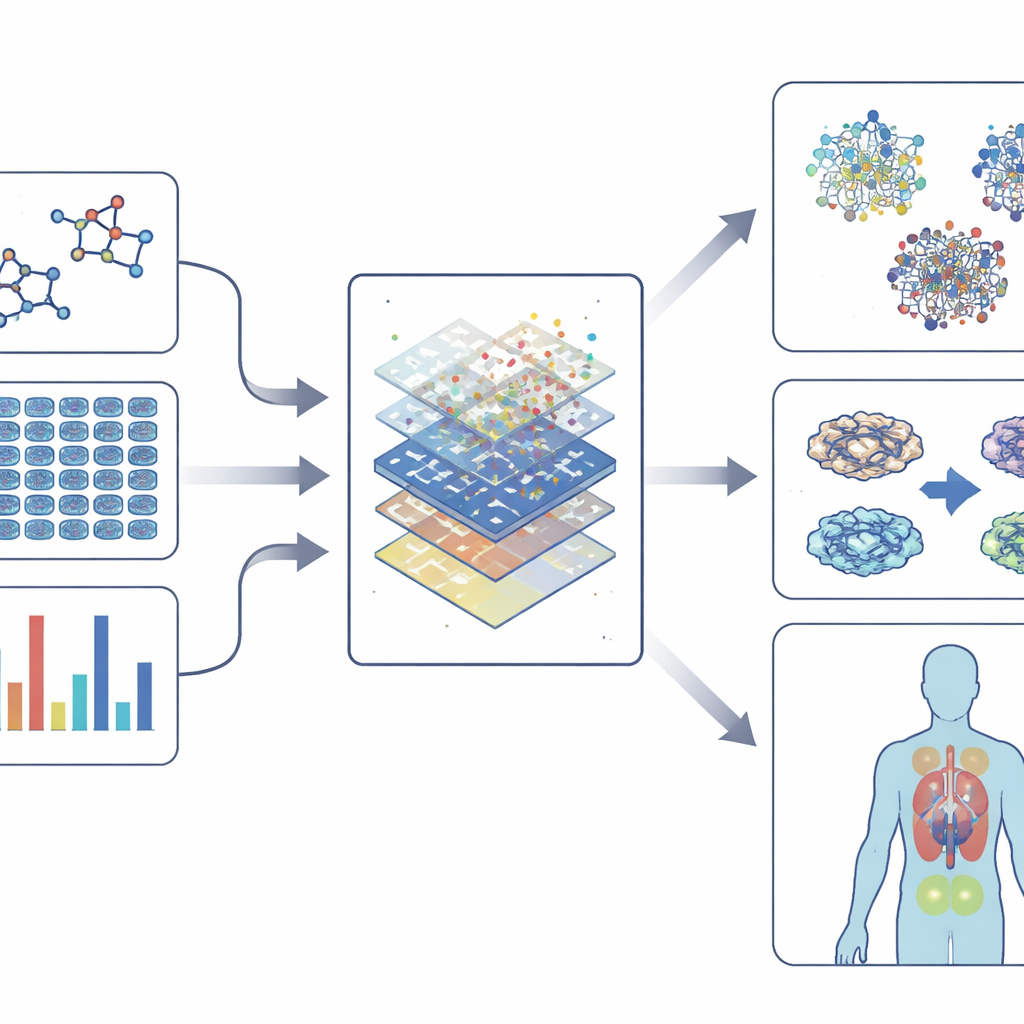
Moderna fenotypiska screeningar genererar enorma datamängder: högupplösta bilder av färgade celler, avläsningar av genaktivitet, kartor över proteinförändringar och till och med beteende hos modellorganismer. För att förstå denna komplexitet förlitar sig fältet på "embeddings"—sätt att omvandla kemi, bilder, genuttryck och interaktionsnätverk till kompakta numeriska fingeravtryck. Dessa fingeravtryck fångar mönster i hur läkemedel ser ut, hur de ändrar celler och hur de kopplar till gener och sjukdomar. Maskininlärningsmodeller, från klassiska algoritmer till djupa neurala nätverk och grafbaserade metoder, lär sig sedan att koppla dessa fingeravtryck till utfall såsom toxicitet, sannolik nytta eller likhet med kända läkemedel. I vissa fall kan de till och med föreslå nya föreningar eller nya användningsområden för befintliga läkemedel.
Använda smartare modeller samtidigt som de förblir begripliga
När modeller blir kraftfullare riskerar de också att bli mer ogenomskinliga. Förklarlig AI (Explainable AI) syftar till att öppna denna svarta låda genom att framhäva vilka egenskaper—såsom särskilda genförändringar eller strukturella delar av en molekyl—som driver en prediktion. Denna transparens hjälper forskare att lita på modellerna, designa säkrare föreningar och förstå varför en fenotypisk effekt uppstår, inte bara att den uppstår. Samtidigt gör singelcells‑ och multi‑omics‑teknologier det möjligt för forskare att se hur olika celltyper i en vävnad reagerar på ett läkemedel, vilket för fältet närmare personligt anpassade behandlingsval.
Hinder på vägen mot bättre läkemedel
Trots sitt löfte står fenotypisk läkemedelsupptäckt inför stora utmaningar. Dataset av hög kvalitet är fortfarande ojämnt spridda och inkonsekventa mellan laboratorier, vilket försvårar träning av modeller som generaliserar väl. Komplexa fenotypiska assay kan vara svåra att reproducera, och övergången från en träff i celler eller djur till en säker, effektiv behandling för människor avslöjar ofta dolda brister. Att reda ut hur en fenotypisk träff fungerar—processen känd som mål‑dekonvolution—kan vara långsam och osäker, särskilt när en förening verkar på flera vägar samtidigt. Fallstudier av misslyckade eller omdisponerade läkemedel understryker hur saknade eller missförstådda mekanismer kan leda till bortkastade prövningar eller oväntade biverkningar.
Vart detta tillvägagångssätt är på väg härnäst
Artikeln avslutar med slutsatsen att den verkliga kraften i fenotypisk läkemedelsupptäckt kommer från att kombinera rika biologiska modeller med avancerad beräkning. Patient‑härledda stamceller, tredimensionella mini‑organ och detaljerad bilddiagnostik kan ge mer människoliknande testsystem, medan generativ AI kan föreslå molekyler skräddarsydda för att korrigera specifika sjukdomssignaturer, även vid sällsynta tillstånd med begränsade data. Om frågor kring datakvalitet, validering och mekanismupptäckt kan lösas, kan denna förenings‑först, systemmedvetna strategi göra läkemedelsupptäckt snabbare, mer effektiv och bättre anpassad till hur sjukdomar beter sig hos verkliga patienter.
Citering: Kumar, S., Pal, A. & Chatterjee, S. Unlocking the potential of computational phenotypic drug discovery: methods, challenges, and future directions. npj Syst Biol Appl 12, 46 (2026). https://doi.org/10.1038/s41540-026-00676-5
Nyckelord: fenotypisk läkemedelsupptäckt, maskininlärning i läkemedelsupptäckt, omdisponering av läkemedel, höginnehålls‑screening, beräkningsfarmakologi