Clear Sky Science · es
Desbloquear el potencial del descubrimiento fenotípico de fármacos por computación: métodos, desafíos y direcciones futuras
Por qué importa este nuevo modo de encontrar medicamentos
La mayoría de los nuevos medicamentos fracasan en algún punto entre el laboratorio y la clínica, incluso tras años de trabajo y costes enormes. Este artículo explica una alternativa en auge llamada descubrimiento fenotípico de fármacos, que observa cómo los compuestos modifican el comportamiento de células u organismos enteros en lugar de centrarse en una molécula preseleccionada. Con la ayuda de la inteligencia artificial y grandes conjuntos de datos biológicos, este enfoque podría descubrir tratamientos para enfermedades complejas que han resistido los métodos tradicionales.
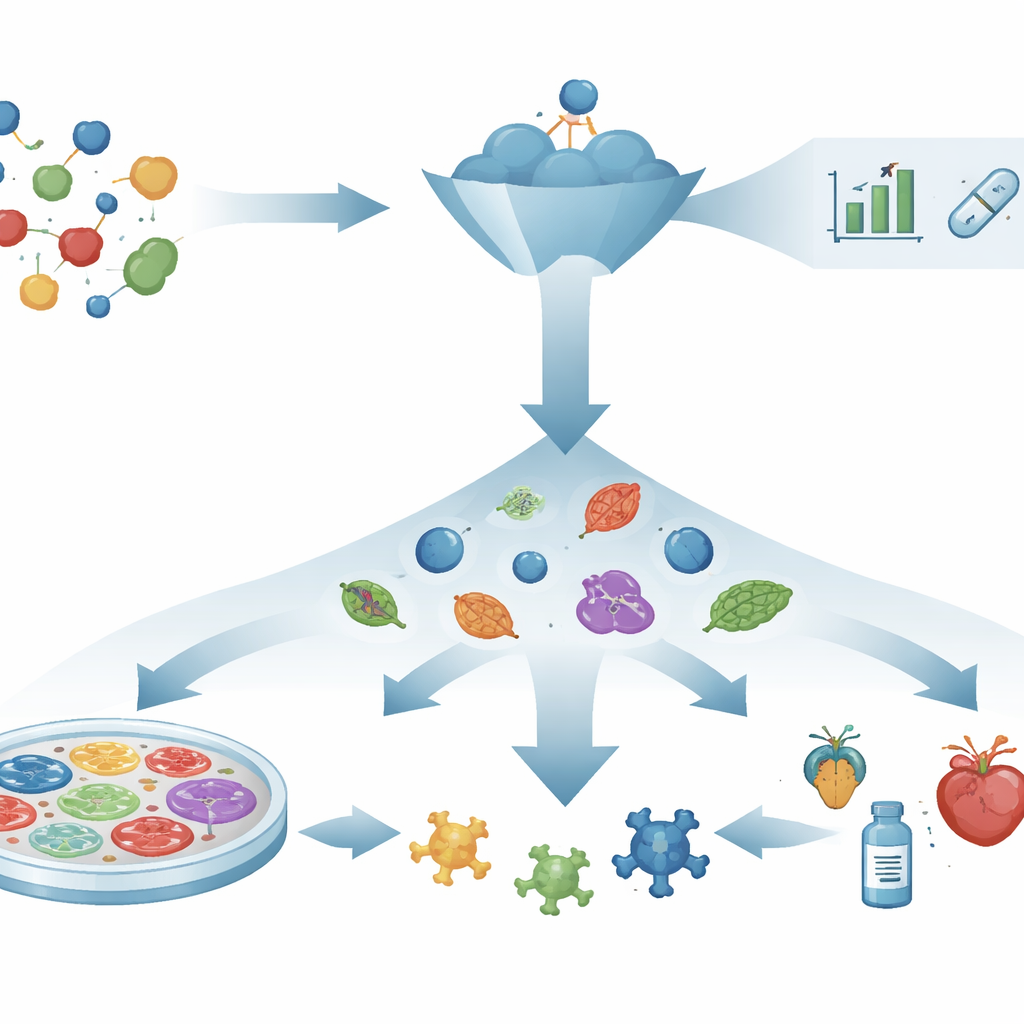
Del pensamiento de cerradura y llave a la observación de sistemas vivos
Durante décadas, el descubrimiento de fármacos ha seguido un guion «primero el mecanismo»: elegir una proteína pensada como causante de la enfermedad, diseñar o buscar compuestos que se unan a ella y esperar que esas interacciones se traduzcan en beneficios reales para la salud. Herramientas potentes como la predicción de estructuras proteicas, el diseño asistido por ordenador y el cribado virtual han acelerado esta búsqueda. Sin embargo, muchos objetivos cuidadosamente seleccionados y moléculas prometedoras siguen sin ayudar a los pacientes, porque cambiar una molécula no siempre arregla una red de enfermedad enmarañada. Esta brecha entre el éxito en tubos de ensayo y el éxito en personas ha reavivado el interés por estrategias que se centran en lo que realmente sucede en sistemas vivos.
Un enfoque que parte del compuesto para detectar cambios útiles
El descubrimiento fenotípico de fármacos invierte el guion. En lugar de empezar con un objetivo conocido, plantea una pregunta más directa: ¿un compuesto empuja un sistema enfermo de vuelta hacia la salud? Los investigadores exponen células, tejidos u organismos pequeños a muchos compuestos y buscan cambios visibles o medibles, como la restauración de la morfología celular, la supervivencia de células frágiles o la recuperación de comportamientos normales. Sólo después de observar un efecto prometedor los científicos investigan cómo actúa el compuesto dentro de la célula. Este enfoque agnóstico respecto al objetivo ya ha dado lugar a medicamentos, por ejemplo para la fibrosis quística y la atrofia muscular espinal, cuyos mecanismos detallados se resolvieron más tarde. Es especialmente útil para enfermedades impulsadas por múltiples vías a la vez, donde escoger un único «objetivo maestro» resulta poco realista.
Convertir lecturas biológicas ricas en números
Los cribados fenotípicos modernos generan cantidades enormes de datos: imágenes de alta resolución de células teñidas, lecturas de actividad génica, mapas de cambios proteicos e incluso el comportamiento de organismos modelo. Para entender esta complejidad, el campo recurre a «embeddings» —formas de convertir la química, las imágenes, la expresión génica y las redes de interacción en huellas numéricas compactas. Estas huellas capturan patrones en cómo se ven los fármacos, cómo alteran las células y cómo se conectan con genes y enfermedades. Modelos de aprendizaje automático, desde algoritmos clásicos hasta redes neuronales profundas y métodos basados en grafos, aprenden entonces a vincular estas huellas con resultados como toxicidad, beneficio probable o similitud con fármacos conocidos. En algunos casos, pueden incluso sugerir nuevos compuestos o nuevos usos para los ya existentes.
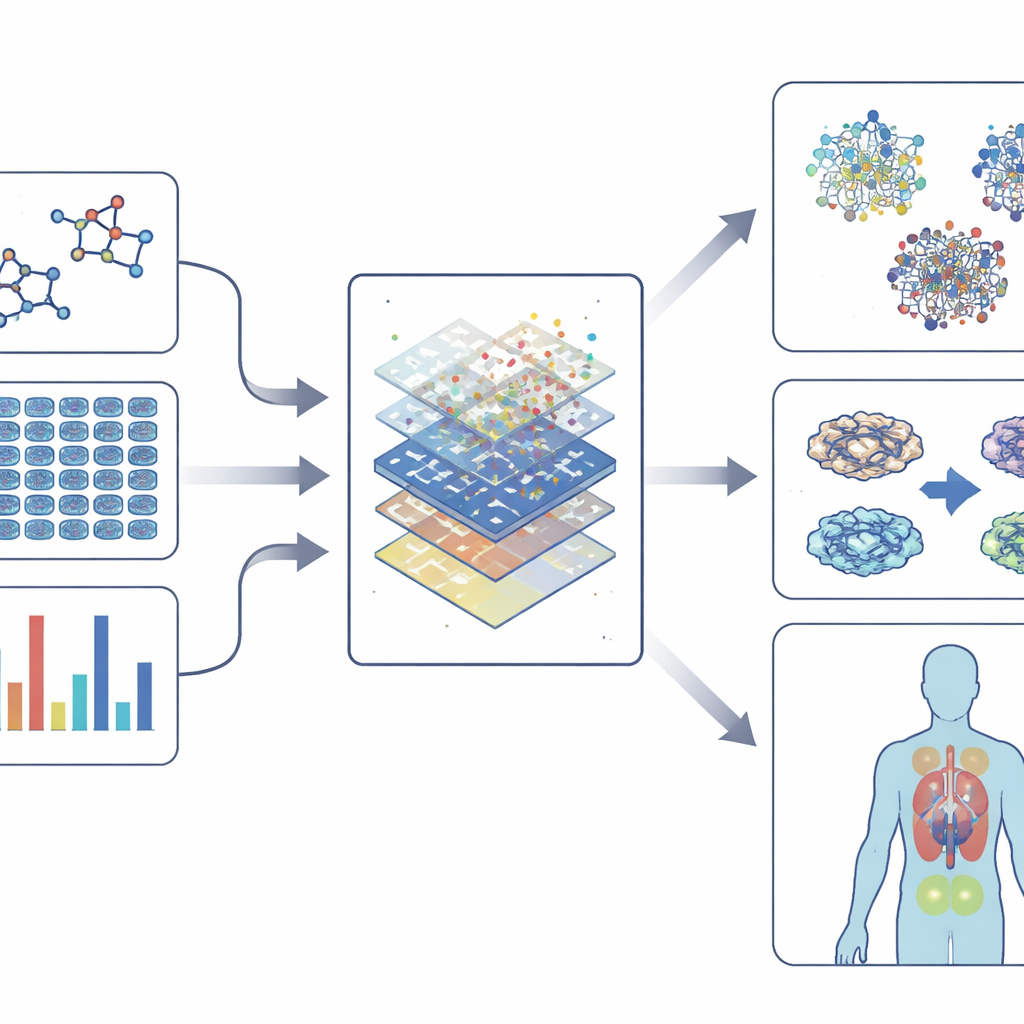
Usar modelos más inteligentes manteniéndolos comprensibles
A medida que los modelos se vuelven más potentes, también corren el riesgo de volverse más opacos. Las herramientas de IA explicable pretenden abrir esta caja negra destacando qué características —como determinados cambios génicos o partes estructurales de una molécula— impulsan una predicción. Esta transparencia ayuda a los investigadores a confiar en los modelos, diseñar compuestos más seguros y entender por qué ocurre un efecto fenotípico, no solo que ocurre. Al mismo tiempo, las tecnologías de célula única y multi-ómica permiten a los científicos ver cómo distintos tipos celulares en un tejido responden a un fármaco, acercando el campo a elecciones terapéuticas más personalizadas.
Obstáculos en el camino hacia mejores medicamentos
A pesar de su promesa, el descubrimiento fenotípico de fármacos afronta desafíos importantes. Los conjuntos de datos de alta calidad siguen siendo fragmentarios e inconsistentes entre laboratorios, lo que dificulta entrenar modelos que generalicen bien. Los ensayos fenotípicos complejos pueden ser difíciles de reproducir, y el paso de un hallazgo en células u animales a una terapia humana segura y eficaz a menudo revela fallos ocultos. Desentrañar cómo funciona un hallazgo fenotípico —el proceso conocido como deconvolución de objetivos— puede ser lento e incierto, especialmente cuando un compuesto actúa sobre varias vías a la vez. Estudios de caso de fármacos fallidos o reposicionados subrayan cómo mecanismos faltantes o mal entendidos pueden llevar a ensayos desperdiciados o a efectos secundarios inesperados.
Hacia dónde se dirige este enfoque
El artículo concluye que el verdadero poder del descubrimiento fenotípico de fármacos vendrá de combinar modelos biológicos ricos con computación avanzada. Células madre derivadas de pacientes, mini-órganos tridimensionales e imágenes de alta resolución pueden proporcionar sistemas de prueba más similares a los humanos, mientras que la IA generativa podría proponer moléculas diseñadas para corregir firmas específicas de enfermedad, incluso en condiciones raras con datos limitados. Si se abordan los problemas de calidad de datos, validación y descubrimiento de mecanismos, esta estrategia que parte del compuesto y es consciente de los sistemas podría hacer el descubrimiento de fármacos más rápido, más eficiente y más alineado con cómo se comportan las enfermedades en pacientes reales.
Cita: Kumar, S., Pal, A. & Chatterjee, S. Unlocking the potential of computational phenotypic drug discovery: methods, challenges, and future directions. npj Syst Biol Appl 12, 46 (2026). https://doi.org/10.1038/s41540-026-00676-5
Palabras clave: descubrimiento fenotípico de fármacos, aprendizaje automático en el descubrimiento de fármacos, reestructuración de fármacos, cribado de alto contenido, farmacología computacional