Clear Sky Science · it
Sbloccare il potenziale della scoperta farmacologica fenotipica computazionale: metodi, sfide e direzioni future
Perché questo nuovo modo di trovare medicine conta
La maggior parte dei nuovi farmaci fallisce da qualche parte tra il laboratorio e la clinica, anche dopo anni di lavoro e costi enormi. Questo articolo spiega un'alternativa in crescita chiamata scoperta farmacologica fenotipica, che osserva come i composti modificano il comportamento di cellule o organismi interi piuttosto che mirare a una singola molecola pre‑selezionata. Con l'aiuto dell'intelligenza artificiale e di grandi set di dati biologici, questo approccio potrebbe rivelare trattamenti per malattie complesse che hanno resistito ai metodi tradizionali.
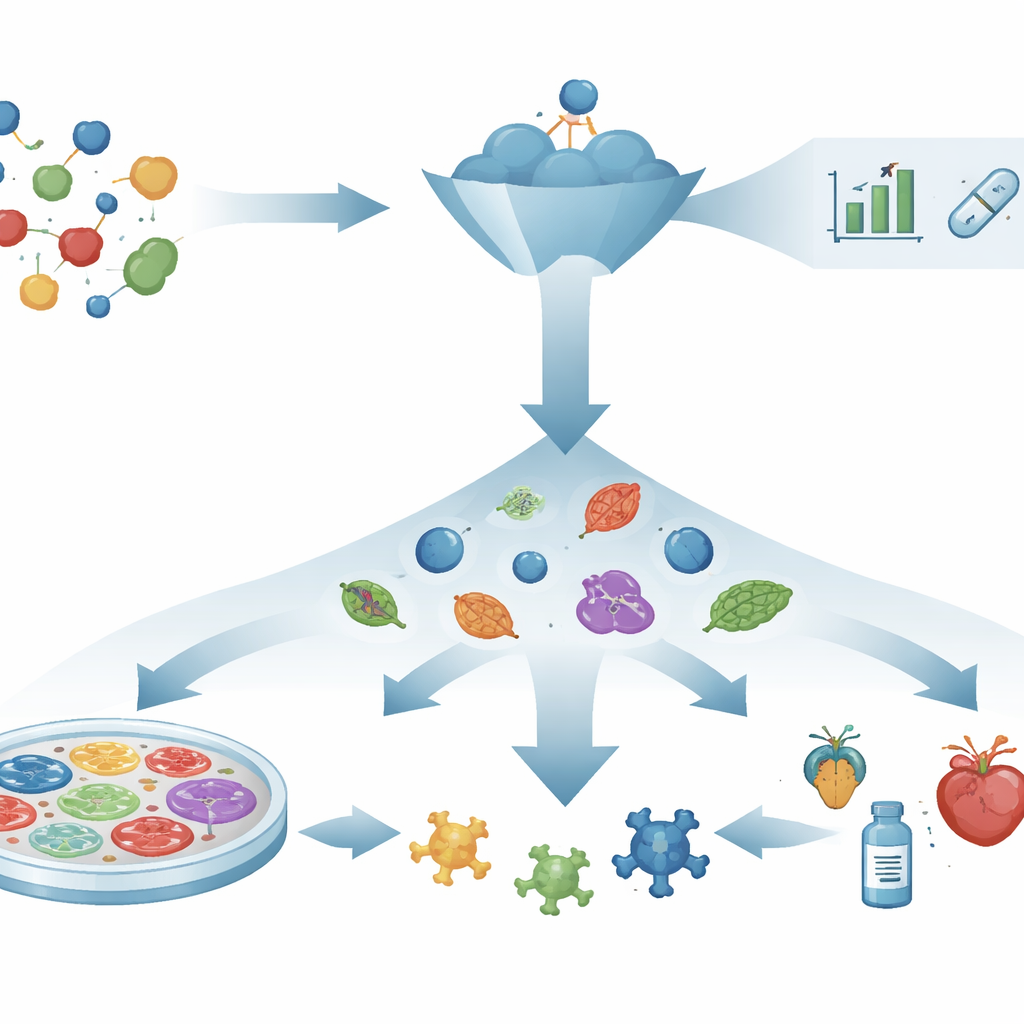
Dal pensiero a serratura‑e‑chiave all'osservazione dei sistemi viventi
Per decenni, la scoperta di farmaci ha seguito uno schema «meccanismo‑prima»: scegliere una singola proteina ritenuta centrale nella malattia, progettare o cercare sostanze chimiche che si leghino ad essa e poi sperare che tali interazioni si traducano in benefici reali per la salute. Strumenti potenti come la predizione della struttura proteica, la progettazione assistita dal computer e lo screening virtuale hanno accelerato questa ricerca. Eppure molti target accuratamente scelti e molecole promettenti continuano a non aiutare i pazienti, perché modificare una singola molecola non risolve sempre una rete patologica complessa. Questo divario tra successo in provetta e successo nell'uomo ha riacceso l'interesse per strategie che si concentrano su ciò che avviene realmente nei sistemi viventi.
Un approccio che parte dal composto per identificare cambiamenti utili
La scoperta farmacologica fenotipica ribalta il copione. Invece di iniziare con un target noto, pone una domanda più diretta: un composto riporta un sistema malato verso la normalità? I ricercatori espongono cellule, tessuti o piccoli organismi a molti composti e cercano cambiamenti visibili o misurabili, come il ripristino della morfologia cellulare, la sopravvivenza di cellule fragili o il recupero di un comportamento normale. Solo dopo aver osservato un effetto promettente gli scienziati indagano come il composto agisca all'interno della cellula. Questo approccio agnostico rispetto al target ha già portato a farmaci come trattamenti per la fibrosi cistica e l'atrofia muscolare spinale, i cui meccanismi dettagliati sono stati chiariti in seguito. È particolarmente utile per malattie guidate da molteplici vie simultanee, dove scegliere un singolo target «maestro» è poco realistico.
Trasformare ricchi riscontri biologici in numeri
Gli screening fenotipici moderni generano enormi quantità di dati: immagini ad alta risoluzione di cellule colorate, profili di attività genica, mappe delle variazioni proteiche e persino il comportamento di organismi modello. Per interpretare questa complessità, il campo si affida agli "embeddings"—metodi per convertire chimica, immagini, espressione genica e reti di interazioni in impronte numeriche compatte. Queste firme catturano i modelli di come appaiono i farmaci, come modificano le cellule e come si collegano a geni e malattie. Modelli di machine learning, dagli algoritmi classici alle reti neurali profonde e ai metodi basati su grafi, imparano quindi a collegare queste impronte a esiti quali tossicità, beneficio potenziale o somiglianza a farmaci noti. In alcuni casi possono persino suggerire nuovi composti o nuovi usi per quelli esistenti.
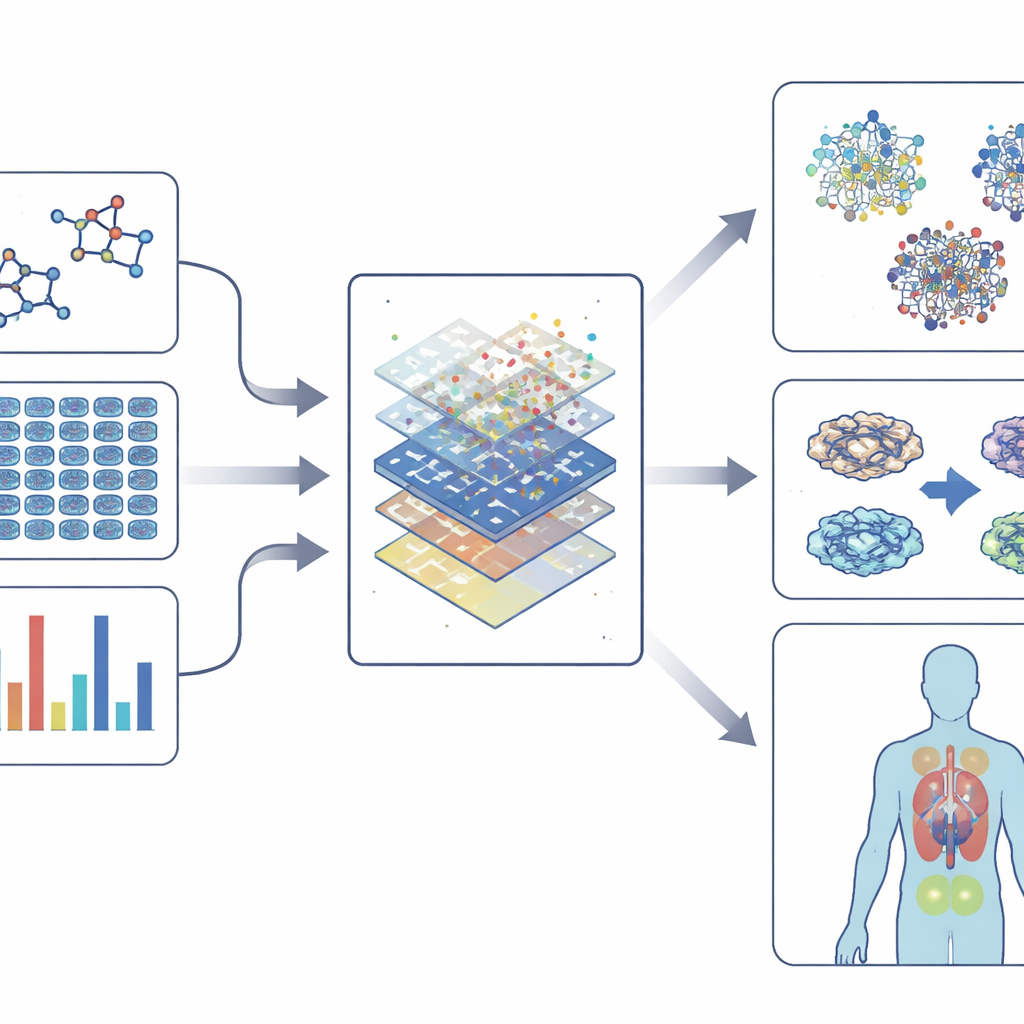
Usare modelli più intelligenti mantenendoli comprensibili
Man mano che i modelli diventano più potenti, rischiano anche di diventare più opachi. Gli strumenti di intelligenza artificiale spiegabile mirano ad aprire questa scatola nera evidenziando quali caratteristiche—come specifiche variazioni geniche o parti strutturali di una molecola—guidano una previsione. Questa trasparenza aiuta i ricercatori a fidarsi dei modelli, progettare composti più sicuri e comprendere perché si verifica un effetto fenotipico, non solo che esso si verifica. Allo stesso tempo, tecnologie a singola cellula e approcci multi‑omici permettono di vedere come diversi tipi cellulari in un tessuto rispondono a un farmaco, avvicinando il campo a scelte terapeutiche più personalizzate.
Ostacoli sulla strada verso farmaci migliori
Nonostante le promesse, la scoperta farmacologica fenotipica affronta sfide importanti. I dataset di alta qualità sono ancora frammentari e incoerenti tra i laboratori, rendendo difficile addestrare modelli che generalizzino bene. Assay fenotipici complessi possono essere difficili da riprodurre, e la transizione da un hit in cellule o animali a una terapia umana sicura ed efficace spesso mette in luce difetti nascosti. Districare come funziona un hit fenotipico—il processo noto come deconvoluzione del target—può essere lento e incerto, specialmente quando un composto agisce su più vie contemporaneamente. Studi di caso su farmaci falliti o riproposti sottolineano come meccanismi mancanti o fraintesi possano portare a trial sprecati o a effetti collaterali inattesi.
Dove sta andando questo approccio
L'articolo conclude che il vero potere della scoperta farmacologica fenotipica deriverà dalla combinazione di modelli biologici ricchi con calcolo avanzato. Cellule staminali derivate da pazienti, mini‑organi tridimensionali e imaging dettagliato possono fornire sistemi di prova più simili all'uomo, mentre l'AI generativa potrebbe proporre molecole su misura per correggere specifiche firme di malattia, anche in condizioni rare con dati limitati. Se si riuscirà a risolvere la qualità dei dati, la validazione e l'identificazione dei meccanismi, questa strategia che parte dal composto e tiene conto dei sistemi potrebbe rendere la scoperta di farmaci più rapida, più efficiente e più in linea con il comportamento delle malattie nei pazienti reali.
Citazione: Kumar, S., Pal, A. & Chatterjee, S. Unlocking the potential of computational phenotypic drug discovery: methods, challenges, and future directions. npj Syst Biol Appl 12, 46 (2026). https://doi.org/10.1038/s41540-026-00676-5
Parole chiave: scoperta farmacologica fenotipica, apprendimento automatico nella scoperta di farmaci, riproporzionamento di farmaci, screening ad alto contenuto, farmacologia computazionale