Clear Sky Science · tr
Fenotipik hesaplamalı ilaç keşfinin potansiyelini açığa çıkarma: yöntemler, zorluklar ve gelecek yönleri
Neden bu yeni ilaç bulma yöntemi önemli
Yeni ilaçların çoğu, yıllarca süren çalışmalar ve büyük maliyetlere rağmen laboratuvardan kliniğe giderken başarısız olur. Bu makale, önceden seçilmiş tek bir moleküle odaklanmak yerine bileşenlerin tüm hücrelerin veya organizmaların davranışını nasıl değiştirdiğini inceleyen yükselen bir alternatif olan fenotipik ilaç keşfini açıklar. Yapay zeka ve büyük biyolojik veri kümelerinin yardımıyla bu yaklaşım, geleneksel yöntemlere direnç gösteren kompleks hastalıklar için yeni tedaviler ortaya çıkarabilir.
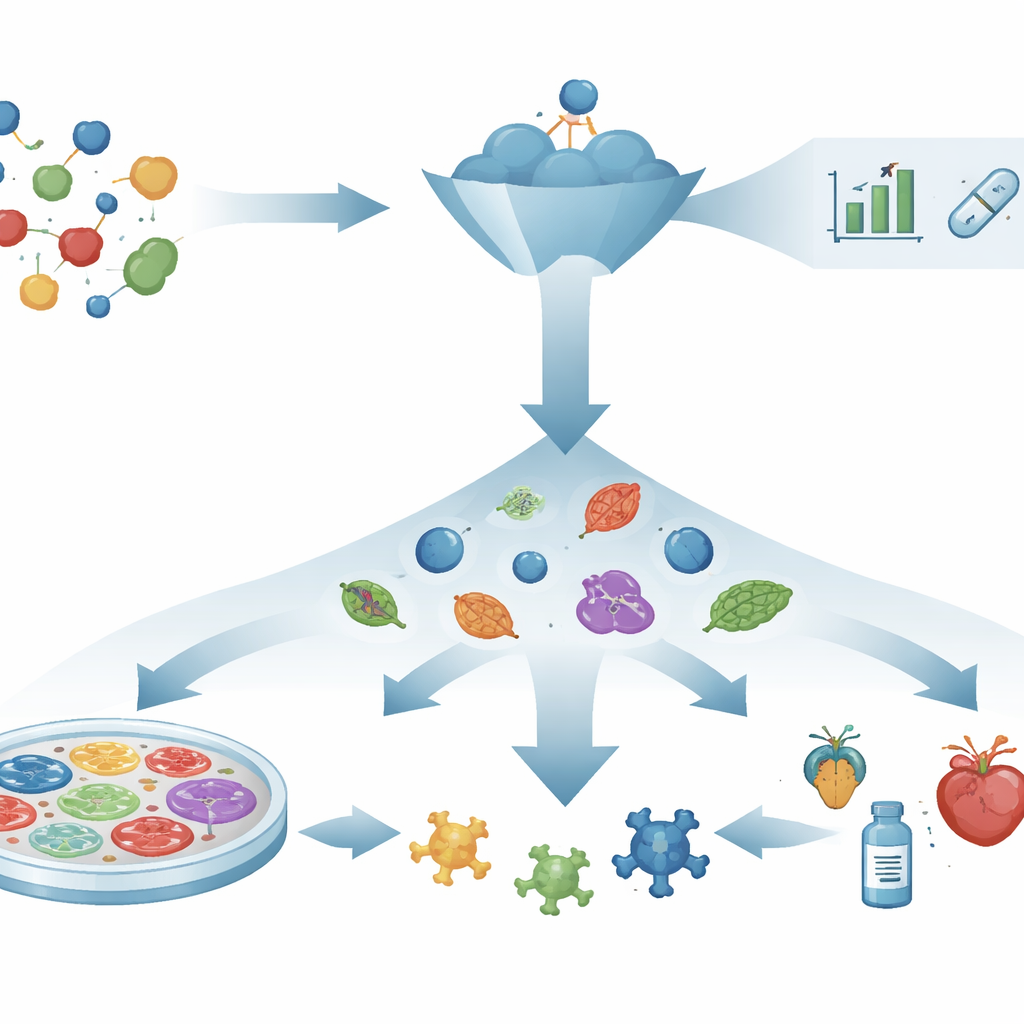
Kilit‑ve‑anahtar düşüncesinden canlı sistemleri gözlemlemeye
On yıllardır ilaç keşfi "önce mekanizma" senaryosunu izledi: hastalığı yönlendirdiği düşünülen tek bir proteini seç, ona bağlanan kimyasalları tasarla veya ara, sonra bu etkileşimlerin gerçek sağlık yararlarına dönüşmesini um. Protein yapı tahmini, bilgisayar destekli tasarım ve sanal tarama gibi güçlü araçlar bu aramayı hızlandırdı. Yine de özenle seçilmiş hedefler ve umut verici moleküller hâlâ hastalara yardımcı olamayabiliyor; çünkü tek bir molekülü değiştirmek, düğümlenmiş bir hastalık ağını her zaman düzeltmiyor. Deney tüplerindeki başarı ile insanlar üzerindeki başarısızlık arasındaki bu uçurum, canlı sistemlerde gerçekte nelerin olduğunu merkeze alan stratejilere yeniden ilgi uyandırdı.
Yararlı değişiklikleri tespit etmenin önce bileşik yaklaşımı
Fenotipik ilaç keşfi anlatıyı tersine çevirir. Bilinen bir hedefle başlamaktan ziyade daha doğrudan bir soru sorar: bir bileşik hasta sistemi sağlığa geri itiyor mu? Araştırmacılar hücreleri, dokuları veya küçük organizmaları çok sayıda bileşiğe maruz bırakır ve hücre şeklinin düzelmesi, hassas hücrelerin hayatta kalması veya normal davranışın geri kazanılması gibi gözle görülür ya da ölçülebilir değişiklikleri ararlar. Ümit verici bir etki görüldükten sonra bilim insanları bileşiğin hücre içinde nasıl çalıştığını araştırır. Bu hedeften bağımsız yaklaşım, mekanizmaları daha sonra çözülen kistik fibrozis ve spinal müsküler atrofi için tedaviler gibi ilaçların geliştirilmesine zaten yol açtı. Birden çok yolak tarafından yönlendirilen hastalıklar için, tek bir "baş" hedef seçmenin gerçekçi olmadığı durumlarda özellikle yararlıdır.
Zengin biyolojik çıktıları sayılara dönüştürmek
Modern fenotipik taramalar büyük miktarda veri üretir: boyanmış hücrelerin yüksek çözünürlüklü görüntüleri, gen aktivite okumaları, protein değişikliklerinin haritaları ve hatta model organizmaların davranışları. Bu karmaşıklığı anlamlı hale getirmek için alan, kimya, görüntüler, gen ifade verileri ve etkileşim ağlarını kompakt sayısal parmak izlerine dönüştürme yolları olan "gömme" yöntemlerine dayanır. Bu parmak izleri ilaçların nasıl göründüğü, hücreleri nasıl değiştirdiği ve genler ile hastalıklarla nasıl bağlantı kurduğuna dair kalıpları yakalar. Klasik algoritmalardan derin sinir ağlarına ve grafik tabanlı yöntemlere kadar makine öğrenmesi modelleri, bu parmak izlerini toksisite, muhtemel fayda veya bilinen ilaçlara benzerlik gibi sonuçlarla ilişkilendirmeyi öğrenir. Bazı durumlarda yeni bileşikler veya mevcutların yeni kullanımları bile önerilebilir.
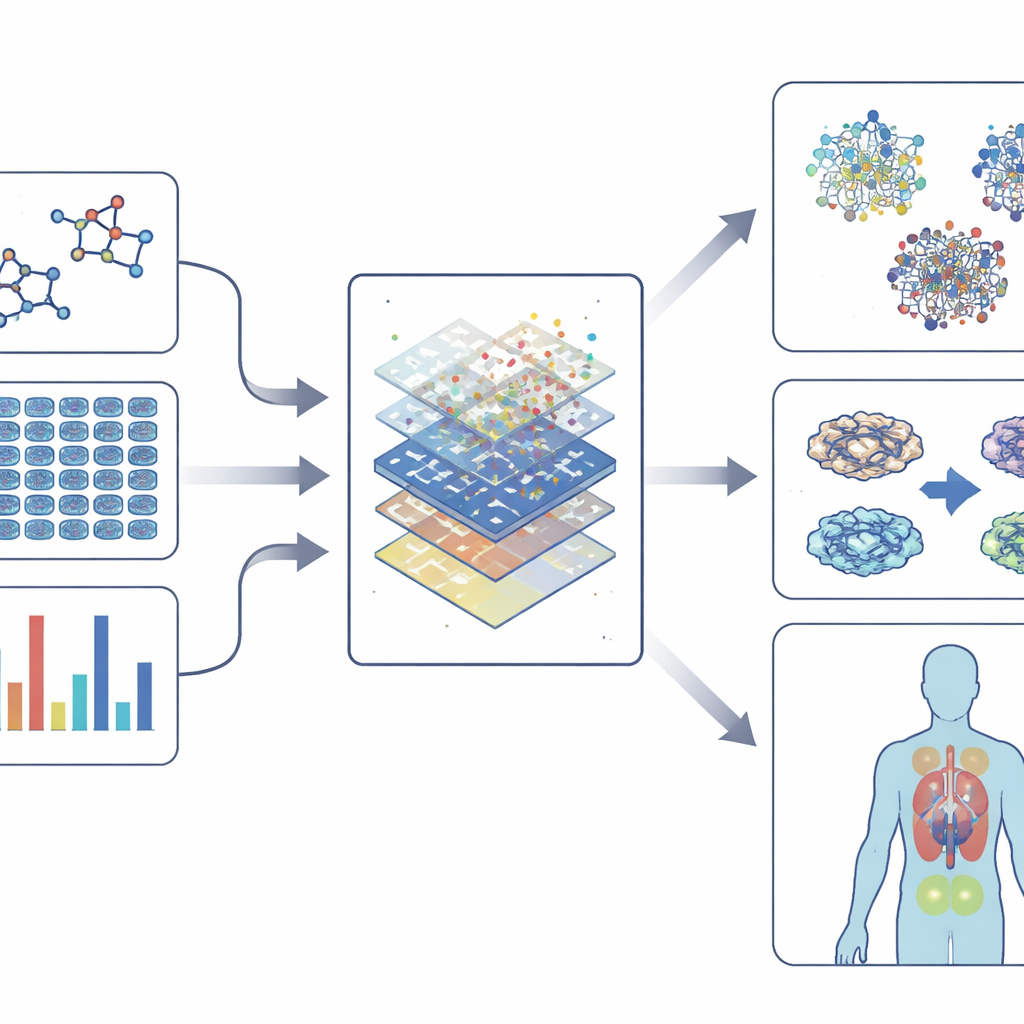
Daha akıllı modeller kullanırken anlaşılabilirliği korumak
Modeller güçlendikçe, aynı zamanda daha opak hale gelme riski taşırlar. Açıklanabilir yapay zeka araçları, bir tahmini hangi özelliklerin—örneğin belirli gen değişiklikleri veya bir molekülün yapısal parçaları—sürüklediğini vurgulayarak bu kara kutuyu açmayı amaçlar. Bu şeffaflık, araştırmacıların modellere güvenmesini, daha güvenli bileşikler tasarlamasını ve yalnızca bir fenotipik etkinin varlığını değil nedenini de anlamasını sağlar. Aynı zamanda tek hücre ve çoklu omik teknolojileri, bir dokudaki farklı hücre tiplerinin bir ilaçtaki tepkilerini görmeyi mümkün kılarak alanı kişiselleştirilmiş tedavi seçeneklerine daha da yaklaştırır.
Daha iyi ilaçlara giden yoldaki engeller
Ümidine rağmen fenotipik ilaç keşfi önemli zorluklarla karşılaşıyor. Yüksek kaliteli veri kümeleri hâlâ düzensiz ve laboratuvarlar arasında tutarsız; bu da iyi genelleşen modeller eğitmeyi zorlaştırıyor. Karmaşık fenotipik testler yeniden üretmesi güç olabilir ve hücrelerde veya hayvanlarda elde edilen bir etkinliğin güvenli, etkili bir insan tedavisine dönüşmesi genellikle gizli kusurları ortaya çıkarır. Bir fenotipik etkinin nasıl çalıştığını çözmek—hedef dekonvolüsyonu olarak bilinen süreç—özellikle bir bileşik birden çok yolakta etki ettiğinde yavaş ve belirsiz olabilir. Başarısız veya yeniden konumlandırılmış ilaçlara dair vaka çalışmaları, eksik veya yanlış anlaşılan mekanizmaların boşa harcanmış denemelere veya beklenmeyen yan etkilere yol açabileceğini gösterir.
Bu yaklaşımın bir sonraki adımları
Makale, fenotipik ilaç keşfinin gerçek gücünün zengin biyolojik modeller ile ileri hesaplamanın birleşiminden geleceğini sonucuna varıyor. Hastadan türetilmiş kök hücreler, üç boyutlu mini‑organlar ve ayrıntılı görüntüleme daha insan benzeri test sistemleri sağlayabilirken, üretken yapay zeka belirli hastalık imzalarını düzeltmeye yönelik moleküller önerebilir; bu nadir durumlarda sınırlı veriler olsa bile geçerlidir. Veri kalitesi, doğrulama ve mekanizma bulma konularındaki sorunlar çözülebilirse, bu bileşik‑öncelikli, sistemleri gözeten strateji ilaç keşfini daha hızlı, daha verimli ve gerçek hastalıklara daha yakın hale getirebilir.
Atıf: Kumar, S., Pal, A. & Chatterjee, S. Unlocking the potential of computational phenotypic drug discovery: methods, challenges, and future directions. npj Syst Biol Appl 12, 46 (2026). https://doi.org/10.1038/s41540-026-00676-5
Anahtar kelimeler: fenotipik ilaç keşfi, ilaç keşfinde makine öğrenmesi, ilaç yeniden konumlandırma, yüksek içerikli tarama, hesaplamalı farmakoloji