Clear Sky Science · pl
Wykorzystanie potencjału obliczeniowego odkrywania leków fenotypowych: metody, wyzwania i kierunki na przyszłość
Dlaczego ten nowy sposób poszukiwania leków ma znaczenie
Większość nowych leków zawodzi gdzieś pomiędzy laboratorium a kliniką, mimo wieloletnich badań i ogromnych kosztów. Ten artykuł wyjaśnia rosnącą alternatywę zwaną odkrywaniem leków fenotypowych, która obserwuje, jak związki zmieniają zachowanie całych komórek lub organizmów, zamiast celować w pojedynczą uprzednio wybraną cząsteczkę. Przy wsparciu sztucznej inteligencji i dużych zbiorów danych biologicznych to podejście może ujawnić terapie dla złożonych chorób, które opierały się tradycyjnym metodom.
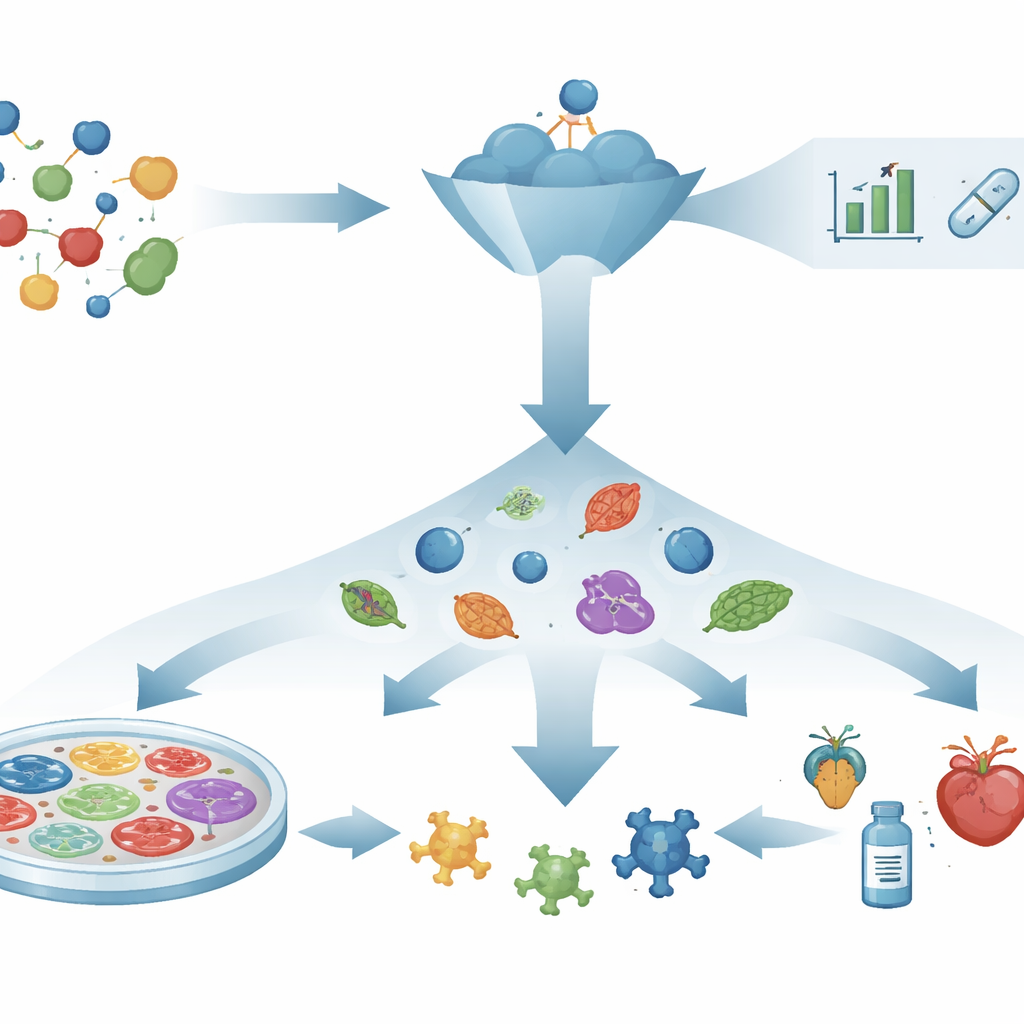
Od myślenia „zamek‑i‑klucz” do obserwacji systemów żywych
Przez dekady odkrywanie leków podążało za scenariuszem „mechanizm‑najpierw”: wybierz pojedyncze białko uważane za motor choroby, zaprojektuj lub wyszukaj związki, które się z nim wiążą, a następnie miej nadzieję, że te interakcje przełożą się na rzeczywiste korzyści zdrowotne. Potężne narzędzia, takie jak przewidywanie struktur białek, komputerowe projektowanie i wirtualny screening, przyspieszyły te poszukiwania. Mimo to wiele starannie wybranych celów i obiecujących cząsteczek nadal nie pomaga pacjentom, ponieważ zmiana jednego elementu nie zawsze naprawia splątane sieci chorobowe. Ta przepaść między sukcesem w probówkach a sukcesem u ludzi wzbudziła odnowione zainteresowanie strategiami skupionymi na tym, co rzeczywiście dzieje się w systemach żywych.
Podejście „związek‑najpierw” do wykrywania pomocnych zmian
Odkrywanie leków fenotypowych odwraca ten scenariusz. Zamiast zaczynać od znanego celu, stawia pytanie bardziej bezpośrednie: czy związek przesuwa chory system w stronę zdrowia? Badacze eksponują komórki, tkanki lub małe organizmy na wiele związków i szukają widocznych lub mierzalnych zmian, takich jak przywrócenie kształtu komórki, przeżycie wrażliwych komórek lub odzyskanie normalnego zachowania. Dopiero po zaobserwowaniu obiecującego efektu naukowcy badają, jak związek działa wewnątrz komórki. To podejście niezależne od celu doprowadziło już do leków, na przykład terapii mukowiscydozy i rdzeniowego zaniku mięśni, których szczegółowe mechanizmy wyjaśniono później. Jest ono szczególnie przydatne w chorobach napędzanych wieloma ścieżkami jednocześnie, gdzie wybór pojedynczego „głównego” celu jest nierealistyczny.
Przekształcanie bogatych biologicznych odczytów w liczby
Nowoczesne ekrany fenotypowe generują olbrzymie ilości danych: obrazy o wysokiej rozdzielczości barwionych komórek, odczyty aktywności genów, mapy zmian białek, a nawet zachowanie organizmów modelowych. Aby zrozumieć tę złożoność, dziedzina opiera się na „osadzeniach” (embeddings) — sposobach konwertowania informacji o chemii, obrazach, ekspresji genów i sieciach oddziaływań na zwarte numeryczne odciski palców. Te odciski ujmują wzorce w wyglądzie leków, w tym jak zmieniają komórki i jak łączą się z genami i chorobami. Modele uczenia maszynowego, od klasycznych algorytmów po głębokie sieci neuronowe i metody oparte na grafach, uczą się łączyć te odciski z wynikami, takimi jak toksyczność, prawdopodobna korzyść czy podobieństwo do znanych leków. W niektórych przypadkach mogą nawet sugerować nowe związki lub nowe zastosowania istniejących leków.
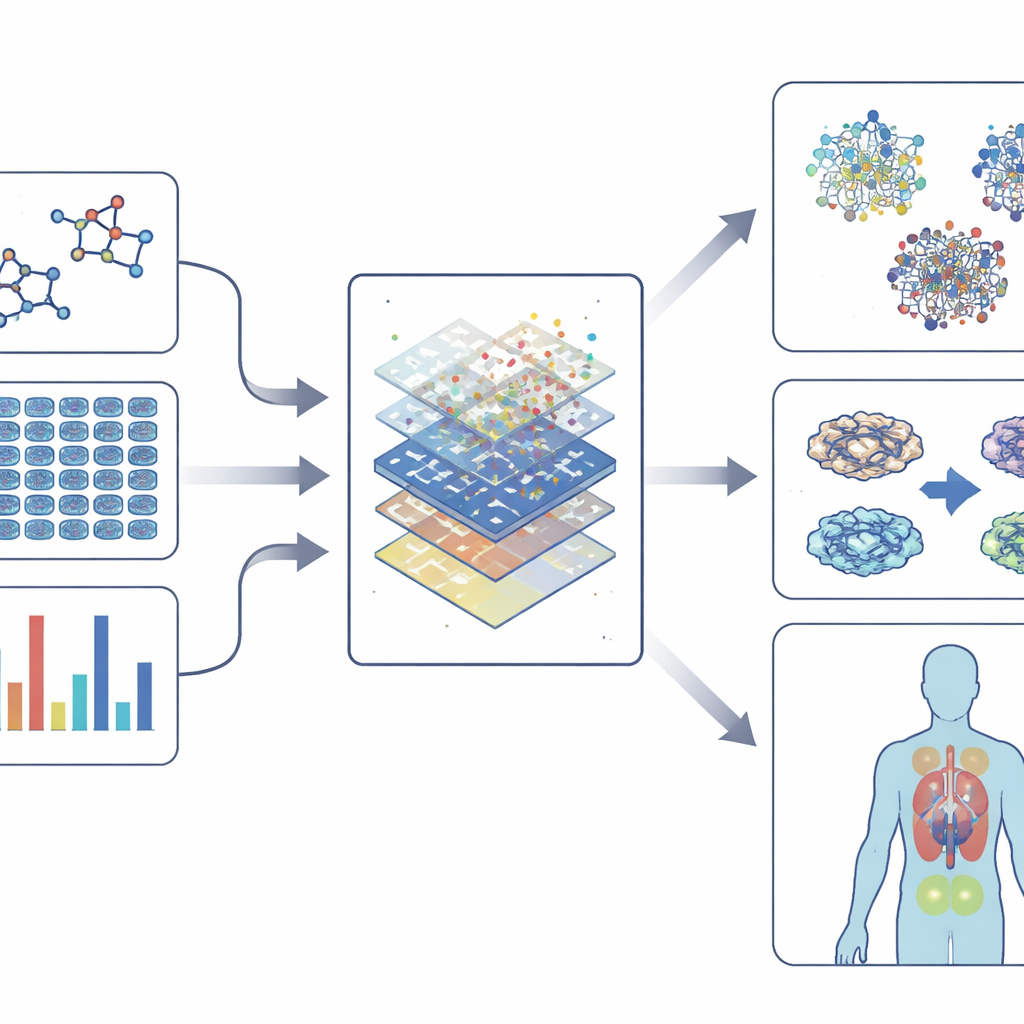
Używanie mądrzejszych modeli przy zachowaniu ich zrozumiałości
W miarę jak modele stają się potężniejsze, istnieje też ryzyko, że staną się bardziej nieprzejrzyste. Narzędzia wyjaśnialnej sztucznej inteligencji dążą do otwarcia tej czarnej skrzynki, podkreślając, które cechy — na przykład konkretne zmiany genów lub fragmenty struktury cząsteczki — napędzają predykcję. Ta przejrzystość pomaga badaczom zaufać modelom, projektować bezpieczniejsze związki i zrozumieć, dlaczego występuje efekt fenotypowy, a nie tylko że on występuje. Równocześnie technologie jednokomórkowe i multi‑omics pozwalają naukowcom zobaczyć, jak różne typy komórek w tkance reagują na lek, przybliżając dziedzinę do spersonalizowanych wyborów terapeutycznych.
Przeszkody na drodze do lepszych leków
Pomimo obietnic, odkrywanie leków fenotypowych napotyka poważne wyzwania. Zbiory danych wysokiej jakości są wciąż niejednolite i niespójne między laboratoriami, co utrudnia trenowanie modeli o dobrej generalizacji. Złożone testy fenotypowe mogą być trudne do odtworzenia, a przejście od „hitu” w komórkach lub zwierzętach do bezpiecznej, skutecznej terapii u ludzi często ujawnia ukryte wady. Rozwiązanie, jak działa trafienie fenotypowe — proces znany jako dekonwolucja celu — może być powolne i niepewne, zwłaszcza gdy związek działa na kilka ścieżek jednocześnie. Studium przypadków nieudanych lub przerepurposjonowanych leków podkreśla, jak brakujące lub źle zrozumiane mechanizmy mogą prowadzić do zmarnowanych prób klinicznych lub niespodziewanych działań niepożądanych.
Dokąd zmierza to podejście
Artykuł konkluduje, że prawdziwa siła odkrywania leków fenotypowych wynika z łączenia bogatych modeli biologicznych z zaawansowanymi metodami obliczeniowymi. Komórki macierzyste pochodzące od pacjentów, trójwymiarowe mini‑organy i szczegółowe obrazowanie mogą dostarczyć bardziej ludzkopodobnych systemów testowych, podczas gdy generatywna AI może proponować cząsteczki dostosowane do korekty konkretnych sygnatur chorobowych, nawet w rzadkich schorzeniach z ograniczonymi danymi. Jeśli uda się rozwiązać problemy jakości danych, walidacji i odnajdywania mechanizmów, to podejście „związek‑najpierw”, świadome systemowo, może uczynić odkrywanie leków szybszym, bardziej efektywnym i bliższym temu, jak choroby zachowują się u rzeczywistych pacjentów.
Cytowanie: Kumar, S., Pal, A. & Chatterjee, S. Unlocking the potential of computational phenotypic drug discovery: methods, challenges, and future directions. npj Syst Biol Appl 12, 46 (2026). https://doi.org/10.1038/s41540-026-00676-5
Słowa kluczowe: odkrywanie leków fenotypowych, uczenie maszynowe w odkrywaniu leków, ponowne zastosowanie leków, skrinning wysokiej zawartości, farmakologia obliczeniowa