Clear Sky Science · zh
经实验校准的多尺度模型预测依赖给药时序的药物联合效应
为何时机在癌症用药中至关重要
癌症治疗不仅关乎选择合适的药物,也关乎以合适的方式和时间给药。许多在简单体外培养皿中看起来很有潜力的药物组合,在真实肿瘤中效果会大打折扣——在那里药物分布不均,细胞以复杂且协调的方式响应。该研究引入了一个计算模型,将单个癌细胞内发生的事情与整个细胞团块的行为连接起来,展示了两种药物的顺序与时机如何决定是仅能适度放缓生长,还是导致肿瘤显著崩溃。 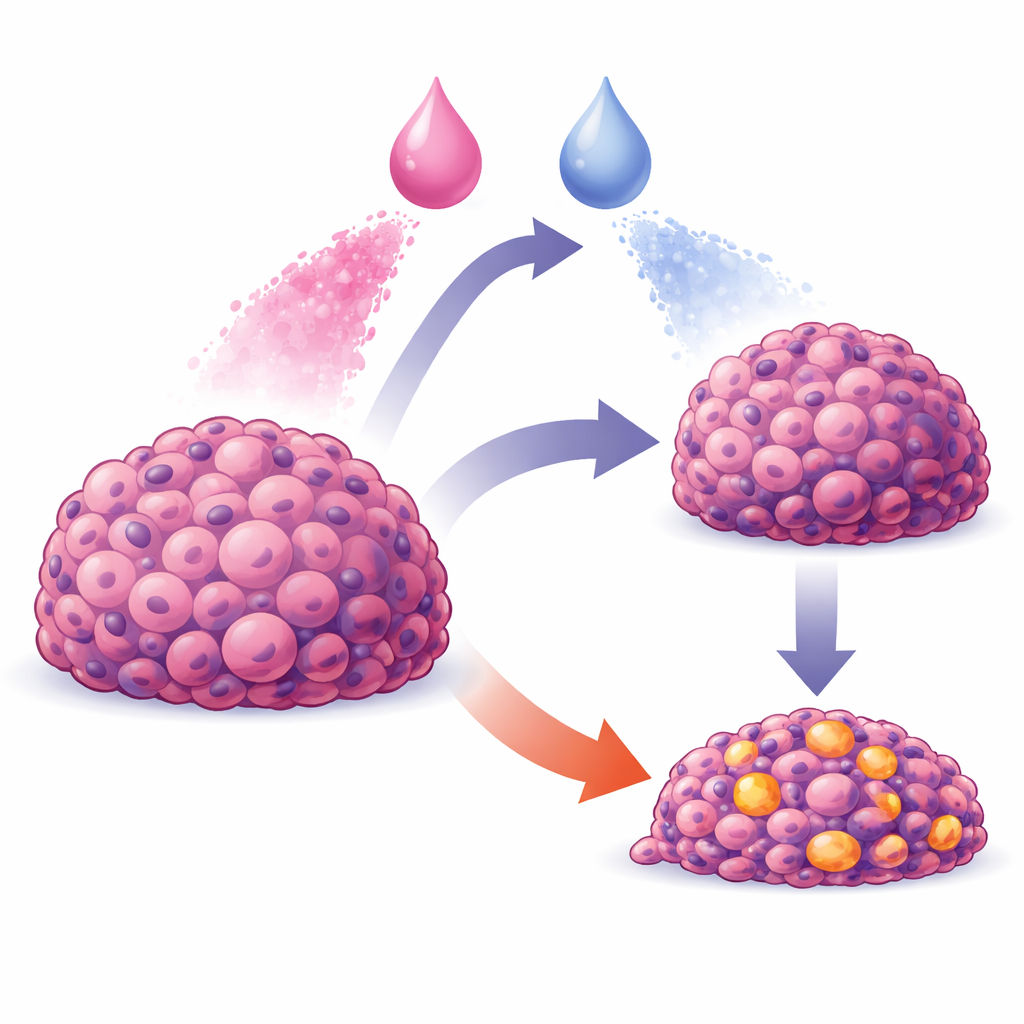
将单细胞与整体肿瘤联系起来
研究者将注意力集中在一种名为 AGS 的人类胃(stomach)癌细胞系上,建立了一个“多尺度”模型以反映其行为。在最细致的层面,每个虚拟细胞携带一个简化的关键信号分子连接图,决定细胞是生长还是死亡。这些内部开关表示为活跃或不活跃,但以允许分级响应的方式组合。在更高层面,每个细胞是模拟组织中的独立主体:细胞相互推动,感到拥挤时停止分裂,并可根据其内部信号选择死亡或继续生长。在更高一层,药物与营养物在虚拟环境中扩散,模拟物质如何进入并穿过类似肿瘤的细胞团簇。
用单药数据训练模型
为了使虚拟系统具备现实性,团队首先用 AGS 细胞在未经处理或暴露于单一药物时的真实生长时间序列数据对模型进行了训练。他们使用了三种与癌症治疗相关的靶向抑制剂:分别抑制 PI3K、MEK 和 AKT,这些蛋白位于促进细胞存活与分裂的通路上。通过在高性能计算机上运行的强大优化算法,他们调整了控制细胞分裂速率、对拥挤的敏感性、药物穿过细胞膜的难易程度以及内部信号如何转化为生长或死亡的参数。用这些参数设置,模型能够紧密再现观测到的生长曲线:一种药物主要减慢生长,另一种在短暂激增后导致细胞回缩,第三种则随时间持续降低细胞群体数量。
在未见联合数据的情况下预测协同作用
一旦模型能模拟单药行为,关键测试就是在未使用任何联合用药数据训练的情况下,能否预测药物联合的结果。研究者构建了与三种单药拟合一致的参数范围,然后针对两对已知具有协同效应的组合——PI3K 加 MEK 抑制以及 AKT 加 MEK 抑制——运行了数千次虚拟实验。令人惊讶的是,模拟的组合再现了真实实验中观察到的比预期更强的生长抑制。模型显示,每一对药物通过不同的优势相互补充:一种药物强力阻断生长信号,另一种推动细胞走向自我毁灭。二者共同既关闭促存活信号,又增强促死亡信号,促使比单独使用任何一种药物都多得多的细胞死亡。 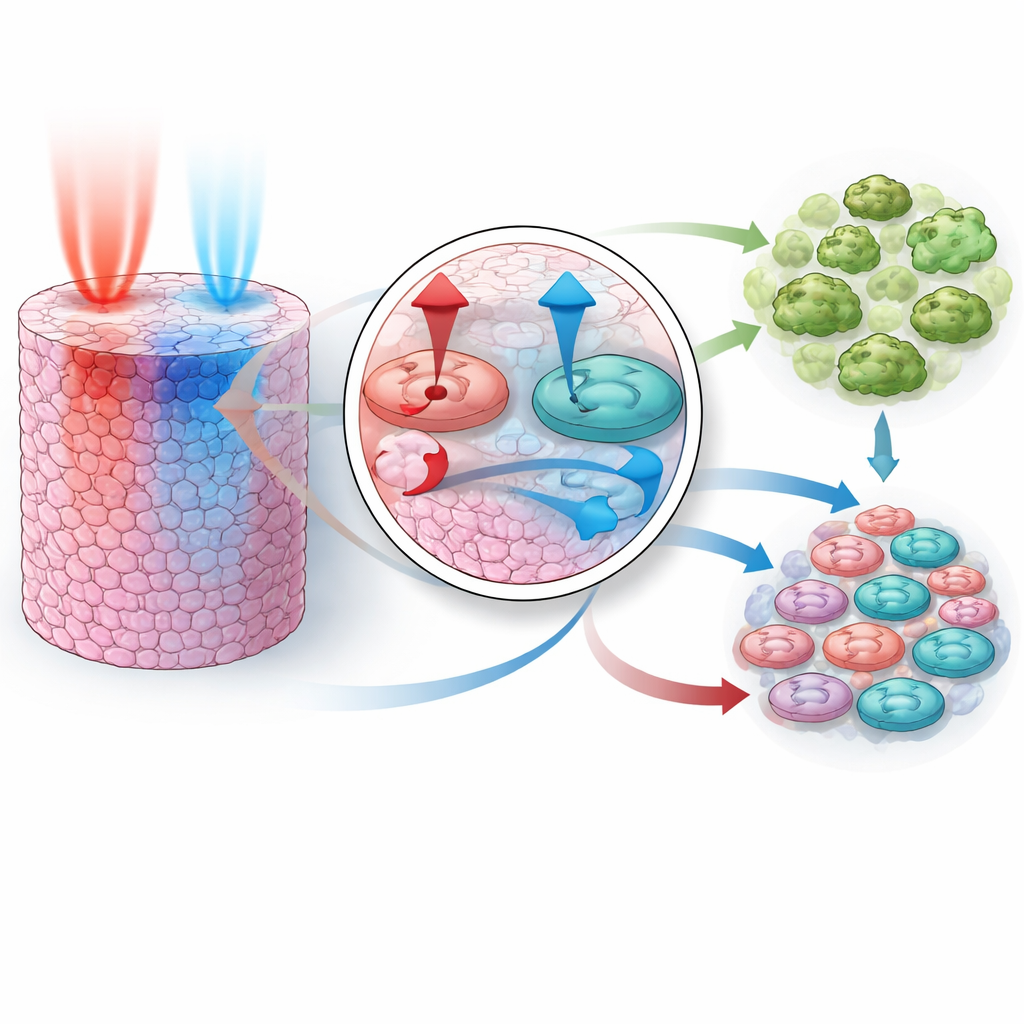
洞察协同作用的机制
由于模型从分子开关追踪到群体结局,它能够提出协同作用产生机制的假说。对于 PI3K 与 MEK 抑制剂,模拟表明细胞整体上被“致死性预激(primed)”:触发凋亡的阈值降低,执行细胞死亡的内部机制变得更活跃,尤其是经由 Caspase-9 相关通路。对于 AKT 与 MEK 组合,模型指向了不同的路径:与生长促进因子相关的生存信号被抑制,而一个鼓励细胞死亡的反向因子获得了更大影响力。在这种情况下,协同作用似乎更依赖于由 Caspase-8 驱动的替代死亡途径。这些不同的机制凸显出相同的总体结果——更强的杀伤作用——可以通过不同的内部线路实现。
时序与药物运输影响疗效
研究团队随后将模型扩展到三维,以模拟一个小型实体肿瘤,其中药物从一侧进入,必须向内层细胞扩散。在这一更逼真的设置下,他们探索了两药同时给药,或一种药在另一种之前不同时长给药时会发生什么,以及两种药物在组织中扩散速度的变化如何影响结果。模拟揭示了一个明确规则:受 PI3K 与 AKT 控制的通路必须在或早于受 MEK 控制的通路被抑制时,组合疗法才能高度有效。如果先抑制 MEK,网络内的反馈会允许 PI3K/AKT 活性回弹,暂时挽救细胞存活并削弱总体效果。每种药物扩散速度的差异会放大这一影响,意味着即使在病人层面上看似“同时”给药,实际到达细胞的顺序也可能不同。
这对未来癌症治疗意味着什么
这项工作表明,一个以单药实验为基础精心校准的计算模型,能够成功预测药物对随时间演化的表现并解释为何给药顺序重要。通过将细胞内的分子逻辑与整个细胞群体的行为以及药物的物理运动联系起来,该框架可以产生具体且可检验的建议,关于哪些给药时程在实验室中以及最终在患者中最有可能奏效。虽然当前结果特定于一种胃癌细胞系,但相同方法可被改编用于其他癌症,帮助研究人员设计更智能的组合与时机策略,而不是仅依赖反复试验。
引用: Hayoun-Mya, O., Montagud, A., Valencia, A. et al. Experimentally calibrated multiscale model predicts schedule dependent drug combination effects. npj Syst Biol Appl 12, 52 (2026). https://doi.org/10.1038/s41540-026-00669-4
关键词: 癌症药物组合, 多尺度建模, 给药时序, 胃癌, 计算肿瘤学