Clear Sky Science · pt
Modelo multiescala calibrado experimentalmente prevê efeitos de combinações de drogas dependentes da programação
Por que o tempo importa no tratamento do câncer
O tratamento do câncer não é apenas escolher os fármacos certos; trata‑se também de administrá‑los da maneira correta e no momento adequado. Muitos pares de drogas promissores parecem eficazes em culturas simples de laboratório, mas perdem potência em tumores reais, onde os fármacos se difundem de forma desigual e as células respondem de maneiras complexas e coordenadas. Este estudo apresenta um modelo computacional que conecta o que ocorre dentro de células cancerosas individuais ao que acontece em uma massa inteira de células, e mostra como a ordem e o tempo de administração de dois fármacos podem determinar a diferença entre um abrandamento modesto do crescimento e o colapso dramático do tumor. 
Ligando células individuais a tumores inteiros
Os pesquisadores concentraram‑se em uma linhagem humana de câncer gástrico chamada AGS e construíram um modelo “multiescala” que espelha seu comportamento. No nível mais detalhado, cada célula virtual carrega um diagrama simplificado das conexões entre moléculas sinalizadoras chave que decidem se a célula cresce ou morre. Esses interruptores internos são representados como ativos ou inativos, mas combinados de forma a permitir respostas graduais. Em um nível superior, cada célula é um agente independente em um tecido simulado: as células empurram umas às outras, param de se dividir quando se sentem congestionadas e podem morrer ou continuar crescendo dependendo de seus sinais internos. Acima disso, drogas e nutrientes difundem‑se por um ambiente virtual, imitando como as substâncias entram e atravessam um aglomerado semelhante a um tumor.
Ensinando o modelo com dados de droga única
Para tornar o sistema virtual realista, a equipe primeiro o treinou com medições reais de como as células AGS crescem ao longo do tempo quando não tratadas ou expostas a drogas únicas. Eles usaram três inibidores direcionados relevantes para o tratamento do câncer: um bloqueando PI3K, outro bloqueando MEK e outro bloqueando AKT, todos proteínas em vias que promovem a sobrevivência e a divisão celular. Usando algoritmos de otimização potentes rodando em computadores de alto desempenho, ajustaram parâmetros que controlam a velocidade de divisão celular, a sensibilidade ao aperto celular, a facilidade com que as drogas atravessam membranas celulares e como os sinais internos são convertidos em crescimento ou morte. Com esses ajustes, o modelo reproduziu de perto as curvas de crescimento observadas: uma droga principalmente retardou o crescimento, outra fez as células encolherem após um breve pico, e uma terceira reduziu continuamente a população ao longo do tempo.
Prevendo sinergia sem vê‑la
Uma vez que o modelo conseguiu imitar o comportamento de droga única, o teste chave foi se ele poderia prever o que acontece quando as drogas são combinadas, sem ter visto quaisquer dados de combinação durante o treinamento. Os pesquisadores construíram intervalos de parâmetros consistentes com os três ajustes de droga única e então executaram milhares de experimentos virtuais para dois pares sinérgicos conhecidos: inibição de PI3K mais MEK, e inibição de AKT mais MEK. Surpreendentemente, as combinações simuladas reproduziram a supressão do crescimento mais forte do que o esperado observada em experimentos reais. O modelo mostrou que cada par funciona por meio da mistura de forças diferentes: uma droga bloqueia fortemente os sinais de crescimento, a outra empurra as células em direção à autodestruição. Juntas, elas desligam tanto as pistas pró‑sobrevivência quanto reforçam os sinais pró‑morte, levando uma fração muito maior de células à morte do que qualquer uma delas isoladamente. 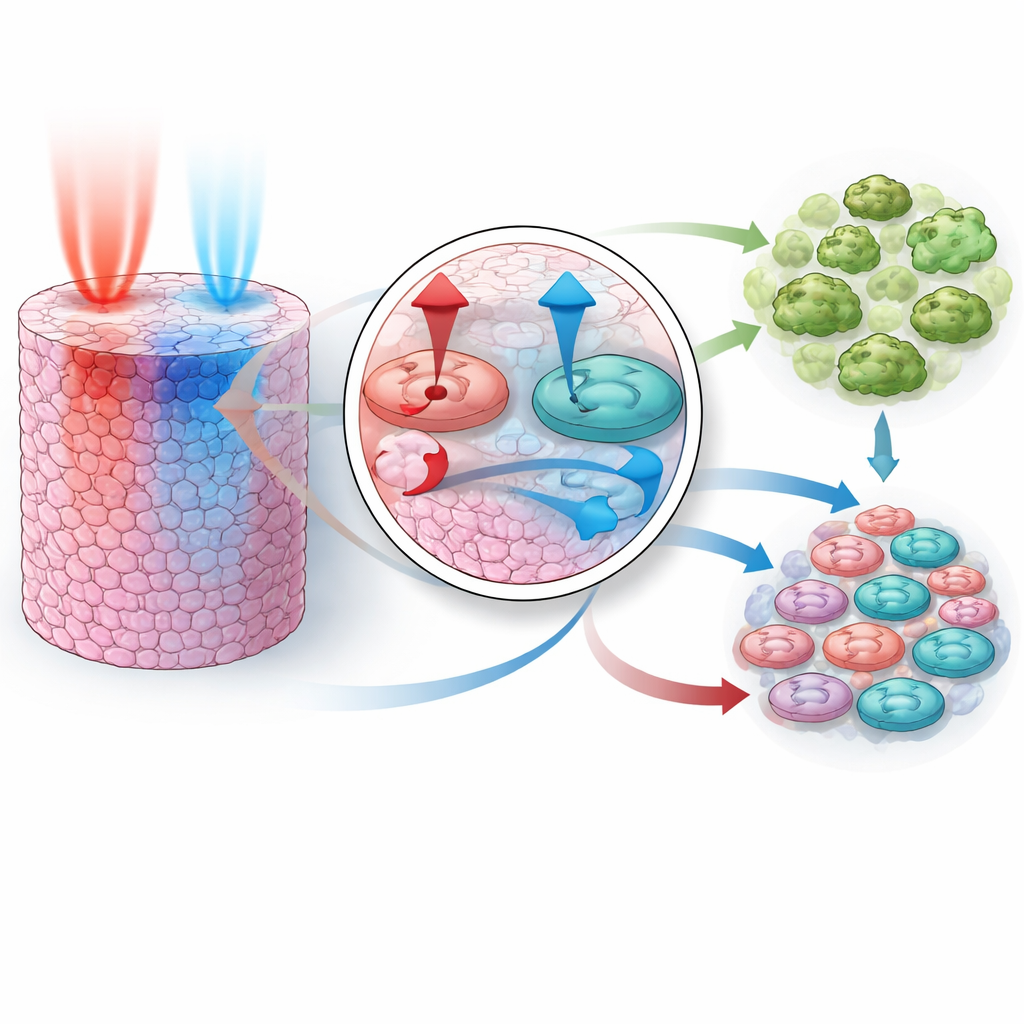
Investigando o mecanismo da sinergia
Porque o modelo acompanha eventos desde interruptores moleculares até desfechos populacionais, ele pode oferecer hipóteses sobre como a sinergia surge. Para os inibidores de PI3K e MEK, as simulações sugeriram que as células ficam globalmente “preparadas” para a morte: seu limiar para desencadear apoptose cai, e a maquinaria interna que executa a morte celular torna‑se mais ativa, especialmente por vias envolvendo a proteína Caspase‑9. Para o par AKT e MEK, o modelo apontou para uma rota diferente: sinais de sobrevivência ligados a um fator promotor de crescimento são atenuados, enquanto um fator contraposto que incentiva a morte celular ganha influência. Nesse caso, a sinergia parece depender mais fortemente de uma via alternativa de morte impulsionada pela Caspase‑8. Esses mecanismos distintos destacam como o mesmo resultado geral—eliminação mais intensa—pode ser alcançado por meio de fiações internas diferentes.
Tempo e movimentação das drogas moldam o sucesso
A equipe então estendeu o modelo para três dimensões para imitar um pequeno tumor sólido, onde as drogas entram por um lado e precisam difundir‑se para o interior através de camadas de células. Nesse cenário mais realista, exploraram o que acontece se as duas drogas são administradas juntas, ou se uma precede a outra por vários intervalos de tempo, e como mudanças na velocidade com que cada droga se move pelo tecido afetam o resultado. As simulações revelaram uma regra clara: a via controlada por PI3K e AKT deve ser desligada antes ou ao mesmo tempo que a via controlada por MEK para que a combinação seja altamente eficaz. Se MEK for bloqueado primeiro, o feedback dentro da rede permite que a atividade PI3K/AKT rebata, resgatando temporariamente a sobrevivência celular e atenuando o efeito global. Diferenças na velocidade de difusão de cada droga amplificam esse efeito, o que significa que mesmo uma dose “simultânea” no nível do paciente pode chegar em uma ordem particular às próprias células.
O que isso significa para o futuro do tratamento do câncer
Este trabalho mostra que um modelo computacional cuidadosamente calibrado, fundamentado em experimentos com drogas únicas, pode antecipar com sucesso como pares de drogas irão se comportar ao longo do tempo e sugerir por que a ordem de dosagem importa. Ao conectar a lógica molecular dentro das células ao comportamento de uma população celular inteira e ao movimento físico das drogas, a estrutura pode gerar ideias concretas e testáveis sobre quais esquemas de administração devem funcionar melhor em laboratório e, eventualmente, em pacientes. Embora os resultados atuais se apliquem especificamente a uma linhagem de câncer gástrico, a mesma abordagem poderia ser adaptada a outros cânceres, ajudando pesquisadores a projetar combinações e estratégias de temporização mais inteligentes em vez de depender apenas de testes por tentativa e erro.
Citação: Hayoun-Mya, O., Montagud, A., Valencia, A. et al. Experimentally calibrated multiscale model predicts schedule dependent drug combination effects. npj Syst Biol Appl 12, 52 (2026). https://doi.org/10.1038/s41540-026-00669-4
Palavras-chave: combinações de drogas contra câncer, modelagem multiescala, programação de drogas, câncer gástrico, oncologia computacional