Clear Sky Science · tr
Deneysel olarak kalibre edilmiş çok ölçekli model, zamanlama bağımlı ilaç kombinasyonu etkilerini öngörüyor
Neden zamanlama kanser ilaç tedavisinde önemlidir
Kanser tedavisi yalnızca doğru ilaçları seçmekle ilgili değildir; onları doğru şekilde ve doğru zamanda vermek de önemlidir. Birçok umut verici ilaç çifti basit laboratuvar kaplarında güçlü görünür, ancak ilaçların düzensiz yayıldığı ve hücrelerin karmaşık, koordine yanıtlar verdiği gerçek tümörlerde etkilerini yitirir. Bu çalışma, tek bir kanser hücresinin içinde olanlarla tüm hücre kitlesinde olanları birbirine bağlayan bir bilgisayar modeli sunar ve iki ilacın sırası ile zamanlamasının büyümeyi ılımlı şekilde yavaşlatmak ile dramatik tümör çöküşü arasında fark yaratabileceğini gösterir. 
Tek hücreleri tüm tümörlere bağlamak
Araştırmacılar insan mide (gastrik) kanseri hücre hattı AGS üzerine odaklandı ve davranışını yansıtan bir “çok ölçekli” model inşa etti. En ayrıntılı düzeyde, her sanal hücre büyüyüp büyümemeye ya da ölmeye karar veren önemli sinyal moleküllerinin basitleştirilmiş bir devre şemasını taşır. Bu iç anahtarlar aktif ya da inaktif olarak temsil edilir, ancak hâlâ dereceye bağlı yanıtları mümkün kılacak şekilde birleşir. Daha üst düzeyde, her hücre simüle edilmiş bir dokuda bağımsız bir ajan gibidir: hücreler birbirlerine baskı yapar, kalabalık olduklarını hissettiklerinde bölünmeyi durdurur ve iç sinyallerine bağlı olarak ölebilir veya büyümeyi sürdürebilir. Bunun üzerinde, ilaçlar ve besinler sanal bir ortamda difüze olur; bu, maddelerin bir tümör benzeri küme içine nasıl girdiklerini ve yayıldıklarını taklit eder.
Modeli tek ilaç verileriyle eğitmek
Sanal sistemi gerçekçi kılmak için ekip önce AGS hücrelerinin tedavi edilmediklerinde veya tek ilaçlara maruz kaldıklarında zaman içinde nasıl büyüdüklerine dair gerçek ölçümlerle modeli eğitti. Kanser tedavisi açısından ilgili üç hedefe yönelik inhibitör kullandılar: biri PI3K–yi, biri MEK–i ve biri AKT–yi engelleyen; bunların hepsi hücre hayatta kalmasını ve bölünmesini destekleyen yolaklardaki proteinlerdir. Yüksek performanslı bilgisayarlarda çalışan güçlü optimizasyon algoritmaları kullanarak hücrelerin ne kadar hızlı bölündüğünü, kalabalığa ne kadar hassas olduklarını, ilaçların hücre zarlarından ne kadar kolay geçtiğini ve iç sinyallerin büyüme veya ölüme nasıl dönüştüğünü kontrol eden parametreleri ayarladılar. Bu ayarlarla model gözlemlenen büyüme eğrilerini yakından yeniden üretti: bir ilaç esas olarak büyümeyi yavaşlattı, bir diğeri kısa bir artıştan sonra hücrelerin küçülmesine neden oldu ve üçüncüsü nüfusu zaman içinde düzenli olarak azalttı.
Görmeden sinerji tahmin etmek
Model tek ilaç davranışını taklit edebildikten sonra ana test, eğitimin hiçbir aşamasında kombinasyon verisi gösterilmeden ilaçlar birlikte verildiğinde ne olduğunu öngörebilmesiydi. Araştırmacılar tüm üç tek ilaç uyumuna tutarlı olan parametre aralıkları oluşturdu, ardından iki bilinen sinerjik çift için binlerce sanal deney çalıştırdılar: PI3K ile MEK inhibisyonu ve AKT ile MEK inhibisyonu. Dikkat çekici biçimde, simüle edilen kombinasyonlar gerçek deneylerde görülen beklenenden daha güçlü büyüme baskılanmasını yeniden üretti. Model, her çiftin farklı güçleri harmanlayarak etki ettiğini gösterdi: bir ilaç büyüme sinyallerini güçlü şekilde engelliyor, diğeri hücreleri kendi kendine yıkıma itiyordu. Birlikte, pro-hayat sinyallerini kapatıp pro-ölüm sinyallerini artırarak, her birinin tek başına yapabileceğinden çok daha büyük bir hücre fraksiyonunu öldürdüler. 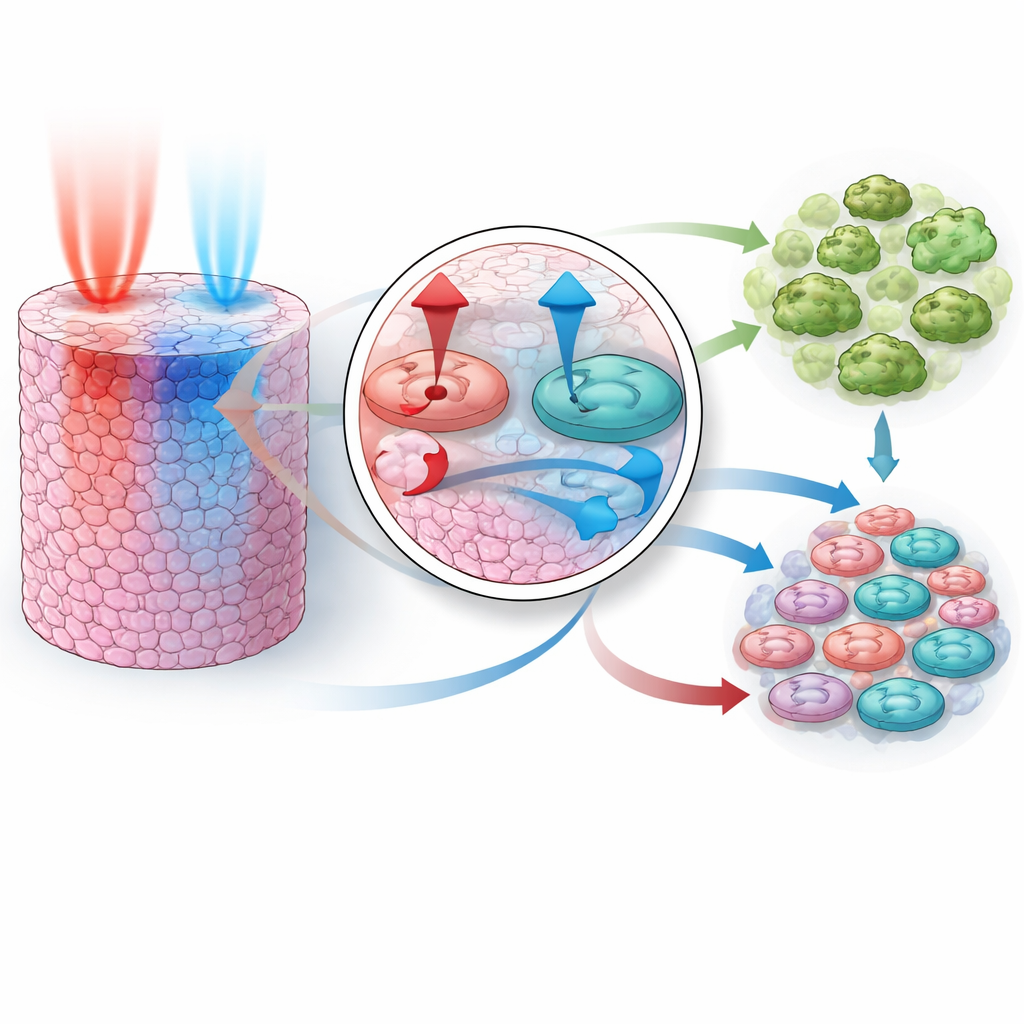
Sinerji mekanizmasının içine bakmak
Model moleküler anahtarlardan popülasyon sonuçlarına kadar olayları takip ettiğinden, sinerjinin nasıl ortaya çıktığına dair hipotezler sunabilir. PI3K ve MEK inhibitörleri için simülasyonlar hücrelerin küresel olarak ölüme “hazırlandığını” önerdi: apoptozu tetikleme eşiği düşüyor ve hücre ölümü yürütme mekanizması, özellikle Caspase-9 içeren yolaklar aracılığıyla daha aktif hale geliyor. AKT ve MEK çiftinde model farklı bir rota işaret etti: büyümeyi teşvik eden bir faktöre bağlı hayatta kalma sinyalleri zayıflatılırken, hücre ölümünü teşvik eden karşıt bir faktörün etkisi artıyor. Bu durumda sinerjinin daha çok Caspase-8 tarafından yönlendirilen alternatif bir ölüm yoluna dayanıyor gibi görünmesi dikkat çekici. Bu farklı mekanizmalar, aynı genel sonucun—daha güçlü hücre öldürme—farklı iç devrelerle nasıl sağlanabileceğini vurguluyor.
Zamanlama ve ilaç hareketi başarımı şekillendirir
Ekip daha sonra modeli küçük bir katı tümörü taklit etmek için üç boyuta genişletti; burada ilaçlar bir taraftan girer ve hücre katmanları boyunca içe doğru difüze olmak zorundadır. Bu daha gerçekçi ortamda, iki ilacın birlikte verildiğinde ne olduğu ya da birinin diğerinden farklı zamanlarda önde gelmesi durumunda neler olduğu ve her bir ilacın doku içindeki hareket hızındaki değişikliklerin sonucu nasıl etkilediği araştırıldı. Simülasyonlar net bir kural ortaya koydu: kombinasyonun yüksek derecede etkili olması için PI3K/AKT tarafından kontrol edilen yolak MEK tarafından kontrol edilen yolaktan önce veya en geç onunla aynı anda kapatılmalı. Eğer MEK önce engellenirse, ağ içindeki geri bildirimler PI3K/AKT aktivitesinin geri sıçramasına izin verir, bu da geçici olarak hücre hayatta kalmasını kurtarır ve genel etkiyi azaltır. Her bir ilacın ne kadar hızlı difüze olduğundaki farklılıklar bu etkiyi artırır; yani hasta düzeyinde bile “eşzamanlı” verilen bir doz hücrelere ulaşırken belirli bir sırada gelebilir.
Gelecekteki kanser tedavisi için ne anlama geliyor
Bu çalışma, tek ilaç deneylerine dayanan dikkatle kalibre edilmiş bir bilgisayar modelinin ilaç çiftlerinin zaman içindeki davranışlarını öngörebileceğini ve dozlama sırasının neden önemli olduğuna dair içgörüler sağlayabileceğini gösteriyor. Hücre içindeki moleküler mantığı tüm hücre popülasyonunun davranışı ve ilaçların fiziksel hareketiyle birleştirerek, çerçeve laboratuvarda ve nihayetinde hastalarda en iyi hangi zamanlama stratejilerinin işe yarayacağına dair somut, test edilebilir fikirler üretebilir. Mevcut sonuçlar özel olarak bir mide kanseri hücre hattına uygulanabilir olsa da, aynı yaklaşım diğer kanserlere uyarlanarak araştırmacıların daha akıllı kombinasyonlar ve zamanlama stratejileri tasarlamasına yardımcı olabilir; sadece deneme-yanılmaya dayanmak yerine.
Atıf: Hayoun-Mya, O., Montagud, A., Valencia, A. et al. Experimentally calibrated multiscale model predicts schedule dependent drug combination effects. npj Syst Biol Appl 12, 52 (2026). https://doi.org/10.1038/s41540-026-00669-4
Anahtar kelimeler: kanser ilaç kombinasyonları, çok ölçekli modelleme, ilaç zamanlaması, mide kanseri, hesaplamalı onkoloji