Clear Sky Science · it
Modello multiscala calibrato sperimentalmente predice gli effetti delle combinazioni di farmaci dipendenti dal calendario
Perché il tempismo conta nel trattamento del cancro
La terapia del cancro non riguarda solo la scelta dei farmaci giusti; riguarda anche il modo e il momento in cui somministrarli. Molte coppie di farmaci promettenti sembrano potenti in semplici colture di laboratorio ma perdono efficacia nei tumori reali, dove i farmaci si distribuiscono in modo non uniforme e le cellule rispondono in modo complesso e coordinato. Questo studio presenta un modello informatico che collega ciò che avviene all’interno di singole cellule tumorali a quanto accade in una massa cellulare, e mostra come l’ordine e il timing di due farmaci possano fare la differenza tra un modesto rallentamento della crescita e un collasso tumorale drammatico. 
Collegare le singole cellule ai tumori interi
I ricercatori si sono concentrati su una linea cellulare umana di cancro gastrico chiamata AGS e hanno costruito un modello “multiscala” che ne rispecchia il comportamento. Al livello più dettagliato, ogni cellula virtuale contiene uno schema semplificato delle vie di segnalazione chiave che decidono se la cellula cresce o muore. Questi interruttori interni sono rappresentati come attivi o inattivi, ma combinati in modo da permettere comunque risposte graduali. A un livello superiore, ogni cellula è un agente indipendente in un tessuto simulato: le cellule si spingono a vicenda, smettono di dividersi quando percepiscono affollamento e possono morire o continuare a crescere in base ai loro segnali interni. Al di sopra di tutto, farmaci e nutrienti diffondono in un ambiente virtuale, imitando come le sostanze si muovono dentro e attraverso un aggregato simile a un tumore.
Addestrare il modello con dati su singoli farmaci
Per rendere il sistema virtuale realistico, il team lo ha prima addestrato su misure reali di come le cellule AGS crescono nel tempo quando sono non trattate o esposte a singoli farmaci. Hanno usato tre inibitori mirati rilevanti per il trattamento del cancro: uno che blocca PI3K, uno che blocca MEK e uno che blocca AKT, tutte proteine in vie che promuovono la sopravvivenza e la divisione cellulare. Utilizzando potenti algoritmi di ottimizzazione eseguiti su computer ad alte prestazioni, hanno regolato i parametri che controllano la velocità di divisione cellulare, la sensibilità all’affollamento, la facilità con cui i farmaci attraversano le membrane cellulari e il modo in cui i segnali interni si traducono in crescita o morte. Con queste impostazioni il modello ha riprodotto da vicino le curve di crescita osservate: un farmaco rallentava principalmente la crescita, un altro causava la riduzione delle cellule dopo un breve picco, e un terzo riduceva costantemente la popolazione nel tempo.
Prevedere la sinergia senza vederla
Una volta che il modello ha potuto mimare il comportamento dei singoli farmaci, la prova cruciale era se potesse prevedere cosa succede quando i farmaci sono combinati, senza aver visto dati di combinazione durante l’addestramento. I ricercatori hanno costruito intervalli di parametri coerenti con i tre adattamenti ai singoli farmaci, poi hanno eseguito migliaia di esperimenti virtuali per due coppie note per essere sinergiche: l’inibizione di PI3K più MEK e l’inibizione di AKT più MEK. Notevolmente, le combinazioni simulate hanno riprodotto la soppressione della crescita più forte del previsto osservata negli esperimenti reali. Il modello ha mostrato che ogni coppia agisce combinando forze diverse: un farmaco blocca fortemente i segnali di crescita, l’altro spinge le cellule verso l’autodistruzione. Insieme spengono i segnali pro-sopravvivenza e potenziano i segnali pro-morte, portando una frazione molto più ampia di cellule alla morte rispetto a quanto potrebbe ciascuno da solo. 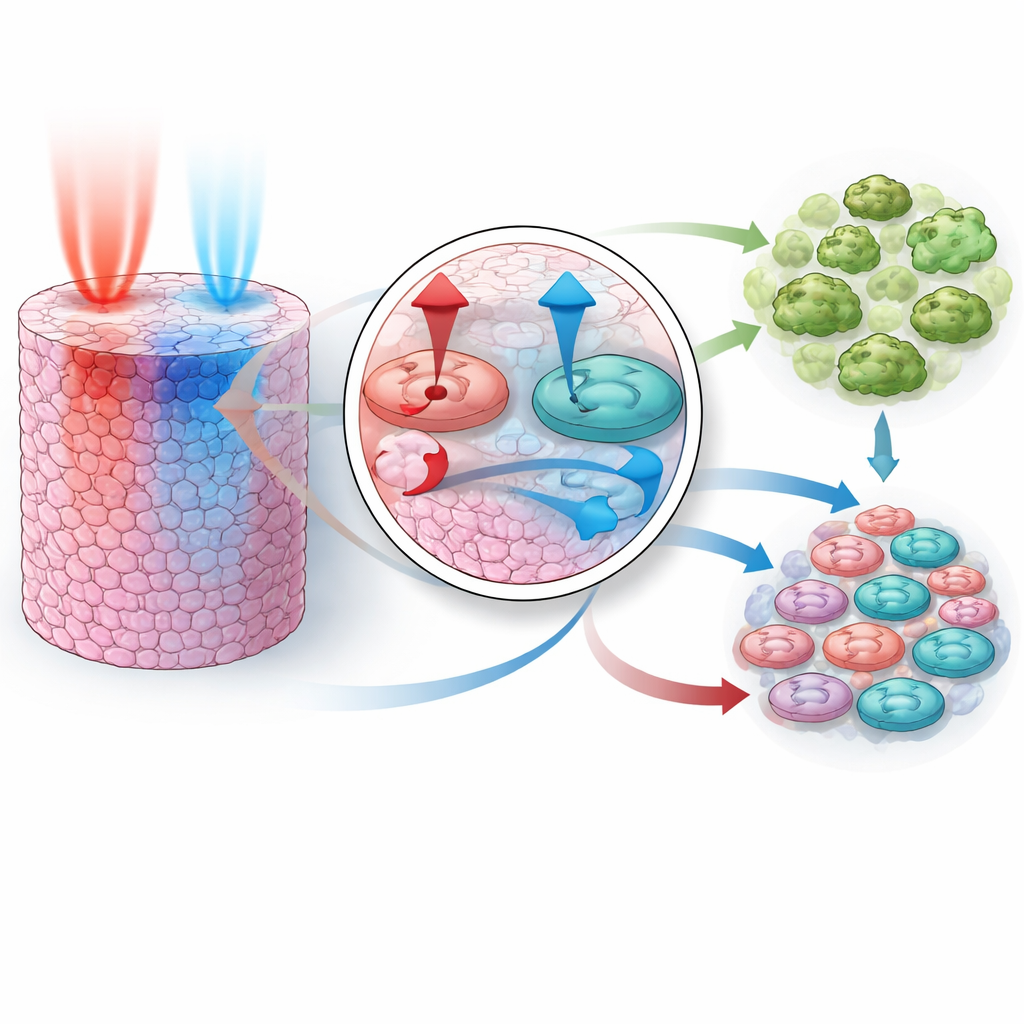
Schermare il meccanismo della sinergia
Poiché il modello traccia gli eventi dagli interruttori molecolari agli esiti di popolazione, può offrire ipotesi su come nasce la sinergia. Per gli inibitori di PI3K e MEK, le simulazioni suggerivano che le cellule diventano globalmente “preparate” alla morte: la soglia per innescare l’apoptosi si abbassa e il meccanismo interno che esegue la morte cellulare diventa più attivo, in particolare attraverso vie che implicano la proteina Caspasi-9. Per la coppia AKT e MEK, il modello indicava una strada diversa: i segnali di sopravvivenza legati a un fattore promotore della crescita vengono attenuati, mentre un fattore controbilanciante che favorisce la morte cellulare guadagna influenza. In questo caso, la sinergia sembra dipendere più pesantemente da una via alternativa di morte guidata da Caspasi-8. Questi meccanismi distinti evidenziano come lo stesso risultato complessivo—una maggiore uccisione—possa essere ottenuto attraverso cablaggi interni differenti.
Il timing e il movimento dei farmaci determinano il successo
Il team ha poi esteso il modello a tre dimensioni per imitare un piccolo tumore solido, dove i farmaci entrano da un lato e devono diffondere verso l’interno attraverso strati di cellule. In questo contesto più realistico hanno esplorato cosa succede se i due farmaci sono somministrati insieme, o se uno precede l’altro di diversi intervalli temporali, e come le variazioni nella velocità con cui ciascun farmaco si muove nel tessuto influenzano l’esito. Le simulazioni hanno rivelato una regola chiara: la via controllata da PI3K e AKT deve essere spenta prima o contemporaneamente alla via controllata da MEK affinché la combinazione sia altamente efficace. Se MEK viene bloccato per primo, il feedback all’interno della rete permette all’attività PI3K/AKT di rimbalzare, salvando temporaneamente la sopravvivenza cellulare e attenuando l’effetto complessivo. Le differenze nella velocità di diffusione di ciascun farmaco amplificano questo effetto, il che significa che anche una somministrazione “simultanea” a livello del paziente può arrivare in un ordine particolare alle singole cellule.
Cosa significa per i trattamenti futuri contro il cancro
Questo lavoro mostra che un modello computazionale accuratamente calibrato, fondato su esperimenti con singoli farmaci, può prevedere con successo come le coppie di farmaci si comporteranno nel tempo e suggerire perché l’ordine di dosaggio sia importante. Collegando la logica molecolare all’interno delle cellule al comportamento di un’intera popolazione cellulare e al movimento fisico dei farmaci, il quadro può generare idee concrete e verificabili su quali schemi temporali dovrebbero funzionare meglio in laboratorio e, in prospettiva, nei pazienti. Pur essendo i risultati attuali specifici per una linea cellulare di cancro gastrico, lo stesso approccio potrebbe essere adattato ad altri tumori, aiutando i ricercatori a progettare combinazioni e strategie di tempistica più intelligenti invece di affidarsi esclusivamente a tentativi ed errori.
Citazione: Hayoun-Mya, O., Montagud, A., Valencia, A. et al. Experimentally calibrated multiscale model predicts schedule dependent drug combination effects. npj Syst Biol Appl 12, 52 (2026). https://doi.org/10.1038/s41540-026-00669-4
Parole chiave: combinazioni di farmaci per il cancro, modellizzazione multiscala, programmazione dei farmaci, cancro gastrico, oncologia computazionale