Clear Sky Science · nl
Experimenteel gekalibreerd multischalige model voorspelt schema-afhankelijke effecten van medicijncombinaties
Waarom timing ertoe doet bij kankerbehandeling
Kankertherapie gaat niet alleen over het kiezen van de juiste middelen; het gaat ook om ze op de juiste manier en op het juiste moment toe te dienen. Veel veelbelovende geneesmiddelpaaren lijken krachtig in eenvoudige laboratoriumschalen, maar verliezen hun effect in echte tumoren, waar medicijnen ongelijk verspreiden en cellen complex en gecoördineerd reageren. Deze studie introduceert een computermodel dat verbindt wat er binnen individuele kankercellen gebeurt met wat er in een hele celmassa plaatsvindt, en toont aan hoe de volgorde en timing van twee geneesmiddelen het verschil kunnen maken tussen bescheiden groeivertraging en dramatisch tumorneergang. 
Het koppelen van individuele cellen aan hele tumoren
De onderzoekers richtten zich op een menselijke maagkankercellijn genaamd AGS en bouwden een "multischaal" model dat het gedrag nabootst. Op het meest gedetailleerde niveau draagt elke virtuele cel een vereenvoudigd bedradingsdiagram van sleutel-signaalmoleculen die bepalen of de cel groeit of sterft. Deze interne schakelaars worden voorgesteld als actief of inactief, maar worden gecombineerd op een manier die toch genuanceerde responsen toestaat. Op een hoger niveau is elke cel een onafhankelijke agent in een gesimuleerd weefsel: cellen duwen tegen elkaar, stoppen met delen wanneer ze zich druk voelen, en kunnen sterven of doorgroeien afhankelijk van hun interne signalen. Daarboven diffunderen medicijnen en voedingsstoffen door een virtuele omgeving, die nabootst hoe stoffen in en door een tumorachtige klomp bewegen.
Het model trainen met gegevens van één geneesmiddel
Om het virtuele systeem realistisch te maken, trainde het team het eerst op echte metingen van hoe AGS-cellen in de tijd groeien wanneer ze onbehandeld zijn of worden blootgesteld aan afzonderlijke geneesmiddelen. Ze gebruikten drie gerichte remmers die relevant zijn voor kankerbehandeling: één die PI3K blokkeert, één die MEK blokkeert en één die AKT blokkeert, allemaal eiwitten in paden die celoverleving en deling bevorderen. Met krachtige optimalisatie-algoritmen op high-performance computers pasten ze parameters aan die bepalen hoe snel cellen delen, hoe gevoelig ze zijn voor dichtheidsremming, hoe gemakkelijk geneesmiddelen celmembranen passeren en hoe interne signalen worden omgezet in groei of dood. Met deze instellingen reproduceerde het model nauwkeurig de waargenomen groeicurven: het ene middel vertraagde vooral de groei, een ander liet cellen na een korte opleving weer krimpen, en een derde verminderde gestaag de populatie in de loop van de tijd.
Synergie voorspellen zonder die gezien te hebben
Zodra het model het gedrag van enkele geneesmiddelen kon nabootsen, was de cruciale test of het kon voorspellen wat er gebeurt wanneer geneesmiddelen worden gecombineerd, zonder dat er combinatiedata tijdens de training werden getoond. De onderzoekers construeerden parameterbereiken die consistent waren met alle drie de enkelmiddel-fits en draaiden vervolgens duizenden virtuele experimenten voor twee bekende synergistische paren: PI3K plus MEK-remming en AKT plus MEK-remming. Opvallend genoeg reproduceerden de gesimuleerde combinaties de sterker-dan-verwachte groeiremming die in echte experimenten werd gezien. Het model toonde dat elk paar werkt door verschillende krachten te combineren: het ene middel blokkeert sterk groeisignalen, het andere duwt cellen richting zelfvernietiging. Samen schakelen ze zowel pro-overlevingssignalen uit als versterken ze pro-doodsignalen, waardoor een veel groter deel van de cellen sterft dan elk middel afzonderlijk zou doen. 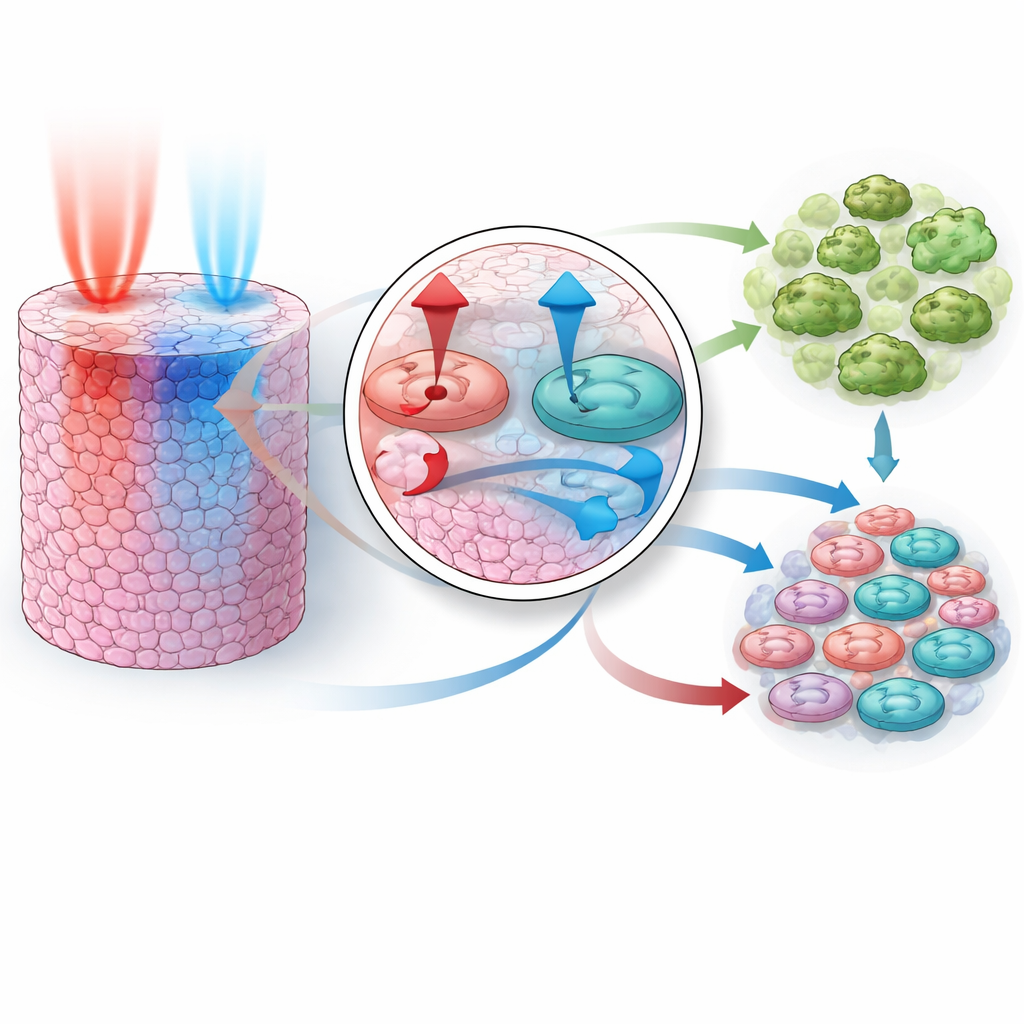
Een kijkje in het mechanisme achter synergie
Aangezien het model gebeurtenissen volgt van moleculaire schakelaars tot populatieresultaten, kan het hypothesen bieden over hoe de synergie ontstaat. Voor PI3K- en MEK-remmers suggereerden de simulaties dat cellen globaal "geprimed" raken voor celdood: hun drempel om apoptose te activeren daalt en het interne apparaat dat celdood uitvoert wordt actiever, vooral via paden waarin het eiwit Caspase-9 een rol speelt. Voor het AKT- en MEK-paar wees het model op een andere route: overlevingssignalen gekoppeld aan een groeibevorderende factor worden gedempt, terwijl een tegengestelde factor die celdood aanmoedigt aan invloed wint. In dit geval lijkt de synergie zwaarder te leunen op een alternatieve doodspad aangedreven door Caspase-8. Deze verschillende mechanismen benadrukken hoe hetzelfde eindresultaat—sterkere doding—via verschillende interne bedrading kan worden bereikt.
Timing en beweging van geneesmiddelen vormen het succes
Het team breidde het model vervolgens uit naar drie dimensies om een kleine solide tumor na te bootsen, waarin geneesmiddelen vanaf één zijde binnenkomen en naar binnen moeten diffunderen door lagen cellen. In deze meer realistische setting onderzochten ze wat er gebeurt als de twee geneesmiddelen gelijktijdig worden gegeven, of als de ene de andere met verschillende tijdsverschillen voorafgaat, en hoe veranderingen in de diffu-snelheid van elk geneesmiddel door weefsel het resultaat beïnvloeden. De simulaties onthulden een duidelijke regel: het pad gecontroleerd door PI3K en AKT moet worden uitgeschakeld vóór of gelijktijdig met het pad gecontroleerd door MEK om de combinatie erg effectief te laten zijn. Als MEK eerst wordt geblokkeerd, laat feedback binnen het netwerk PI3K/AKT-activiteit terugveren, wat de celoverleving tijdelijk redt en het totale effect dempt. Verschillen in hoe snel elk middel diffuseert versterken dit effect, wat betekent dat zelfs een "gelijktijdige" dosis op patiëntniveau in werkelijkheid in een bepaalde volgorde bij de cellen kan aankomen.
Wat dit betekent voor toekomstige kankerbehandeling
Dit werk toont aan dat een zorgvuldig gekalibreerd computermodel, gebaseerd op enkelmiddel-experimenten, succesvol kan voorspellen hoe geneesmiddelpaaren zich in de tijd zullen gedragen en kan suggereren waarom de toedieningsvolgorde van belang is. Door moleculaire logica binnen cellen te koppelen aan het gedrag van een gehele celpopulatie en aan de fysieke beweging van geneesmiddelen, kan het raamwerk concrete, toetsbare ideeën genereren over welke schema's het beste in het laboratorium en uiteindelijk bij patiënten zouden moeten werken. Hoewel de huidige resultaten specifiek gelden voor één maagkankercellijn, kan dezelfde aanpak worden aangepast aan andere kankersoorten en onderzoekers helpen slimmere combinaties en timingstrategieën te ontwerpen in plaats van uitsluitend op trial-and-error te vertrouwen.
Bronvermelding: Hayoun-Mya, O., Montagud, A., Valencia, A. et al. Experimentally calibrated multiscale model predicts schedule dependent drug combination effects. npj Syst Biol Appl 12, 52 (2026). https://doi.org/10.1038/s41540-026-00669-4
Trefwoorden: combinaties van kankermedicijnen, multischaalmodellering, medicijnschema's, maagkanker, computationele oncologie