Clear Sky Science · de
Experimentell kalibriertes multiskaliges Modell sagt zeitplanabhängige Wirkungen von Medikamentenkombinationen voraus
Warum das Timing bei Krebsbehandlung wichtig ist
Krebstherapie besteht nicht nur darin, die richtigen Medikamente auszuwählen; es geht auch darum, sie auf die richtige Weise und im richtigen Zeitpunkt zu verabreichen. Viele vielversprechende Wirkstoffpaare erscheinen in einfachen Laborversuchen wirkungsvoll, verlieren aber ihre Kraft in realen Tumoren, in denen sich Medikamente ungleichmäßig verteilen und Zellen komplex und koordiniert reagieren. Diese Studie stellt ein Computermodell vor, das verbindet, was in einzelnen Krebszellen passiert, mit dem, was in einem ganzen Zellverband geschieht, und zeigt, wie Reihenfolge und Timing von zwei Medikamenten den Unterschied zwischen mäßiger Wachstumshemmung und dramatischem Tumorzusammenbruch ausmachen können. 
Verknüpfung einzelner Zellen mit ganzen Tumoren
Die Forschenden konzentrierten sich auf eine humane Magenkrebs-Zelllinie namens AGS und bauten ein „multiskaliges“ Modell, das ihr Verhalten nachbildet. Auf der detailliertesten Ebene trägt jede virtuelle Zelle ein vereinfachtes Schaltbild zentraler Signalmoleküle, die entscheiden, ob die Zelle wächst oder abstirbt. Diese internen Schalter werden als aktiv oder inaktiv dargestellt, sind aber so kombiniert, dass dennoch abgestufte Reaktionen möglich sind. Auf einer höheren Ebene ist jede Zelle ein unabhängiger Agent in einem simulierten Gewebe: Zellen üben Druck aufeinander aus, stoppen die Teilung, wenn sie sich beengt fühlen, und können je nach internen Signalen sterben oder weiter wachsen. Darüber hinaus diffundieren Medikamente und Nährstoffe durch eine virtuelle Umgebung, was nachahmt, wie Substanzen in und durch einen tumorähnlichen Zellverband gelangen.
Das Modell mit Einzelsubstanzdaten anlernen
Um das virtuelle System realistisch zu machen, trainierte das Team es zunächst anhand realer Messungen, wie AGS-Zellen über die Zeit wachsen, wenn sie unbehandelt bleiben oder einzelnen Wirkstoffen ausgesetzt sind. Sie verwendeten drei zielgerichtete Inhibitoren, die für die Krebstherapie relevant sind: einen, der PI3K blockiert, einen, der MEK blockiert, und einen, der AKT blockiert — alles Proteine in Signalwegen, die Zellüberleben und Teilung fördern. Mit leistungsstarken Optimierungsalgorithmen auf Hochleistungsrechnern stimmten sie Parameter ab, die steuern, wie schnell Zellen sich teilen, wie empfindlich sie auf Dichte reagieren, wie leicht Medikamente Zellmembranen passieren und wie interne Signale in Wachstum oder Tod umgesetzt werden. Mit diesen Einstellungen reproduzierte das Modell eng die beobachteten Wachstumskurven: Ein Medikament verlangsamte hauptsächlich das Wachstum, ein anderes ließ die Zellen nach einem kurzen Anstieg wieder zurückgehen, und ein drittes reduzierte die Population im Zeitverlauf stetig.
Synergie vorhersagen, ohne sie gesehen zu haben
Sobald das Modell das Verhalten einzelner Wirkstoffe nachahmen konnte, bestand die eigentliche Prüfung darin, ob es vorhersagen kann, was passiert, wenn Medikamente kombiniert werden, ohne während des Trainings irgendwelche Kombinationsdaten zu sehen. Die Forschenden stellten Parameterbereiche zusammen, die mit allen drei Einzelsubstanzanpassungen konsistent waren, und führten dann Tausende virtueller Experimente für zwei bekannte synergistische Paare durch: PI3K- plus MEK-Hemmung und AKT- plus MEK-Hemmung. Bemerkenswerterweise reproduzierten die simulierten Kombinationen die stärker als erwartete Wachstumshemmung, wie sie in realen Experimenten beobachtet wurde. Das Modell zeigte, dass jedes Paar durch das Zusammenwirken unterschiedlicher Stärken wirkt: Ein Wirkstoff blockiert stark Wachstumssignale, der andere treibt Zellen in Richtung Selbstzerstörung. Zusammen schalten sie sowohl pro‑Überlebenssignale ab als auch pro‑Todes‑Signale hoch, sodass ein viel größerer Anteil der Zellen stirbt als durch einen Wirkstoff allein. 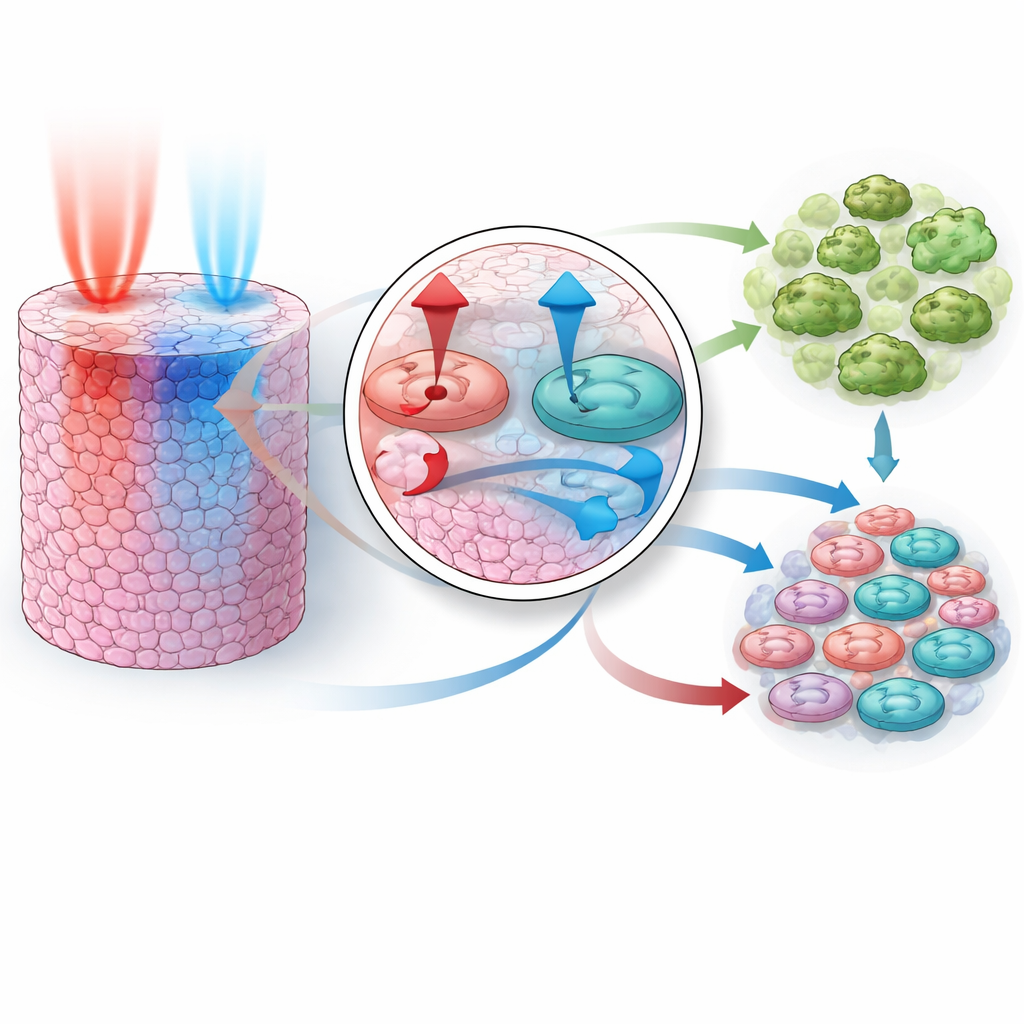
Einen Blick in den Mechanismus der Synergie werfen
Weil das Modell Ereignisse von molekularen Schaltern bis zu Populationsauswirkungen verfolgt, kann es Hypothesen darüber liefern, wie die Synergie entsteht. Für PI3K‑ und MEK‑Inhibitoren deuteten die Simulationen darauf hin, dass die Zellen global für den Tod „vorgespannte“ Zustände erreichen: Die Schwelle, die die Apoptose auslöst, sinkt, und die interne Maschinerie, die den Zelltod ausführt, wird aktiver, insbesondere über Wege, an denen das Protein Caspase‑9 beteiligt ist. Beim AKT‑ und MEK‑Paar zeigte das Modell auf einen anderen Weg: Überlebenssignale, die mit einem wachstumsfördernden Faktor verknüpft sind, werden gedämpft, während ein gegensteuernder Faktor, der den Zelltod fördert, an Einfluss gewinnt. In diesem Fall scheint die Synergie stärker von einem alternativen Todesweg abhängig zu sein, der durch Caspase‑8 getrieben wird. Diese unterschiedlichen Mechanismen verdeutlichen, wie dasselbe Gesamtergebnis — stärkere Abtötung — durch unterschiedliche interne Verdrahtungen erreicht werden kann.
Timing und Wirkstoffbewegung formen den Erfolg
Das Team erweiterte das Modell dann in drei Dimensionen, um einen kleinen soliden Tumor zu simulieren, in dem Medikamente von einer Seite eintreten und durch Zellschichten nach innen diffundieren müssen. In diesem realistischeren Setting untersuchten sie, was passiert, wenn die beiden Medikamente gleichzeitig verabreicht werden, oder wenn eines dem anderen um verschiedene Zeitabstände vorausgeht, und wie Änderungen der Diffusionsgeschwindigkeit jedes Wirkstoffs durch das Gewebe das Ergebnis beeinflussen. Die Simulationen enthüllten eine klare Regel: Der durch PI3K und AKT gesteuerte Weg muss vor oder gleichzeitig mit dem durch MEK gesteuerten Weg abgeschaltet werden, damit die Kombination hochwirksam ist. Wird MEK zuerst blockiert, erlaubt Feedback innerhalb des Netzwerks der PI3K/AKT‑Aktivität ein Wiederaufleben, das vorübergehend das Überleben der Zellen rettet und die Gesamtwirkung abschwächt. Unterschiede in der Diffusionsgeschwindigkeit der einzelnen Wirkstoffe verstärken diesen Effekt, was bedeutet, dass selbst eine auf Patientenebene „gleichzeitige“ Gabe auf der Ebene der einzelnen Zellen in einer bestimmten Reihenfolge ankommen kann.
Was das für die zukünftige Krebsbehandlung bedeutet
Diese Arbeit zeigt, dass ein sorgfältig kalibriertes Computermodell, das auf Einzelsubstanzexperimenten basiert, erfolgreich vorhersagen kann, wie Wirkstoffpaare sich über die Zeit verhalten, und erklären kann, warum die Reihenfolge der Gabe wichtig ist. Indem es molekulare Logik innerhalb der Zellen mit dem Verhalten einer gesamten Zellpopulation und der physikalischen Bewegung von Medikamenten verbindet, kann das Framework konkrete, testbare Ideen darüber generieren, welche Behandlungspläne im Labor und schließlich beim Menschen am besten funktionieren sollten. Zwar gelten die aktuellen Ergebnisse speziell für eine Magenkrebs-Zelllinie, doch der gleiche Ansatz könnte an andere Krebsarten angepasst werden und Forschenden helfen, intelligentere Kombinationen und Zeitpläne zu entwerfen, statt sich ausschließlich auf Versuch‑und‑Irrtum zu verlassen.
Zitation: Hayoun-Mya, O., Montagud, A., Valencia, A. et al. Experimentally calibrated multiscale model predicts schedule dependent drug combination effects. npj Syst Biol Appl 12, 52 (2026). https://doi.org/10.1038/s41540-026-00669-4
Schlüsselwörter: Kombinationen von Krebsmedikamenten, Multiskalenmodellierung, Medikamenten-Timing, Magenkrebs, Computationale Onkologie