Clear Sky Science · es
Modelo multiescala calibrado experimentalmente predice efectos de combinaciones de fármacos dependientes del calendario
Por qué el momento importa en el tratamiento del cáncer
La terapia contra el cáncer no consiste solo en elegir los fármacos adecuados; también implica administrarlos de la manera correcta y en el momento oportuno. Muchas parejas de fármacos prometedoras parecen eficaces en simples placas de laboratorio, pero pierden potencia en tumores reales, donde los medicamentos se distribuyen de manera desigual y las células responden de forma compleja y coordinada. Este estudio presenta un modelo por ordenador que conecta lo que ocurre dentro de células cancerosas individuales con lo que sucede en una masa entera de células, y muestra cómo el orden y la sincronización de dos fármacos pueden marcar la diferencia entre una moderada ralentización del crecimiento y un colapso tumoral espectacular. 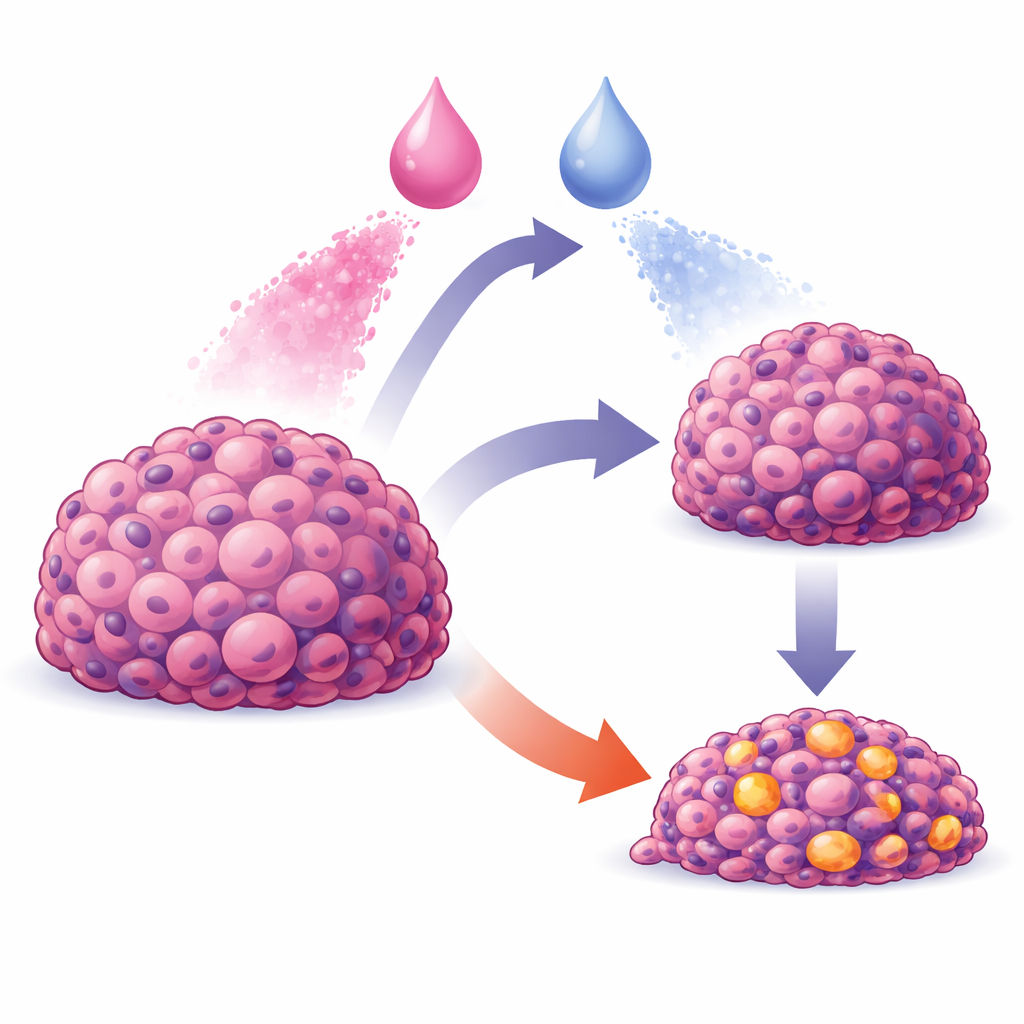
Vinculando células individuales con tumores completos
Los investigadores se centraron en una línea celular humana de cáncer gástrico (estómago) llamada AGS y construyeron un modelo “multiescala” que refleja su comportamiento. En el nivel más detallado, cada célula virtual lleva un diagrama de cableado simplificado de moléculas de señalización clave que deciden si la célula crece o muere. Estos interruptores internos se representan como activos o inactivos, pero combinados de manera que aún permiten respuestas graduadas. A un nivel superior, cada célula es un agente independiente en un tejido simulado: las células se empujan entre sí, dejan de dividirse cuando notan hacinamiento y pueden morir o seguir creciendo según sus señales internas. Por encima de eso, los fármacos y los nutrientes difunden a través de un entorno virtual, imitando cómo se mueven las sustancias dentro y a través de un conglomerado similar a un tumor.
Enseñando el modelo con datos de fármacos individuales
Para hacer realista el sistema virtual, el equipo primero lo entrenó con mediciones reales de cómo crecen las células AGS a lo largo del tiempo cuando están sin tratar o expuestas a fármacos individuales. Usaron tres inhibidores dirigidos relevantes para el tratamiento del cáncer: uno que bloquea PI3K, otro que bloquea MEK y otro que bloquea AKT, todas proteínas en vías que promueven la supervivencia y la división celular. Utilizando potentes algoritmos de optimización ejecutados en ordenadores de alto rendimiento, ajustaron parámetros que controlan la velocidad de división celular, la sensibilidad al hacinamiento, la facilidad con que los fármacos atraviesan las membranas celulares y cómo las señales internas se convierten en crecimiento o muerte. Con estos ajustes, el modelo reprodujo de manera fiel las curvas de crecimiento observadas: un fármaco ralentizaba principalmente el crecimiento, otro causaba que las células se redujeran tras un breve aumento, y un tercero disminuía de forma sostenida la población con el tiempo.
Prediciendo sinergia sin haberla visto
Una vez que el modelo pudo imitar el comportamiento ante fármacos individuales, la prueba clave fue si podía predecir lo que ocurre cuando se combinan fármacos, sin haber visto datos de combinaciones durante el entrenamiento. Los investigadores construyeron rangos de parámetros coherentes con los tres ajustes individuales y luego realizaron miles de experimentos virtuales para dos pares conocidos por su sinergia: inhibición de PI3K más MEK y de AKT más MEK. Sorprendentemente, las combinaciones simuladas reprodujeron la supresión del crecimiento más fuerte de lo esperado observada en experimentos reales. El modelo mostró que cada par actúa combinando diferentes fuerzas: un fármaco bloquea con fuerza las señales de crecimiento y el otro empuja a las células hacia la autodestrucción. Juntos, ambos apagan las señales pro‑supervivencia y aumentan las señales pro‑muerte, llevando a una fracción mucho mayor de células a morir que cualquiera de los dos por separado. 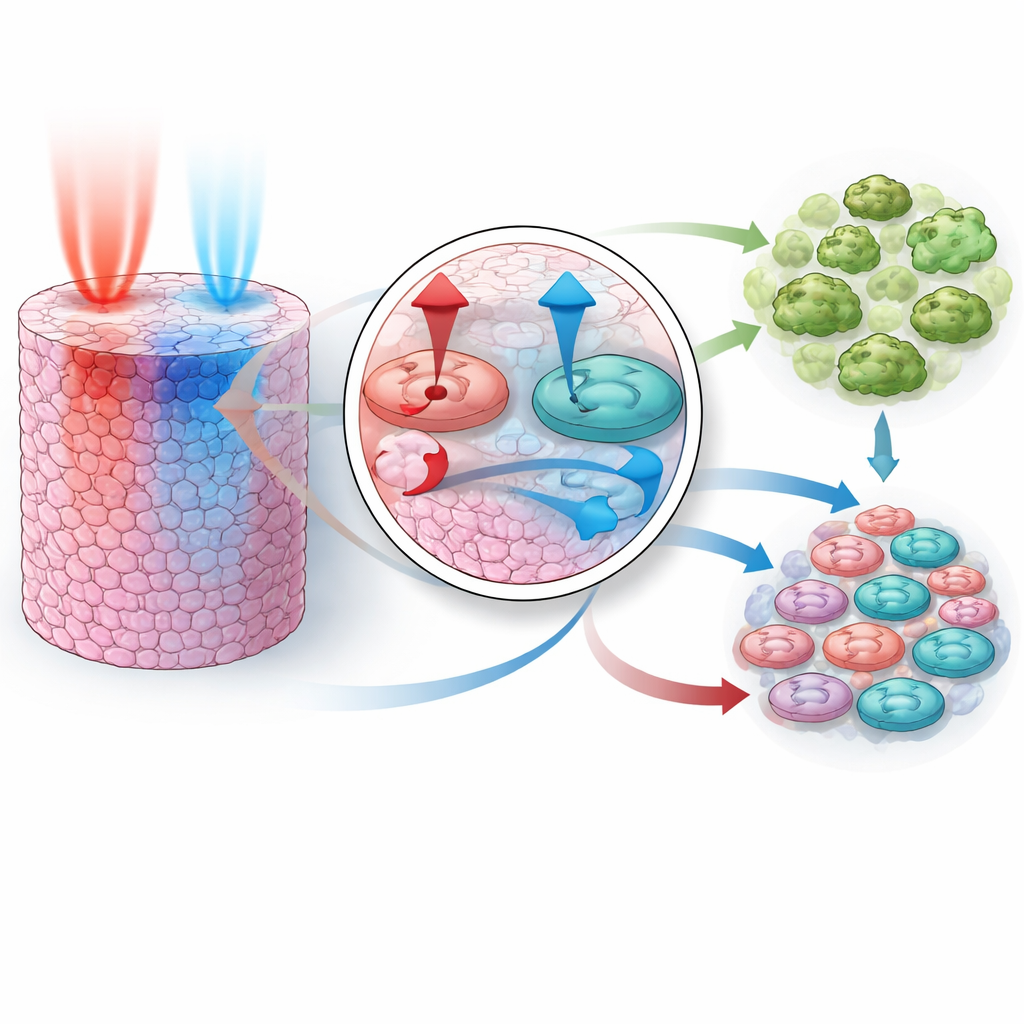
Escudriñando el mecanismo de la sinergia
Dado que el modelo rastrea eventos desde los interruptores moleculares hasta los resultados poblacionales, puede ofrecer hipótesis sobre cómo surge la sinergia. Para los inhibidores de PI3K y MEK, las simulaciones sugirieron que las células se vuelven globalmente “preparadas” para la muerte: su umbral para desencadenar apoptosis disminuye y la maquinaria interna que ejecuta la muerte celular se vuelve más activa, especialmente a través de vías que implican la proteína Caspasa‑9. Para el par AKT y MEK, el modelo apuntó a una ruta diferente: las señales de supervivencia vinculadas a un factor promotor del crecimiento se atenúan, mientras que un factor contrapuesto que fomenta la muerte celular gana influencia. En este caso, la sinergia parece depender más de una vía alternativa de muerte impulsada por Caspasa‑8. Estos mecanismos distintos subrayan cómo el mismo resultado global —una mayor eficacia citotóxica— puede alcanzarse mediante cableados internos diferentes.
El tiempo y el movimiento de los fármacos condicionan el éxito
El equipo amplió entonces el modelo a tres dimensiones para imitar un pequeño tumor sólido, donde los fármacos entran por un lado y deben difundirse hacia el interior a través de capas de células. En este entorno más realista, exploraron qué ocurre si los dos fármacos se administran juntos o si uno precede al otro por distintos intervalos de tiempo, y cómo los cambios en la velocidad de difusión de cada fármaco a través del tejido afectan el resultado. Las simulaciones revelaron una regla clara: la vía controlada por PI3K y AKT debe ser silenciada antes o al mismo tiempo que la vía controlada por MEK para que la combinación sea altamente eficaz. Si MEK se bloquea primero, la retroalimentación dentro de la red permite que la actividad de PI3K/AKT rebote, rescatando temporalmente la supervivencia celular y atenuando el efecto global. Las diferencias en la rapidez con que cada fármaco difunde amplifican este efecto, lo que significa que incluso una dosis “simultánea” a nivel del paciente puede llegar a las células en un orden particular.
Qué significa esto para el tratamiento futuro del cáncer
Este trabajo demuestra que un modelo informático cuidadosamente calibrado, basado en experimentos con fármacos individuales, puede anticipar con éxito cómo se comportarán las parejas de fármacos a lo largo del tiempo y sugerir por qué el orden de dosificación importa. Al conectar la lógica molecular dentro de las células con el comportamiento de toda una población celular y con el movimiento físico de los fármacos, el marco puede generar ideas concretas y comprobables sobre qué calendarios deberían funcionar mejor en el laboratorio y, eventualmente, en pacientes. Aunque los resultados actuales se aplican específicamente a una línea celular gástrica, el mismo enfoque podría adaptarse a otros cánceres, ayudando a los investigadores a diseñar combinaciones y estrategias de dosificación más inteligentes en lugar de depender únicamente de ensayo y error.
Cita: Hayoun-Mya, O., Montagud, A., Valencia, A. et al. Experimentally calibrated multiscale model predicts schedule dependent drug combination effects. npj Syst Biol Appl 12, 52 (2026). https://doi.org/10.1038/s41540-026-00669-4
Palabras clave: combinaciones de fármacos contra el cáncer, modelado multiescala, programación de fármacos, cáncer gástrico, oncología computacional