Clear Sky Science · ja
実験で較正した多階層モデルがスケジュール依存の薬剤併用効果を予測する
がん治療でタイミングが重要な理由
がん治療は適切な薬を選ぶだけではなく、投与方法やタイミングが重要です。単純な培養皿では有望に見える薬の組み合わせが、腫瘍内で薬が不均一に広がり、細胞が複雑かつ協調的に応答する実際の環境では効果を失うことがよくあります。本研究は、単一細胞内部で起きることを細胞集団全体の振る舞いと結びつけるコンピュータモデルを提示し、2剤の順序とタイミングが成長の緩やかな抑制と劇的な腫瘍崩壊を分けることを示します。 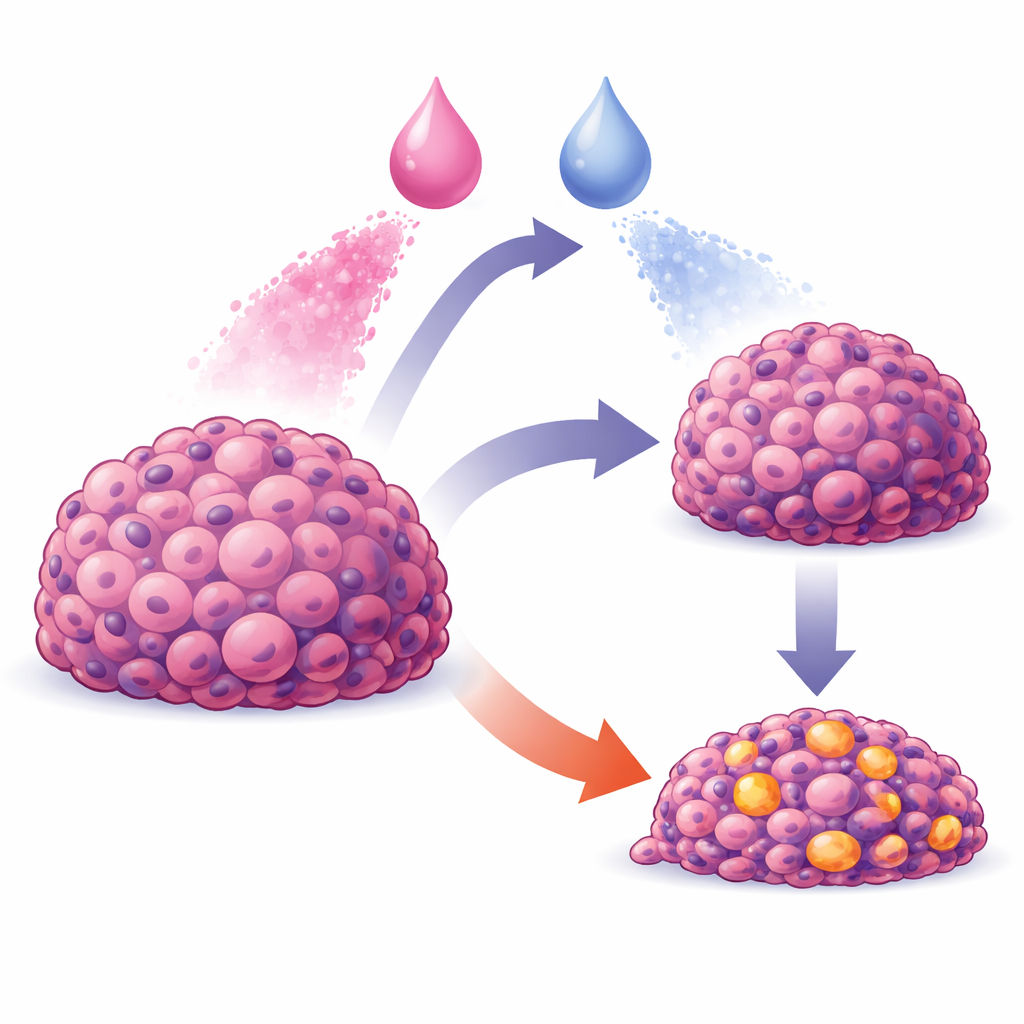
単一細胞と全腫瘍の接続
研究者たちはヒト胃(胃)癌細胞株AGSに着目し、その挙動を反映する「多階層」モデルを構築しました。最も詳細なレベルでは、各仮想細胞が増殖か死の決定に関わる主要なシグナル分子の簡略化された配線図を持ちます。これらの内部スイッチは活性/非活性として表現されますが、組み合わせにより段階的な応答も可能にしています。より高次のレベルでは、各細胞はシミュレーション上の組織内で独立したエージェントとして扱われ、互いに押し合い、混雑を感知すると分裂を止め、内部信号に応じて死ぬか成長を続けるかが決まります。その上位で、薬剤や栄養素は仮想環境中を拡散し、物質が腫瘍様の集団にどのように流入・移動するかを模倣します。
単剤データでモデルを学習させる
仮想システムを現実的にするために、研究チームはまず未処置および単剤曝露時のAGS細胞の増殖を実測データでモデルに学習させました。彼らはがん治療に関連する3つの標的阻害剤を用いました:PI3K阻害剤、MEK阻害剤、AKT阻害剤で、いずれも細胞生存と分裂を促す経路のタンパク質です。高性能計算機上で強力な最適化アルゴリズムを使い、細胞分裂の速度、混雑に対する感受性、薬剤の細胞膜透過性、内部信号が増殖や死に変換される仕組みを制御するパラメータを調整しました。これらの設定により、モデルは観察された増殖曲線を忠実に再現しました:ある薬は主に増殖を遅らせ、別の薬は一時的な増加の後に細胞が収縮し、三つ目は時間経過で集団を着実に減少させました。
併用効果を見ずに相乗効果を予測する
モデルが単剤の振る舞いを模倣できるようになった後、鍵となる試験は学習中に併用データを一切与えずに併用時の挙動を予測できるかどうかでした。研究者たちは三つの単剤フィットに整合するパラメータ範囲を構成し、既知の相乗的ペアであるPI3K+MEK阻害とAKT+MEK阻害について何千もの仮想実験を行いました。驚くべきことに、シミュレーションによる併用は実験で見られた期待以上の成長抑制を再現しました。モデルは各ペアが異なる強みを組み合わせて作用していることを示しました:一方の薬が増殖シグナルを強力に遮断し、もう一方が細胞を自己破壊へと傾ける。両者がそろうことで生存シグナルが遮断され、死を促すシグナルが増強され、どちらか一方だけでは達成できないほど多くの細胞が死に向かいます。 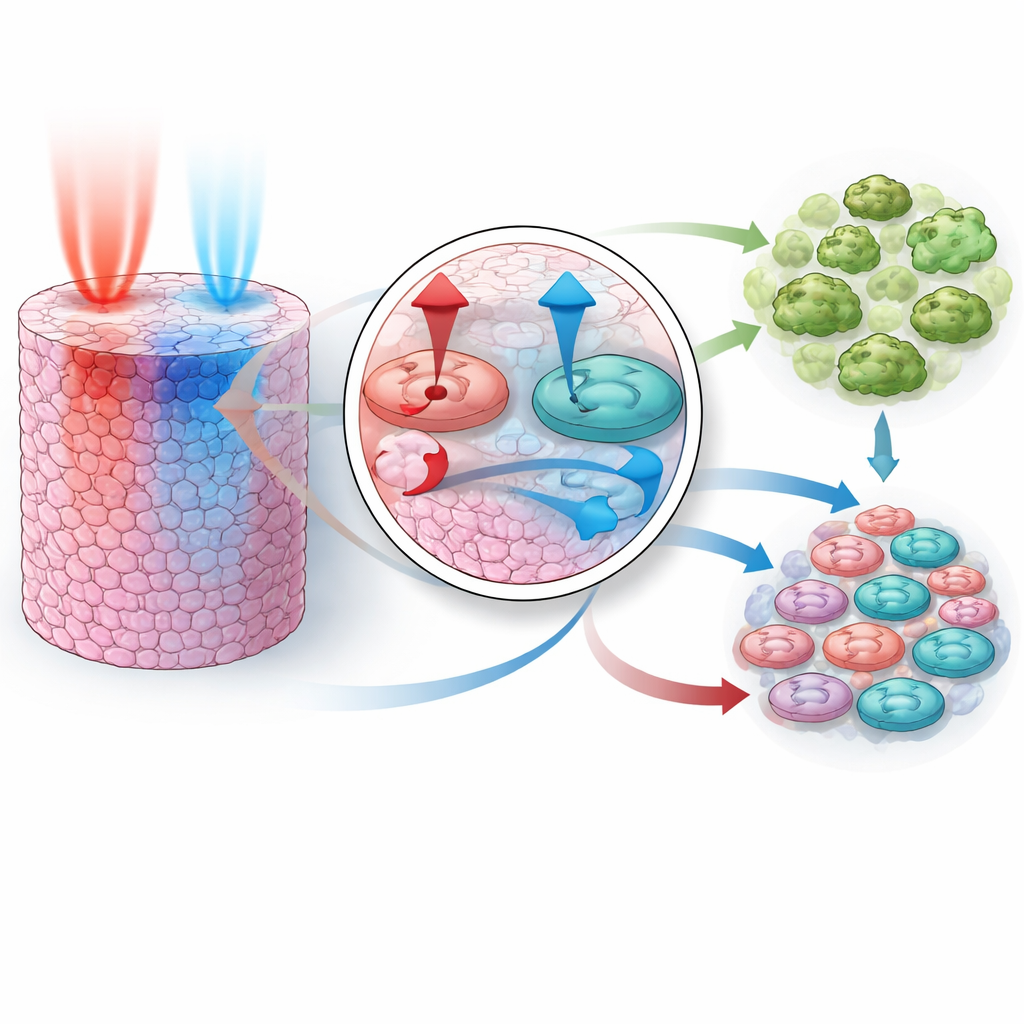
相乗作用のメカニズムを覗く
モデルは分子スイッチから集団の結果までを追跡するため、相乗作用がどのように生じるかについて仮説を提示できます。PI3KとMEK阻害剤の場合、シミュレーションは細胞が全体的に「死に対して準備ができた(プライムされた)」状態になることを示唆しました:アポトーシスを誘導する閾値が下がり、特にCaspase-9を関与させる経路を通じて細胞死を実行する内部機構の活性が高まります。AKTとMEKの組み合わせでは異なる経路が示されました:成長促進因子に結び付く生存シグナルが弱まり、それに対抗して細胞死を促す因子の影響力が増します。この場合、相乗効果はCaspase-8が駆動する別の死の経路により大きく依存しているようです。これらの異なるメカニズムは、同じ最終結果—強い細胞死—が内部配線の違いを通じて達成され得ることを際立たせます。
成功を形作るのはタイミングと薬の移動
研究チームはモデルを三次元に拡張し、薬剤が一方の側から侵入して層を透過していく小さな固形腫瘍を模倣しました。このより現実的な設定で、2剤を同時に投与する場合や一方を別の前にさまざまな時間差で投与する場合、ならびに各薬の組織内拡散速度を変化させると結果がどう変わるかを調べました。シミュレーションは明確なルールを明らかにしました:PI3K/AKT経路で制御される経路は、組み合わせ治療が高い効果を示すために、MEKが制御する経路よりも先、あるいは同時に抑えられていなければなりません。もしMEKが先に遮断されると、ネットワーク内のフィードバックによりPI3K/AKT活性が回復し、細胞生存が一時的に救出されて全体効果が弱まります。各薬の拡散速度の違いはこの影響を増幅し、患者レベルで「同時投与」しても細胞に到達する順序が異なることがあり得ることを示します。
今後のがん治療にとっての意味
この研究は、単剤実験に基づいて注意深く較正されたコンピュータモデルが、薬剤ペアの時間経過に伴う挙動を予測し、投与順序が重要となる理由を示唆できることを示しています。細胞内の分子論理を細胞集団の振る舞いや薬剤の物理的移動と結びつけることで、どのスケジュールが実験室や最終的には患者で最も有効かについて、具体的で検証可能なアイデアを生み出せます。現在の結果は特定の胃がん細胞株に特化したものである一方で、同じ手法は他のがんにも適用でき、試行錯誤に頼るのではなく、より賢明な併用と投与タイミングの設計を研究者に助けるでしょう。
引用: Hayoun-Mya, O., Montagud, A., Valencia, A. et al. Experimentally calibrated multiscale model predicts schedule dependent drug combination effects. npj Syst Biol Appl 12, 52 (2026). https://doi.org/10.1038/s41540-026-00669-4
キーワード: がん薬剤併用, 多階層モデリング, 薬剤スケジューリング, 胃がん, 計算腫瘍学