Clear Sky Science · fr
Modèle multiéchelle calibré expérimentalement prédit des effets de combinaisons médicamenteuses dépendants du calendrier
Pourquoi le timing compte dans le traitement du cancer
Le traitement du cancer ne se résume pas à choisir les bons médicaments ; il s’agit aussi de les administrer de la bonne manière et au bon moment. De nombreuses paires médicamenteuses prometteuses paraissent puissantes dans des conditions de laboratoire simples, mais perdent leur efficacité dans de véritables tumeurs, où les médicaments se répartissent de façon inégale et où les cellules répondent de manière complexe et coordonnée. Cette étude présente un modèle informatique qui relie ce qui se passe à l’intérieur de cellules cancéreuses individuelles à ce qui se passe dans une masse cellulaire entière, et montre comment l’ordre et le timing de deux médicaments peuvent faire la différence entre un ralentissement modéré de la croissance et un effondrement tumoral spectaculaire. 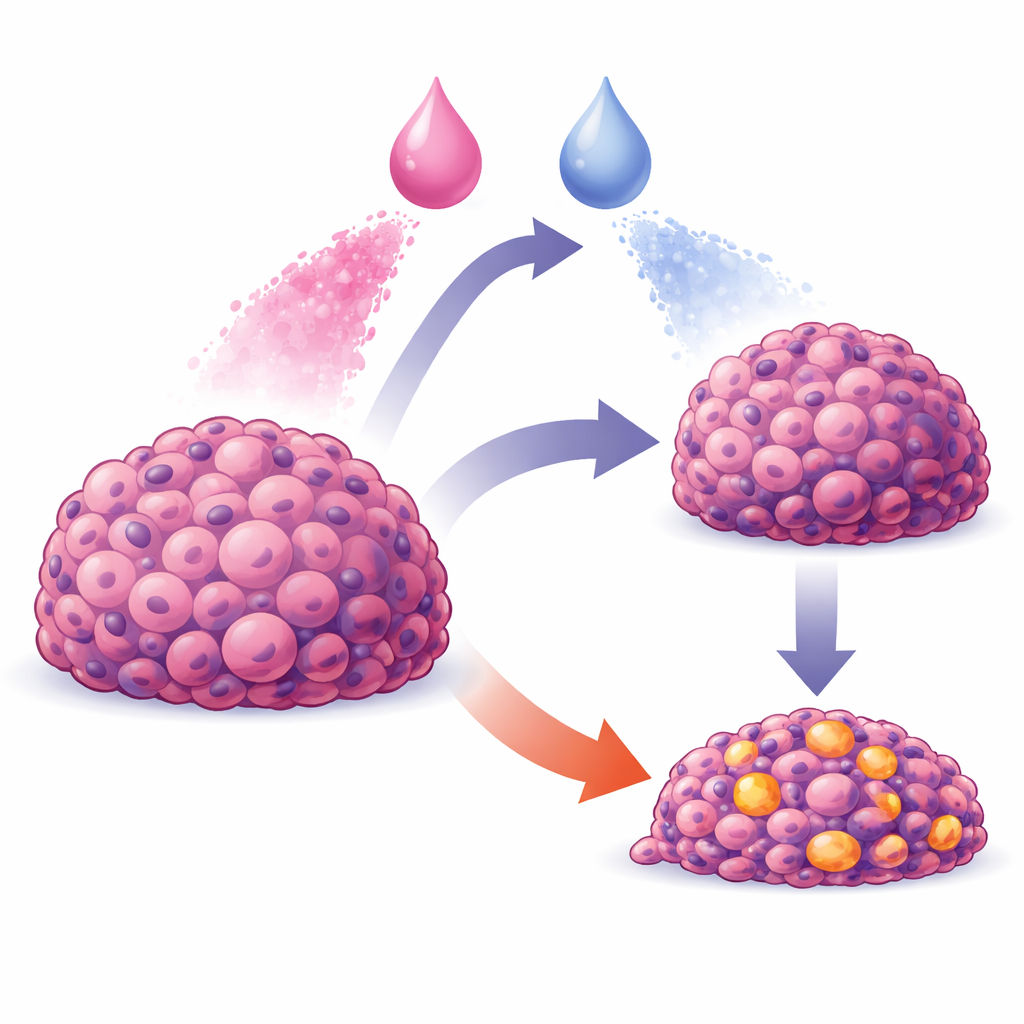
Relier la cellule unique à la tumeur entière
Les chercheurs se sont concentrés sur une lignée cellulaire humaine de cancer gastrique appelée AGS et ont construit un modèle « multiéchelle » reproduisant son comportement. Au niveau le plus détaillé, chaque cellule virtuelle porte un schéma simplifié des principales molécules de signalisation qui déterminent si la cellule croît ou meurt. Ces interrupteurs internes sont représentés comme actifs ou inactifs, mais combinés de façon à permettre des réponses graduées. À un niveau supérieur, chaque cellule est un agent indépendant dans un tissu simulé : les cellules se poussent mutuellement, arrêtent de se diviser lorsqu’elles se sentent à l’étroit, et peuvent mourir ou continuer à croître selon leurs signaux internes. Au-delà de cela, les médicaments et les nutriments diffusent à travers un environnement virtuel, imitant la façon dont les substances pénètrent et traversent un amas de cellules rappelant une tumeur.
Enseigner le modèle avec des données sur un seul médicament
Pour rendre le système virtuel réaliste, l’équipe l’a d’abord entraîné sur des mesures réelles de la croissance des cellules AGS au fil du temps, non traitées ou exposées à un seul médicament. Ils ont utilisé trois inhibiteurs ciblés pertinents pour le traitement du cancer : l’un bloquant la PI3K, un autre bloquant la MEK, et un troisième bloquant l’AKT, tous des protéines de voies qui favorisent la survie et la division cellulaires. En utilisant des algorithmes d’optimisation puissants exécutés sur des ordinateurs haute performance, ils ont ajusté des paramètres contrôlant la vitesse de division des cellules, leur sensibilité à la densité, la facilité avec laquelle les médicaments traversent les membranes cellulaires, et la manière dont les signaux internes sont convertis en croissance ou en mort. Avec ces réglages, le modèle a reproduit de près les courbes de croissance observées : un médicament ralentissait principalement la croissance, un autre provoquait un recul de la population après un bref pic, et un troisième réduisait régulièrement le nombre de cellules au fil du temps.
Prédire la synergie sans l’avoir vue
Une fois que le modèle pouvait imiter le comportement d’un seul médicament, le test clé était de savoir s’il pouvait prédire ce qui se passe lorsque les médicaments sont combinés, sans avoir été alimenté par des données de combinaisons lors de l’entraînement. Les chercheurs ont construit des plages de paramètres compatibles avec les trois ajustements mono-médicament, puis ont exécuté des milliers d’expériences virtuelles pour deux paires connues pour être synergiques : inhibition de PI3K plus MEK, et inhibition d’AKT plus MEK. De manière remarquable, les combinaisons simulées reproduisaient la suppression de croissance plus forte que prévu observée dans les expériences réelles. Le modèle montrait que chaque paire agit en combinant des forces complémentaires : un médicament bloque fortement les signaux de croissance, l’autre pousse les cellules vers l’autodestruction. Ensemble, ils éteignent à la fois les signaux pro-survie et renforcent les signaux pro-mort, entraînant une fraction beaucoup plus grande de cellules vers la mort que chacun ne pourrait le faire seul. 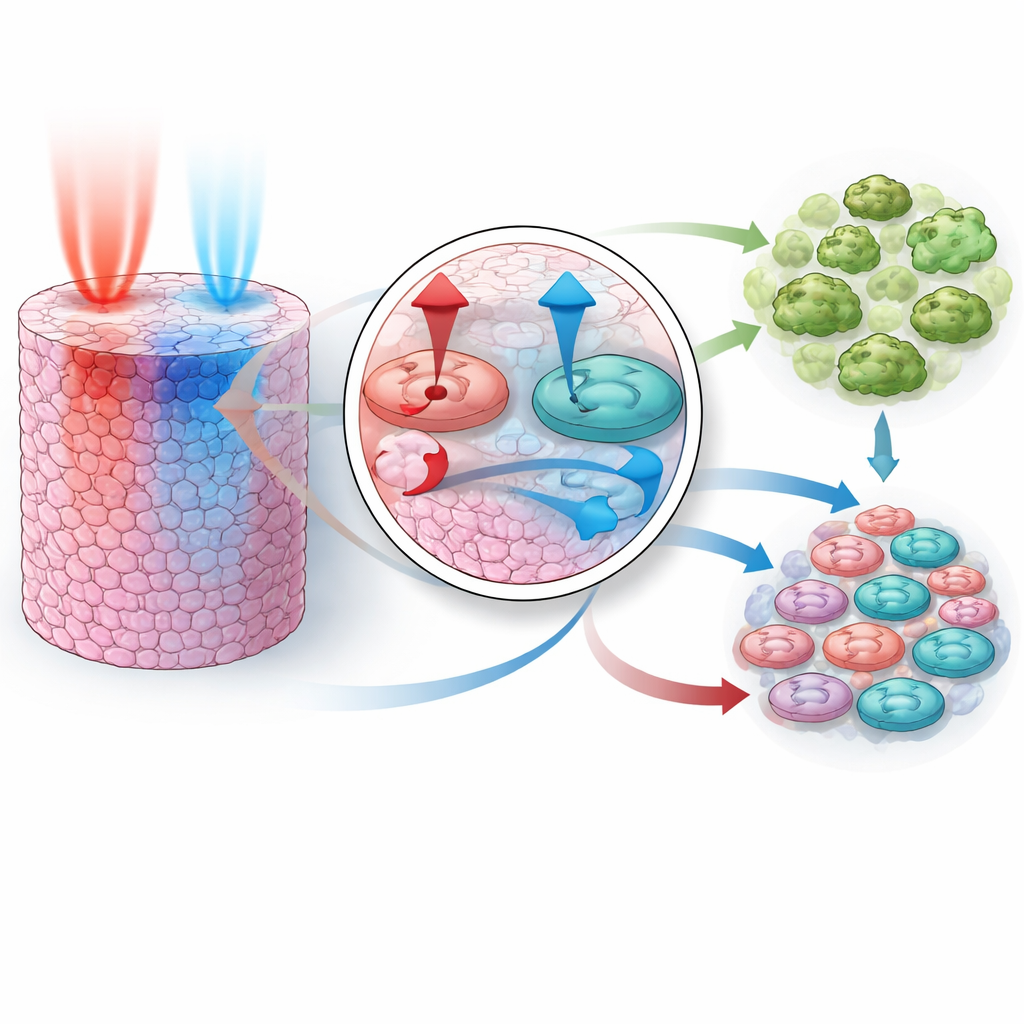
Explorer le mécanisme de la synergie
Parce que le modèle suit les événements depuis les interrupteurs moléculaires jusqu’aux résultats au niveau de la population, il peut proposer des hypothèses sur l’origine de la synergie. Pour les inhibiteurs de PI3K et MEK, les simulations suggèrent que les cellules deviennent globalement « préparées » à la mort : leur seuil de déclenchement de l’apoptose baisse, et la machinerie interne exécutant la mort cellulaire devient plus active, en particulier via des voies impliquant la protéine Caspase-9. Pour la paire AKT et MEK, le modèle indique une route différente : les signaux de survie liés à un facteur promoteur de croissance sont atténués, tandis qu’un facteur antagoniste favorisant la mort cellulaire gagne en influence. Dans ce cas, la synergie semble dépendre davantage d’une voie alternative de mort dirigée par Caspase-8. Ces mécanismes distincts illustrent comment un même résultat global — un effet cytotoxique renforcé — peut être atteint par des câblages internes différents.
Le timing et le mouvement des médicaments façonnent le succès
L’équipe a ensuite étendu le modèle en trois dimensions pour imiter une petite tumeur solide, où les médicaments pénètrent d’un côté et doivent diffuser vers l’intérieur à travers des couches cellulaires. Dans ce cadre plus réaliste, ils ont exploré ce qui se passe si les deux médicaments sont administrés ensemble, ou si l’un précède l’autre de différents laps de temps, et comment des variations de la vitesse de diffusion de chaque médicament dans le tissu affectent le résultat. Les simulations ont révélé une règle claire : la voie contrôlée par PI3K et AKT doit être inhibée avant ou en même temps que la voie contrôlée par MEK pour que la combinaison soit très efficace. Si MEK est bloqué en premier, des rétroactions au sein du réseau permettent à l’activité PI3K/AKT de rebondir, sauvant temporairement la survie cellulaire et atténuant l’effet global. Les différences dans la rapidité de diffusion de chaque médicament amplifient cet effet, ce qui signifie qu’une dose « simultanée » au niveau du patient peut arriver en réalité dans un ordre particulier au niveau des cellules elles-mêmes.
Ce que cela implique pour les traitements futurs du cancer
Ce travail montre qu’un modèle informatique soigneusement calibré, fondé sur des expériences en mono-traitement, peut anticiper avec succès le comportement des paires de médicaments au fil du temps et expliquer pourquoi l’ordre d’administration importe. En reliant la logique moléculaire à l’intérieur des cellules au comportement d’une population cellulaire entière et au mouvement physique des médicaments, le cadre peut générer des idées concrètes et testables sur quels schémas posologiques devraient fonctionner au mieux en laboratoire et, à terme, chez les patients. Bien que les résultats actuels s’appliquent spécifiquement à une lignée de cancer gastrique, la même approche pourrait être adaptée à d’autres cancers, aidant les chercheurs à concevoir des combinaisons et des stratégies temporelles plus intelligentes plutôt que de s’en remettre uniquement à l’essai‑erreur.
Citation: Hayoun-Mya, O., Montagud, A., Valencia, A. et al. Experimentally calibrated multiscale model predicts schedule dependent drug combination effects. npj Syst Biol Appl 12, 52 (2026). https://doi.org/10.1038/s41540-026-00669-4
Mots-clés: combinaisons de médicaments anticancéreux, modélisation multiéchelle, programmation des traitements, cancer gastrique, oncologie computationnelle