Clear Sky Science · ar
نموذج متعدد المقياس معاير تجريبياً يتنبأ بتأثيرات تركيبات الأدوية المعتمدة على الجدول الزمني
لماذا التوقيت مهم في علاج السرطان
العلاج من السرطان لا يقتصر على اختيار الأدوية الصحيحة فحسب؛ بل على إعطائها بالطريقة الصحيحة وفي الوقت المناسب أيضاً. تبدو العديد من الأزواج الدوائية الواعدة قوية في أطباق المختبر البسيطة لكنها تفقد فعاليتها في الأورام الحقيقية، حيث تنتشر الأدوية بشكل غير متساوٍ وتستجيب الخلايا بطرق معقدة ومنسقة. تقدم هذه الدراسة نموذجاً حاسوبياً يربط ما يحدث داخل خلية سرطانية مفردة بما يحدث في كتلة كاملة من الخلايا، ويُظهر كيف يمكن أن يحدد ترتيب وتوقيت دواءين الفارق بين إبطاء نمو طفيف وانهيار كبير للورم. 
ربط الخلايا المفردة بالأورام الكاملة
ركز الباحثون على سلالة خلوية بشرية لسرطان المعدة تُسمى AGS وبنوا نموذجاً «متعدد المقياس» يعكس سلوكها. على أدق مستوى، تحمل كل خلية افتراضية مخططاً مبسّطاً للدارات الحيوية للجزيئات الإشارية الرئيسية التي تقرر ما إذا كانت الخلية ستنمو أم تموت. تمثل هذه المفاتيح الداخلية كحالة نشطة أو غير نشطة، ولكن مدمجة بطريقة تسمح بردود فعل متدرجة. على مستوى أعلى، تعمل كل خلية كعامل مستقل في نسيج محاكى: تضغط الخلايا على بعضها، تتوقف عن الانقسام عند شعورها بالازدحام، ويمكن أن تموت أو تستمر في النمو اعتماداً على إشاراتها الداخلية. فوق ذلك، تنتشر الأدوية والمغذيات عبر بيئة افتراضية، مقلدةً كيف تتحرك المواد إلى داخل الكتلة الشبيهة بالورم وخلالها.
تعليم النموذج ببيانات الدواء الواحد
لجعل النظام الافتراضي واقعياً، درّب الفريق النموذج أولاً على قياسات حقيقية لكيفية نمو خلايا AGS مع مرور الوقت عندما تكون غير معالجة أو معرضة لأدوية مفردة. استخدموا ثلاثة مثبطات موجهة ذات صلة بعلاج السرطان: واحد يثبط PI3K، وآخر يثبط MEK، وثالث يثبط AKT، وهي بروتينات في مسارات تعزز بقاء الخلايا وانقسامها. باستخدام خوارزميات تحسين قوية على حواسب عالية الأداء، ضبطوا معلمات تتحكم بسرعة انقسام الخلايا، وحساسيتها للازدحام، وسهولة عبور الأدوية أغشية الخلايا، وكيف تُحوّل الإشارات الداخلية إلى نمو أو موت. بهذه الإعدادات، كرَّر النموذج منحنيات النمو المرصودة عن كثب: دواء واحد أبطأ النمو بشكل رئيسي، وآخر تسبب في انكماش الخلايا بعد اندفاعة قصيرة، وثالث خفّض العدد بانتظام مع مرور الوقت.
التنبؤ بالتآزر دون رؤيته أثناء التدريب
بمجرد أن استطاع النموذج محاكاة سلوك الدواء الواحد، كان الاختبار الرئيسي هو ما إذا كان يستطيع التنبؤ بما يحدث عند دمج الأدوية، دون أن تُعرض عليه أي بيانات عن التركيبات أثناء التدريب. بنى الباحثون نطاقات للمعلمات تتوافق مع جميع تطابقات الأدوية المفردة الثلاثة، ثم أجروا آلاف التجارب الافتراضية لاثنين من الأزواج المعروفة بتآزرها: تثبيط PI3K مع MEK، وتثبيط AKT مع MEK. بشكل ملحوظ، أعادت التركيبات المحاكاة الضغط الأقوى من المتوقع على النمو كما شوهد في التجارب الحقيقية. أظهر النموذج أن كل زوج يعمل بدمج قوى مختلفة: دواء واحد يعيق إشارات النمو بقوة، والآخر يدفع الخلايا نحو الانتحار الذاتي. معاً، يغلقان إشارات البقاء ويعززان إشارات الموت، ما يدفع جزءاً أكبر بكثير من الخلايا إلى الموت مما يستطيع أي منهما فعله بمفرده. 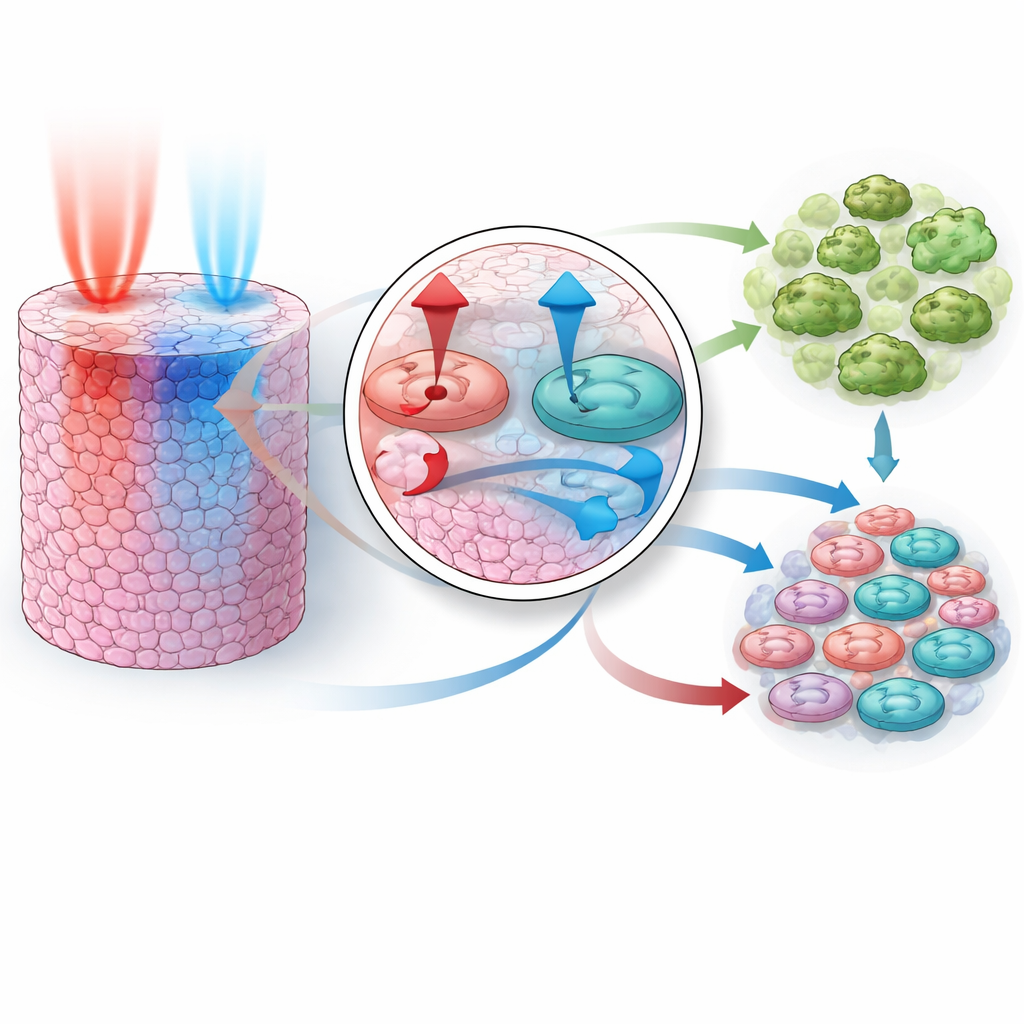
التعمق في آلية التآزر
لأن النموذج يتتبع الأحداث من المفاتيح الجزيئية إلى نتائج السكان، يمكنه تقديم فرضيات حول كيفية نشوء التآزر. بالنسبة لمثبطي PI3K وMEK، اقترحت المحاكاة أن الخلايا تصبح «مهيأة» بشكل عام للموت: ينخفض العتبة اللازمة لإطلاق الاستماتة، وتصبح الآلية الداخلية التي تنفذ موت الخلية أكثر نشاطاً، خاصة عبر مسارات تشمل البروتين Caspase-9. بالنسبة لزوج AKT وMEK، أشار النموذج إلى مسار مختلف: تُخفف إشارات البقاء المرتبطة بعامل محفز للنمو، بينما يكتسب عامل مضاد يروج لموت الخلايا نفوذاً أكبر. في هذه الحالة، يبدو أن التآزر يعتمد بصورة أكبر على مسار موت بديل يقوده Caspase-8. تبرز هذه الآليات المختلفة كيف يمكن أن يتحقق نفس الناتج العام—قتل أقوى—من خلال دارات داخلية مغايرة.
يشكّل التوقيت وحركة الدواء النجاح
ثم وسع الفريق النموذج إلى ثلاثة أبعاد لمحاكاة ورم صلب صغير، حيث تدخل الأدوية من جهة واحدة ويجب أن تنتشر إلى الداخل عبر طبقات الخلايا. في هذا الإطار الأكثر واقعية، استكشفوا ما يحدث إذا أعطي الدواءان معاً، أو إذا سبق أحدهما الآخر بفترات زمنية مختلفة، وكيف تؤثر تغييرات سرعة حركة كل دواء عبر النسيج على النتيجة. كَشَفت المحاكاة قاعدة واضحة: يجب تعطيل المسار الذي يتحكم فيه PI3K وAKT قبل أو في نفس وقت تعطيل المسار الذي يتحكم فيه MEK لكي يكون الجمع فعالاً بدرجة عالية. إذا تم حجب MEK أولاً، تسمح ردود الفعل داخل الشبكة لفعالية PI3K/AKT بأن تعود، مما ينقذ الخلايا مؤقتاً ويخفف الأثر العام. الاختلافات في سرعات انتشار الأدوية تضخم هذا التأثير، ما يعني أن جرعة «متزامنة» على مستوى المريض قد تصل بترتيب معين إلى الخلايا نفسها.
ماذا يعني هذا لعلاج السرطان في المستقبل
تُظهر هذه الدراسة أن نموذجاً حاسوبياً معايراً بعناية ومستنداً إلى تجارب الأدوية المفردة، يمكنه التنبؤ بنجاح بكيفية تصرف أزواج الأدوية مع مرور الوقت وتوضيح سبب أهمية ترتيب الجرعات. من خلال ربط المنطق الجزيئي داخل الخلايا بسلوك مجموعة الخلايا وحركة الأدوية الفيزيائية، يستطيع الإطار توليد أفكار ملموسة قابلة للاختبار حول أي الجداول الزمنية قد تنجح في المختبر ولاحقاً لدى المرضى. وبينما تنطبق النتائج الحالية على سلالة واحدة من سرطان المعدة على وجه الخصوص، يمكن تكييف النهج نفسه مع سرطانات أخرى، لمساعدة الباحثين على تصميم تجمعات واستراتيجيات توقيت أذكى بدلاً من الاعتماد فقط على التجربة والخطأ.
الاستشهاد: Hayoun-Mya, O., Montagud, A., Valencia, A. et al. Experimentally calibrated multiscale model predicts schedule dependent drug combination effects. npj Syst Biol Appl 12, 52 (2026). https://doi.org/10.1038/s41540-026-00669-4
الكلمات المفتاحية: تركيبات أدوية السرطان, نمذجة متعددة المقياس, جدولة الأدوية, سرطان المعدة, علم الأورام الحاسوبي