Clear Sky Science · he
מודל רב-סקאלי כיול ניסוי מנבא השפעות תלויי לוח זמנים בשילובי תרופות
מדוע התזמון חשוב בטיפול בסרטן
טיפול בסרטן אינו רק בחירה של התרופות הנכונות; הוא גם בחירה של האופן שבו מעניקים אותן ובזמנים המתאימים. זוגות תרופות מבטיחים רבים נראים עוצמתיים במנות מעבדה פשוטות אך מאבדים את עוצמתם בגידולים אמיתיים, שבהם התרופות מתפשטות באופן לא אחיד והתאים מגיבים בצורה מורכבת ומתואמת. המחקר הזה מציג מודל ממוחשב המקשר בין מה שמתרחש בתוך תא סרטן יחיד למה שקורה במסת תאים שלמה, ומצביע על כך שהסדר והתזמון של שתי תרופות יכולים להכריע בין האטה מתונה של הצמיחה לבין התמוטטות דרמטית של הגידול. 
קישור בין תאים יחידים לגידולים שלמים
החוקרים התמקדו בקו תאי סרטן קיבה אנושי הנקרא AGS ובנו "מודל רב-סקאלי" המשקף את התנהגותו. ברמה המפורטת ביותר, כל תא וירטואלי נושא דיאגרמת חיווט מפושטת של מולקולות איתות מרכזיות המכריעות האם התא יגדל או ימות. מתגים פנימיים אלה מיוצגים כפעילים או לא פעילים, אך משולבים באופן המאפשר תגובות מדורגות. ברמה גבוהה יותר, כל תא הוא סוכן עצמאי ברקמה מדומה: תאים דוחפים אחד את השני, מפסיקים להתחלק כשהם חשים צפיפות, ויכולים למות או להמשיך לגדול בהתאם לאותות הפנימיים שלהם. מעל לכך, תרופות וחומרי מזון מפזרים דרך סביבה וירטואלית, מחקה כיצד חומרים נכנסים ונדחפים דרך צבר תאי דמוי גידול.
לאמן את המודל על פי נתונים של תרופה יחידה
כדי להפוך את המערכת הווירטואלית לריאלית, הצוות קודם כל אילף אותה על מדידות אמיתיות של האופן שבו תאי AGS גדלים לאורך זמן כאשר אינם מטופלים או חשופים לתרופות יחידות. הם השתמשו בשלושה מעכבים ממוקדים הרלוונטיים לטיפול בסרטן: אחד החוסם PI3K, אחד החוסם MEK, ואחד החוסם AKT — כולם חלבונים במסלולים המעודדים הישרדות ותא חלוקה. באמצעות אלגוריתמי אופטימיזציה רבי עוצמה שרצו על מחשבים בעלי ביצועים גבוהים, כיוונו פרמטרים שמפקחים על קצב חלוקת התאים, הרגישות שלהם לצפיפות, הקלות שבה תרופות חודרות ממברנות התא, ואופן שבו אותות פנימיים מתורגמים לצמיחה או למות. בעזרת הגדרות אלה, המודל שיחזר במדויק את עקומות הגדילה שנצפו: תרופה אחת האטה בעיקר את הצמיחה, אחרת גרמה לתאים להתכווץ אחרי פרץ קצר, ושלישית הקטינה בעקביות את האוכלוסייה לאורך זמן.
לחזות סינרגיה מבלי לראות אותה
ברגע שהמודל הצליח לחקות התנהגות של תרופה יחידה, המבחן המרכזי היה האם יוכל לחזות מה קורה כשמשלבים תרופות, מבלי להיחשף לנתוני שילובים במהלך האימון. החוקרים בנו טווחי פרמטרים שתאמו את כל שלוש ההתאמות ליחידות התרופות, ואז הריצו אלפי ניסויים וירטואליים לשני זוגות ידועים כסינרגטיים: עיכוב PI3K ביחד עם MEK, ועיכוב AKT ביחד עם MEK. באופן מרשים, השילובים המדומים שיחזרו את עוצמת הדיכוי החזקה מהמצופה בצמיחה שנראתה בניסויים אמיתיים. המודל הראה כי כל זוג פועל על ידי שילוב חוזקות שונות: תרופה אחת חוסמת בחוזקה אותות צמיחה, והאחרת דוחפת את התאים לעבר השמדה עצמית. יחד, הן גם מכבות רמזים לתפקיד הישרדות וגם מחזקות אותות לעבר מוות, ודוחפות חלק גדול יותר של תאים למות מאשר כל אחת מהן לחוד. 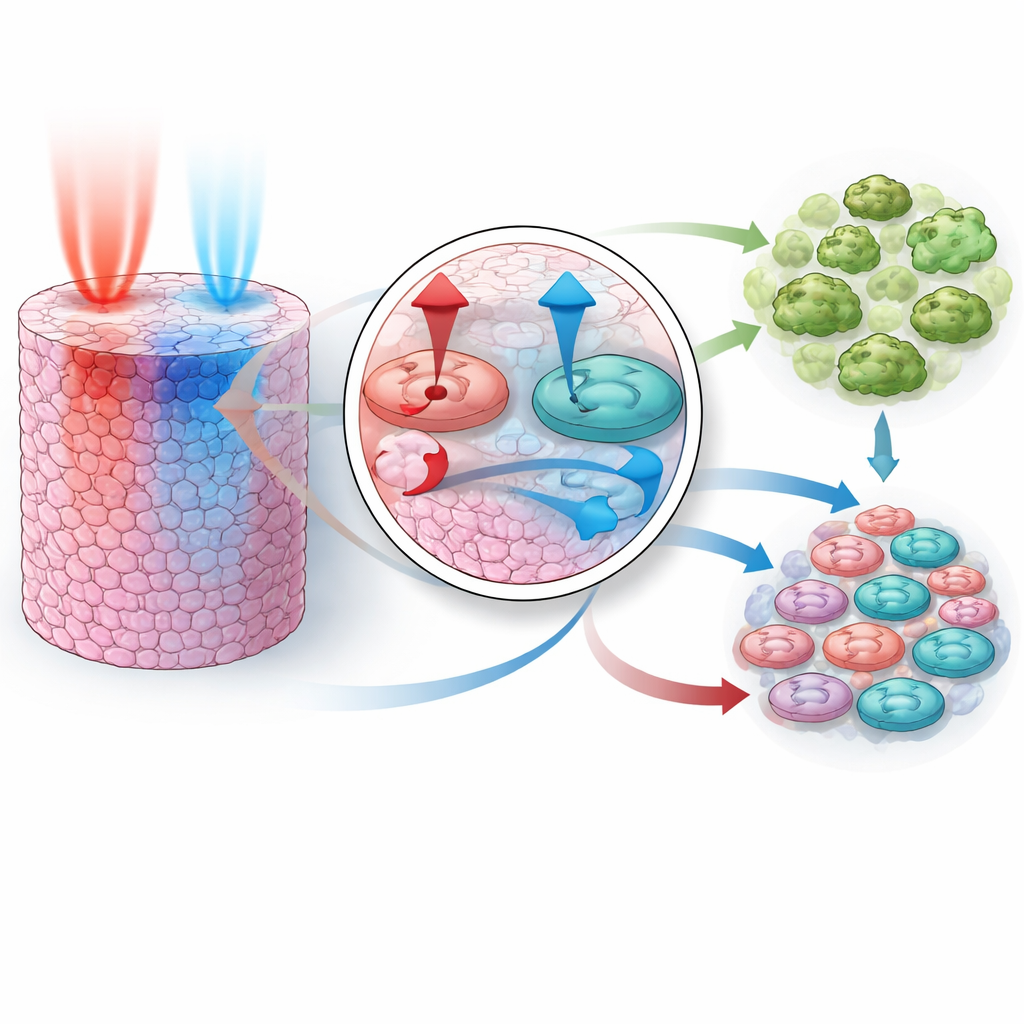
להציץ במנגנון הסינרגיה
מכיוון שהמודל עוקב אחרי אירועים ממתגים מולקולריים עד לתוצאות באוכלוסייה, הוא יכול להציע השערות לגבי מקור הסינרגיה. בעבור מעכבי PI3K ו-MEK, הסימולציות הציעו כי התאים נעשים באופן גלובלי "מוכנים" למות: הסף שלהם להוביל לאפופטוזיס יורד, והמנגנון הפנימי שמבצע את מוות התא נעשה פעיל יותר, במיוחד דרך מסלולים המעורבים בחלבון Caspase-9. עבור זוג AKT ו-MEK, המודל הצביע על נתיב שונה: האותות התומכים בהישרדות הקשורים לגורם המעודד צמיחה מדוכאים, בעוד גורם מנוגד המעודד מוות תופס השפעה רבה יותר. במקרה זה, נראה שהסינרגיה תלויה יותר בדרך חלופית למוות שמונעת על ידי Caspase-8. מנגנונים מובחנים אלה מדגישים כיצד אותה תוצאה כוללת — הרג חזק יותר — יכולה להשיג באמצעות חיווט פנימי שונה.
תזמון ותנועה של תרופות מעצבים את ההצלחה
הצוות הרחיב אז את המודל לתלת־ממד כדי לחקות גידול מוצק קטן, שבו התרופות נכנסות מצד אחד וחייבות לדיפוזיה פנימה דרך שכבות של תאים. בהגדרה מציאותית יותר זו, הם בדקו מה קורה אם שתי התרופות ניתנות יחד, או אם אחת מקדימה את השנייה בהפרשים של זמן שונים, וכיצד שינויים בקצב התפשטות כל תרופה ברקמה משפיעים על התוצאה. הסימולציות חשפו כלל ברור: המסלול הנשלט על ידי PI3K ו-AKT חייב להיות מושתק לפני או באותו זמן כמו המסלול הנשלט על ידי MEK כדי שהשילוב יהיה אפקטיבי מאוד. אם MEK נחסם קודם, משוב בתוך הרשת מאפשר לפעילות PI3K/AKT להחלים, מציל באופן זמני את הישרדות התא ומחליש את האפקט הכולל. הבדלים במהירות הדיפוזיה של כל תרופה מגבירים אפקט זה, משמעות הדבר היא שגם מינון "סימולטני" ברמת המטופל עשוי להגיע בסדר מסוים לתאים עצמם.
מה המשמעות לטיפול בסרטן בעתיד
העבודה מראה שמודל ממוחשב כיול בקפידה, המבוסס על ניסויים של תרופה יחידה, יכול לחזות בהצלחה כיצד זוגות תרופות יתנהגו לאורך זמן ולהציע מדוע סדר המינונים חשוב. על ידי חיבור לוגיקה מולקולרית בתוך תאים להתנהגות של אוכלוסיית תאים ושל התנועה הפיזית של תרופות, המסגרת יכולה לייצר רעיונות קונקרטיים וניתנים לבחינה לגבי אילו לוחות זמנים אמורים לעבוד הכי טוב במעבדה ובסופו של דבר אצל מטופלים. בעוד שהתוצאות הנוכחיות חלות ספציפית על קו תאי סרטן קיבה אחד, ניתן להתאים את הגישה לצורות סרטן אחרות, וכך לסייע לחוקרים לעצב שילובים ותזמון חכמים יותר במקום להסתמך רק על ניסוי וטעייה.
ציטוט: Hayoun-Mya, O., Montagud, A., Valencia, A. et al. Experimentally calibrated multiscale model predicts schedule dependent drug combination effects. npj Syst Biol Appl 12, 52 (2026). https://doi.org/10.1038/s41540-026-00669-4
מילות מפתח: שילובי תרופות בסרטן, מִדּוּל רב-סקאלי, תזמון תרופתי, סרטן קיבה, אונקולוגיה חישובית