Clear Sky Science · sv
Experimentellt kalibrerad multiskalmodell förutspår schema‑beroende effekter av läkemedelskombinationer
Varför timing spelar roll vid cancerbehandling
Cancerterapi handlar inte bara om att välja rätt läkemedel; det handlar också om att ge dem på rätt sätt och vid rätt tidpunkt. Många lovande läkemedelspar ser kraftfulla ut i enkla laboratorieförsök men förlorar sin verkan i verkliga tumörer, där läkemedel sprids ojämnt och celler svarar på komplexa, koordinerade sätt. Denna studie presenterar en datorbaserad modell som kopplar vad som händer inuti enskilda cancerceller till vad som händer i en hel cellmassa, och visar hur ordningen och tidpunkten för två läkemedel kan vara avgörande mellan måttlig tillväxthämning och dramatisk tumörkollaps. 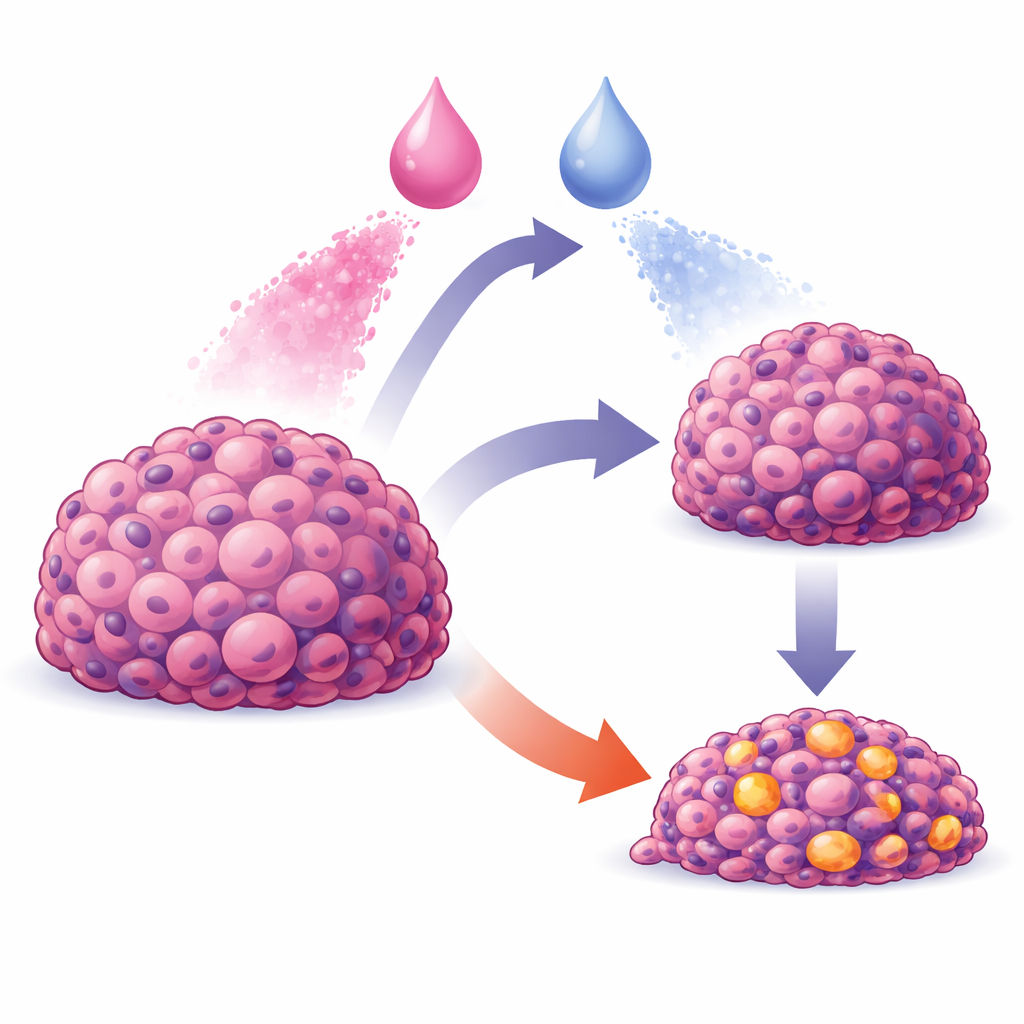
Att länka enskilda celler till hela tumörer
Forskarna fokuserade på en human magcancercellinje kallad AGS och byggde en ”multiskalig” modell som speglar dess beteende. På den mest detaljerade nivån bär varje virtuell cell ett förenklat kopplingsschema av viktiga signalmolekyler som avgör om cellen växer eller dör. Dessa interna brytare representeras som antingen aktiva eller inaktiva, men kombineras på ett sätt som fortfarande tillåter graderade svar. På en högre nivå är varje cell en självständig agent i en simulerad vävnad: celler trycker mot varandra, slutar dela sig när de blir trånga och kan dö eller fortsätta växa beroende på sina interna signaler. Därutöver diffunderar läkemedel och näringsämnen genom en virtuell omgivning, vilket efterliknar hur substanser rör sig in i och genom en tumörliknande klump.
Att lära modellen med enkla läkemedelsdata
För att göra det virtuella systemet realistiskt tränade teamet först modellen på verkliga mätningar av hur AGS‑celler växer över tid när de är obehandlade eller exponeras för enskilda läkemedel. De använde tre målinriktade hämmare som är relevanta för cancerbehandling: en som blockerar PI3K, en som blockerar MEK och en som blockerar AKT — alla proteiner i vägar som främjar cellsurvival och delning. Med kraftfulla optimeringsalgoritmer körda på högpresterande datorer justerade de parametrar som styr hur snabbt celler delar sig, hur känsliga de är för trängsel, hur lätt läkemedel passerar cellmembran och hur interna signaler omvandlas till tillväxt eller död. Med dessa inställningar återgav modellen noggrant de observerade tillväxtkurvorna: ett läkemedel bromsade framför allt tillväxten, ett annat fick cellerna att krympa tillbaka efter en kort surge och ett tredje minskade populationen stadigt över tid.
Att förutsäga synergier utan att ha sett dem
När modellen kunde efterlikna beteendet vid enskilda läkemedel var det avgörande testet om den kunde förutsäga vad som händer när läkemedel kombineras, utan att ha visats några kombinationsdata under träningen. Forskarna konstruerade parameterrang som var förenliga med alla tre enstaka läkemedelsanpassningarna och körde sedan tusentals virtuella experiment för två kända synergiska par: PI3K plus MEK‑hämning och AKT plus MEK‑hämning. Anmärkningsvärt nog återskapade de simulerade kombinationerna den starkare‑än‑förväntade tillväxthämning som sågs i verkliga experiment. Modellen visade att varje par verkar genom att kombinera olika styrkor: ett läkemedel blockerar kraftfullt tillväxtsignaler medan det andra driver celler mot självdestruktion. Tillsammans stänger de både ner pro‑survival‑signaler och förstärker pro‑dödsignaler, vilket driver en mycket större andel celler mot död än vad något av dem kunde åstadkomma ensamt. 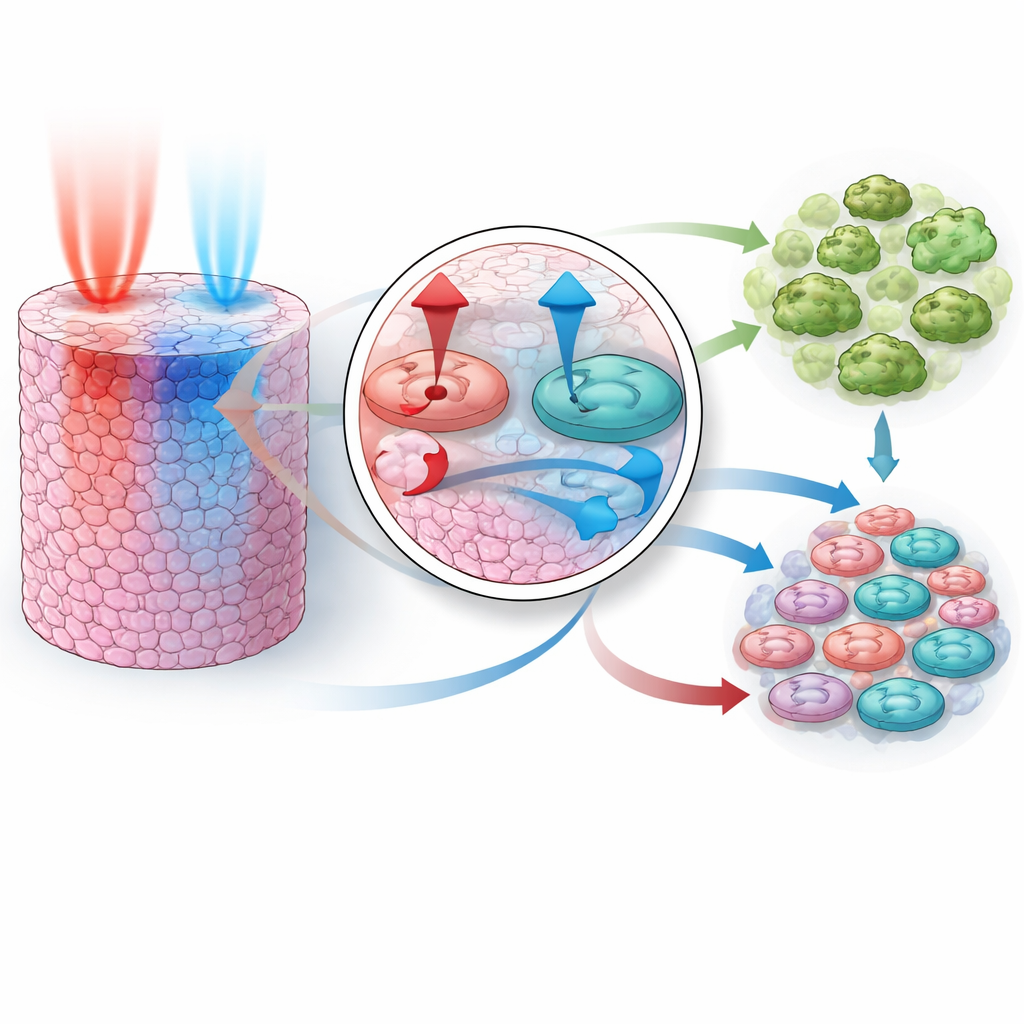
Insikt i mekanismen bakom synergier
Eftersom modellen spårar händelser från molekylära brytare till populationsutfall kan den erbjuda hypoteser om hur synergierna uppstår. För PI3K‑ och MEK‑hämmare föreslog simuleringarna att celler blir globalt ”förberedda” för död: deras tröskel för att utlösa apoptos sjunker och den interna maskineriet som verkställer celldöd blir mer aktiv, särskilt genom vägar som involverar proteinet Caspase‑9. För AKT‑ och MEK‑paret pekade modellen på en annan väg: överlevnadssignaler kopplade till en tillväxtfrämjande faktor dämpas medan en motverkande faktor som uppmuntrar celldöd får större inflytande. I detta fall verkar synergien i större utsträckning bero på en alternativ dödväg som drivs av Caspase‑8. Dessa skilda mekanismer understryker hur samma övergripande utfall — starkare dödande — kan uppnås genom olika interna kopplingar.
Tidpunkt och läkemedelsrörelse formar framgång
Teamet utvidgade därefter modellen till tre dimensioner för att efterlikna en liten solid tumör, där läkemedel kommer in från ena sidan och måste diffundera in genom cellskikten. I denna mer realistiska miljö undersökte de vad som händer om de två läkemedlen ges samtidigt eller om det ena föregår det andra med olika tidsintervall, samt hur förändringar i hur snabbt varje läkemedel rör sig genom vävnaden påverkar utfallet. Simuleringarna avslöjade en tydlig regel: vägen som kontrolleras av PI3K och AKT måste stängas ner före eller samtidigt som vägen som kontrolleras av MEK för att kombinationen ska vara mycket effektiv. Om MEK blockeras först tillåter feedback i nätverket PI3K/AKT‑aktiviteten att återhämta sig, vilket tillfälligt räddar cellsurvival och dämpar den totala effekten. Skillnader i hur snabbt varje läkemedel diffunderar förstärker denna effekt, vilket innebär att även en ”samtidig” dos på patientnivå kan anlända i en bestämd ordning till cellerna själva.
Vad detta betyder för framtida cancerbehandling
Detta arbete visar att en noggrant kalibrerad datorbaserad modell, förankrad i experiment med enskilda läkemedel, framgångsrikt kan förutse hur läkemedelspar beter sig över tid och föreslå varför dosordningen spelar roll. Genom att koppla molekylär logik inuti celler till beteendet hos en hel cellpopulation och till den fysiska rörelsen av läkemedel kan ramverket generera konkreta, testbara idéer om vilka scheman som bör fungera bäst i labbet och, så småningom, hos patienter. Även om de nuvarande resultaten gäller specifikt för en magcancercellinje kan samma angreppssätt anpassas till andra cancerformer och hjälpa forskare att designa smartare kombinationer och tidstrategier i stället för att enbart förlita sig på trial‑and‑error‑testning.
Citering: Hayoun-Mya, O., Montagud, A., Valencia, A. et al. Experimentally calibrated multiscale model predicts schedule dependent drug combination effects. npj Syst Biol Appl 12, 52 (2026). https://doi.org/10.1038/s41540-026-00669-4
Nyckelord: cancermedel i kombination, multiskalig modellering, läkemedelsschemaläggning, gastric cancer, beräkningsonkologi