Clear Sky Science · pl
Eksperymentalnie skalibrowany model wieloskalowy przewiduje zależne od harmonogramu efekty kombinacji leków
Dlaczego czas podania ma znaczenie w leczeniu nowotworów
Terapię nowotworową nie ogranicza wybór właściwych leków — ważne jest też ich właściwe podanie i właściwy moment. Wiele obiecujących par leków działa silnie w prostych modelach laboratoryjnych, lecz traci skuteczność w rzeczywistych guzach, gdzie leki rozprowadzają się nierównomiernie, a komórki reagują w złożony, skoordynowany sposób. W tym badaniu przedstawiono model komputerowy łączący wydarzenia zachodzące w pojedynczych komórkach nowotworowych z zachowaniem całej masy komórek i pokazano, jak kolejność i timing dwóch leków mogą zadecydować o tym, czy nastąpi jedynie umiarkowane spowolnienie wzrostu, czy dramatyczny kolaps guza. 
Łączenie pojedynczych komórek z całymi guzami
Naukowcy skupili się na ludzkiej linii komórkowej raka żołądka AGS i zbudowali „model wieloskalowy”, który odwzorowuje jej zachowanie. Na najbardziej szczegółowym poziomie każda wirtualna komórka zawiera uproszczony schemat połączeń kluczowych molekuł sygnałowych decydujących o wzroście lub śmierci komórki. Te wewnętrzne przełączniki są przedstawione jako aktywne lub nieaktywne, ale połączone w sposób pozwalający na odpowiedzi gradacyjne. Na wyższym poziomie każda komórka jest niezależnym agentem w symulowanej tkance: komórki naciskają na siebie, przestają się dzielić, gdy czują przeludnienie, i mogą umrzeć lub nadal rosnąć w zależności od sygnałów wewnętrznych. Powyżej tego poziomu leki i składniki odżywcze dyfundują przez wirtualne środowisko, naśladując sposób, w jaki substancje przemieszczają się do wnętrza i przez skupisko przypominające guz.
Uczenie modelu na danych z pojedynczych leków
Aby uczynić system wirtualny realistycznym, zespół najpierw nauczył go na podstawie rzeczywistych pomiarów wzrostu komórek AGS w czasie, gdy były one nieleczone lub eksponowane na pojedyncze leki. Użyto trzech inhibitorów ukierunkowanych, istotnych w terapii przeciwnowotworowej: jednego blokującego PI3K, jednego blokującego MEK oraz jednego blokującego AKT — wszystkie białka w szlakach sprzyjających przeżyciu i podziałowi komórek. Korzystając z wydajnych algorytmów optymalizacyjnych uruchamianych na komputerach wysokiej wydajności, dostrojono parametry kontrolujące tempo podziału komórek, wrażliwość na przeludnienie, łatwość przenikania leków przez błony komórkowe oraz sposób, w jaki sygnały wewnętrzne przekładane są na wzrost lub śmierć. Przy tych ustawieniach model wiernie odtwarzał obserwowane krzywe wzrostu: jeden lek głównie spowalniał wzrost, inny powodował cofnięcie się populacji po krótkim wzroście, a trzeci stopniowo zmniejszał liczbę komórek w czasie.
Przewidywanie synergii bez danych o kombinacjach
Kiedy model potrafił naśladować zachowanie pojedynczych leków, kluczowym testem było sprawdzenie, czy przewidzi, co się stanie przy kombinacjach leków, nie widząc żadnych danych o kombinacjach w fazie treningu. Badacze skonstruowali zakresy parametrów zgodne ze wszystkimi trzema dopasowaniami do pojedynczych leków, a następnie przeprowadzili tysiące wirtualnych eksperymentów dla dwóch znanych synergicznych par: inhibitora PI3K razem z inhibitorem MEK oraz inhibitora AKT razem z inhibitorem MEK. Co ciekawe, symulowane kombinacje odtworzyły silniejsze niż oczekiwane tłumienie wzrostu obserwowane w rzeczywistych eksperymentach. Model pokazał, że każda para działa przez połączenie różnych mocnych stron: jeden lek silnie blokuje sygnały wzrostowe, drugi popycha komórki w kierunku autodestrukcji. Razem wyciszają sygnały pro-przeżyciowe i wzmacniają sygnały pro-śmierci, doprowadzając do śmierci znacznie większego odsetka komórek niż przy zastosowaniu któregokolwiek z nich osobno. 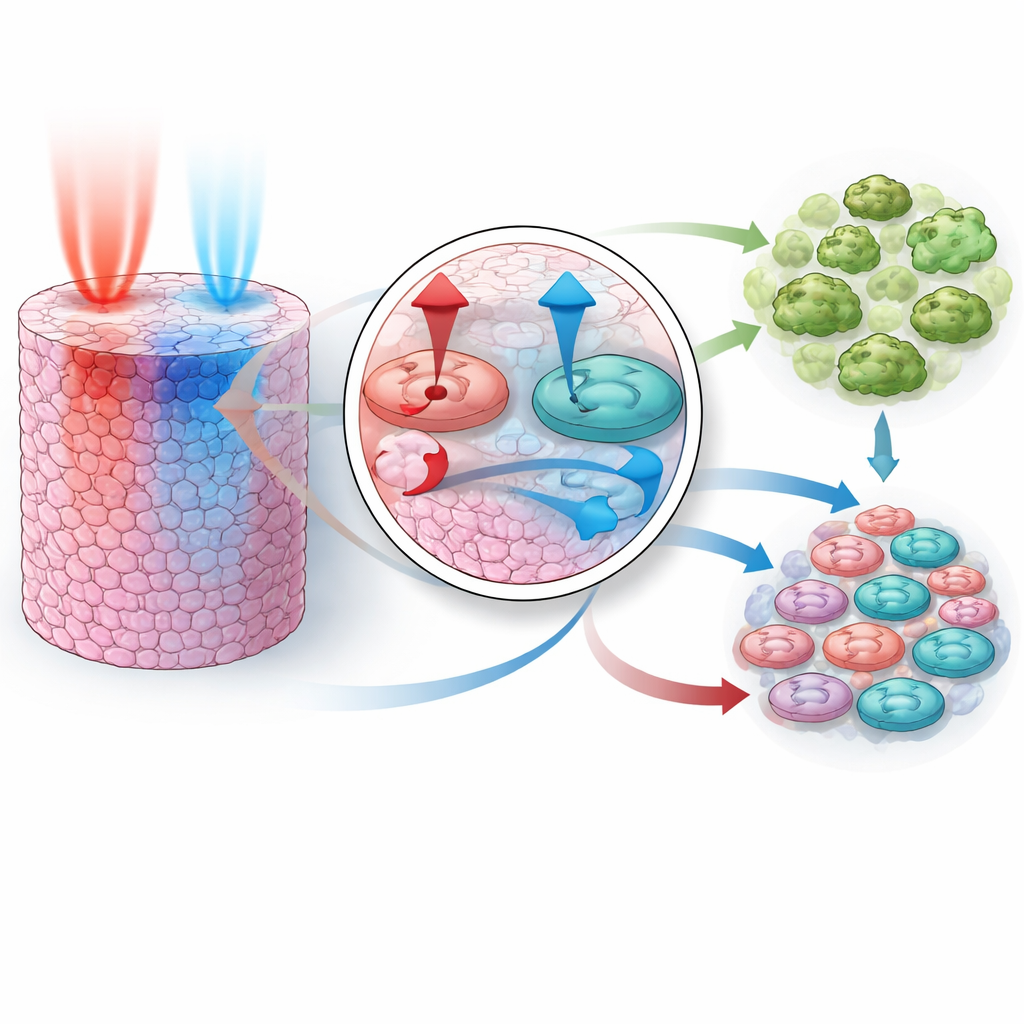
Zaglądanie w mechanizm synergii
Ponieważ model śledzi zdarzenia od molekularnych przełączników po wyniki populacyjne, może dostarczać hipotez dotyczących źródła synergii. Dla inhibitorów PI3K i MEK symulacje sugerowały, że komórki stają się globalnie „zaprzyjaźnione” ze śmiercią — ich próg wywołania apoptozy spada, a wewnętrzne mechanizmy wykonawcze śmierci komórki stają się bardziej aktywne, szczególnie poprzez szlaki związane z białkiem Kaspaza-9. W przypadku pary AKT i MEK model wskazywał inną drogę: osłabione zostają sygnały przeżyciowe powiązane z czynnikiem promującym wzrost, podczas gdy przeciwstawny czynnik zachęcający do śmierci komórki zyskuje na znaczeniu. W tym scenariuszu synergia wydaje się bardziej zależna od alternatywnej ścieżki śmierci prowadzonej przez Kaspazę-8. Te odrębne mechanizmy uwypuklają, że ten sam ogólny efekt — silniejsze zabijanie — może być osiągnięty przez różne wewnętrzne układy połączeń.
Timing i ruch leków kształtują powodzenie terapii
Zespół rozszerzył następnie model do trzech wymiarów, aby naśladować mały guz lity, w którym leki wchodzą z jednej strony i muszą dyfundować przez kolejne warstwy komórek. W tym bardziej realistycznym ustawieniu badali, co się dzieje, gdy dwa leki podaje się jednocześnie, albo gdy jeden poprzedza drugi o różne odstępy czasu, oraz jak zmiany szybkości przemieszczania się każdego leku przez tkankę wpływają na wynik. Symulacje ujawniły jasną zasadę: szlak kontrolowany przez PI3K i AKT musi być wyłączony przed lub równocześnie z szlakiem kontrolowanym przez MEK, aby kombinacja była wysoce skuteczna. Jeśli MEK zostanie zablokowany pierwszy, sprzężenia zwrotne w sieci pozwalają na odbicie aktywności PI3K/AKT, tymczasowo ratując przeżycie komórek i osłabiając ogólny efekt. Różnice w szybkości dyfuzji każdego leku wzmacniają to zjawisko, co oznacza, że nawet „jednoczesna” dawka na poziomie pacjenta może dotrzeć do komórek w określonej kolejności.
Co to oznacza dla przyszłości leczenia raka
Ta praca pokazuje, że starannie skalibrowany model komputerowy, oparty na eksperymentach z pojedynczymi lekami, może trafnie przewidzieć zachowanie par leków w czasie i zasugerować, dlaczego kolejność dawkowania ma znaczenie. Łącząc logikę molekularną w komórkach z zachowaniem całej populacji komórek oraz z fizycznym ruchem leków, ramy te mogą generować konkretne, możliwe do przetestowania pomysły na schematy, które powinny sprawdzić się w laboratorium, a w końcu u pacjentów. Choć obecne wyniki dotyczą specyficznie jednej linii komórek raka żołądka, tę samą metodę można dostosować do innych nowotworów, pomagając badaczom projektować mądrzejsze kombinacje i strategie czasowe zamiast polegać wyłącznie na metodzie prób i błędów.
Cytowanie: Hayoun-Mya, O., Montagud, A., Valencia, A. et al. Experimentally calibrated multiscale model predicts schedule dependent drug combination effects. npj Syst Biol Appl 12, 52 (2026). https://doi.org/10.1038/s41540-026-00669-4
Słowa kluczowe: kombinacje leków przeciwnowotworowych, modelowanie wieloskalowe, harmonogram podawania leków, rak żołądka, onkologia obliczeniowa