Clear Sky Science · zh
脑脊液来源α‑突触核蛋白寡聚体沿血管周间隙扩散驱动区域特异性帕金森样病理
这对帕金森病为何重要
人们常把帕金森病看作一种运动障碍,以震颤和僵硬为特征。但在这些运动症状出现的多年之前,许多患者就会丧失嗅觉。本研究提出了一个简单却影响深远的问题:浮游在大脑清澈液体中的有毒蛋白,是否可能在嗅觉相关的大脑区域率先诱发疾病,早于运动中枢受累?通过追踪这些蛋白的流向及其在小鼠体内造成的损伤,研究人员发现了一个隐藏的“管道”系统,可能推动帕金森病的逐步进展——并指向一种意想不到的新方法来减缓这种进程。
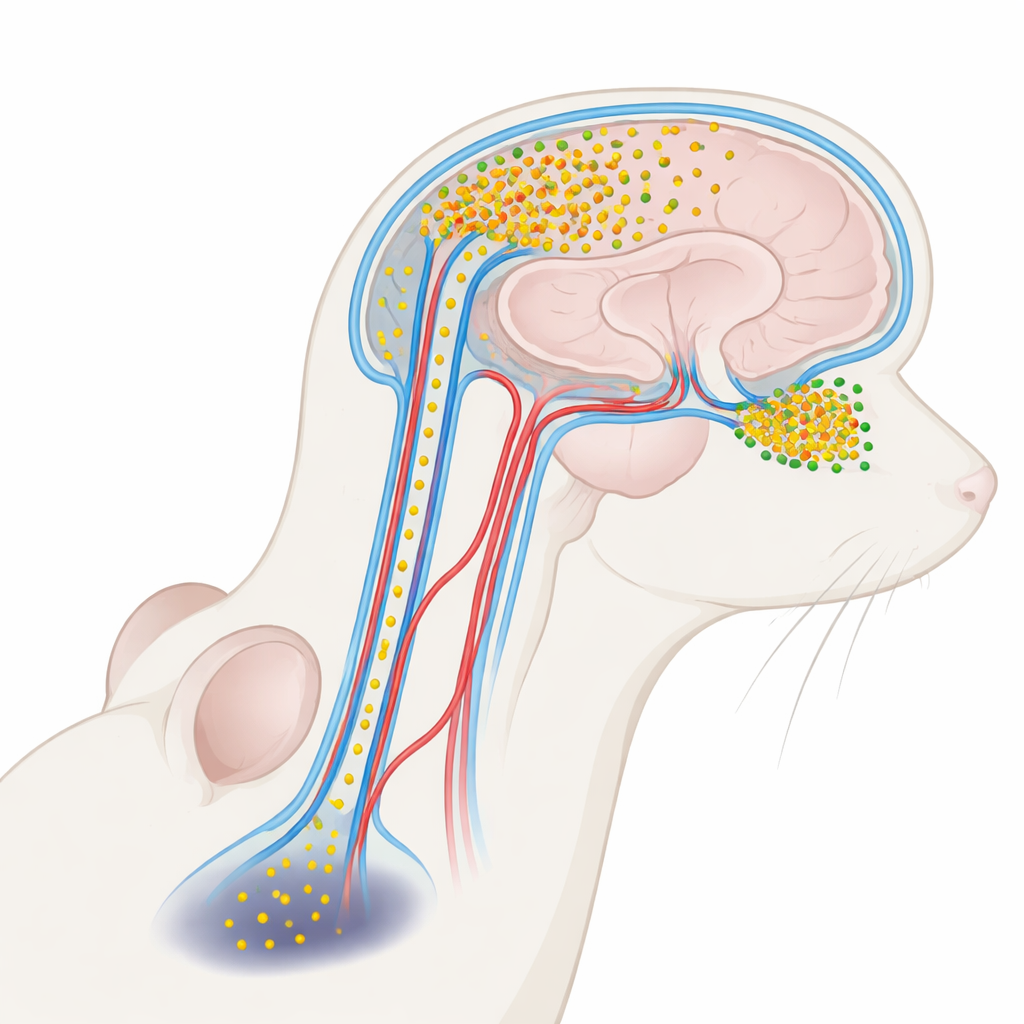
随脑液迁移的有害蛋白
帕金森病与一种称为α‑突触核蛋白的蛋白密切相关。在健康大脑中,它有助于神经元间的通讯。然而在疾病状态下,α‑突触核蛋白可以聚集成小而可溶的簇——寡聚体,这类结构对神经元尤其有毒。帕金森病患者的脑脊液(即浸润脑与脊髓的清澈液体)中,这些寡聚体的水平更高。以往大多数研究将脑脊液中的α‑突触核蛋白视为疾病的有用标志物,而非积极的致病因子。本文作者提出,脑脊液中携带的寡聚体是否会回渗入脑组织并损伤特定区域,从而解释嗅觉问题为何会早于运动问题出现。
大脑的“管道”和易感的嗅觉中枢
脑脊液不仅起缓冲作用;它还沿血管旁的通道循环,这些血管周间隙是更广泛“糖淋巴”清除系统的一部分。研究者用发光标签和先进的三维显微成像,将标记的α‑突触核蛋白注入小鼠的脑脊液并观察其去向。他们发现该蛋白沿着这些血管周路径进入大脑,并呈极不均匀的方式累积。位于大脑前方负责气味处理的嗅球吸收了远多于像黑质这样更深层负责运动的区域的进入蛋白。即便在嗅球内部,某些亚区的流入也比其他区更重,表明局部液体流动和血管布局塑造了精细的易感性。
从无声流入到炎症与神经元丧失
为检验这种流入造成的后果,研究团队向小鼠输注有毒的α‑突触核蛋白寡聚体,并随时间检查其脑组织。在嗅球和黑质中,称为小胶质细胞和星形胶质细胞的免疫支持细胞被激活,炎性分子升高。但这些反应在嗅球中明显更强。在那里,产生多巴胺的神经元——使用与帕金森病相关的相同化学递质的细胞——早期开始死亡,并在数周内持续减少。相比之下,黑质中的多巴胺神经元在更晚期才出现明显的丧失。这种分阶段的损伤与临床表现相呼应:嗅觉回路早期受损,随后才是控制运动的细胞受累。
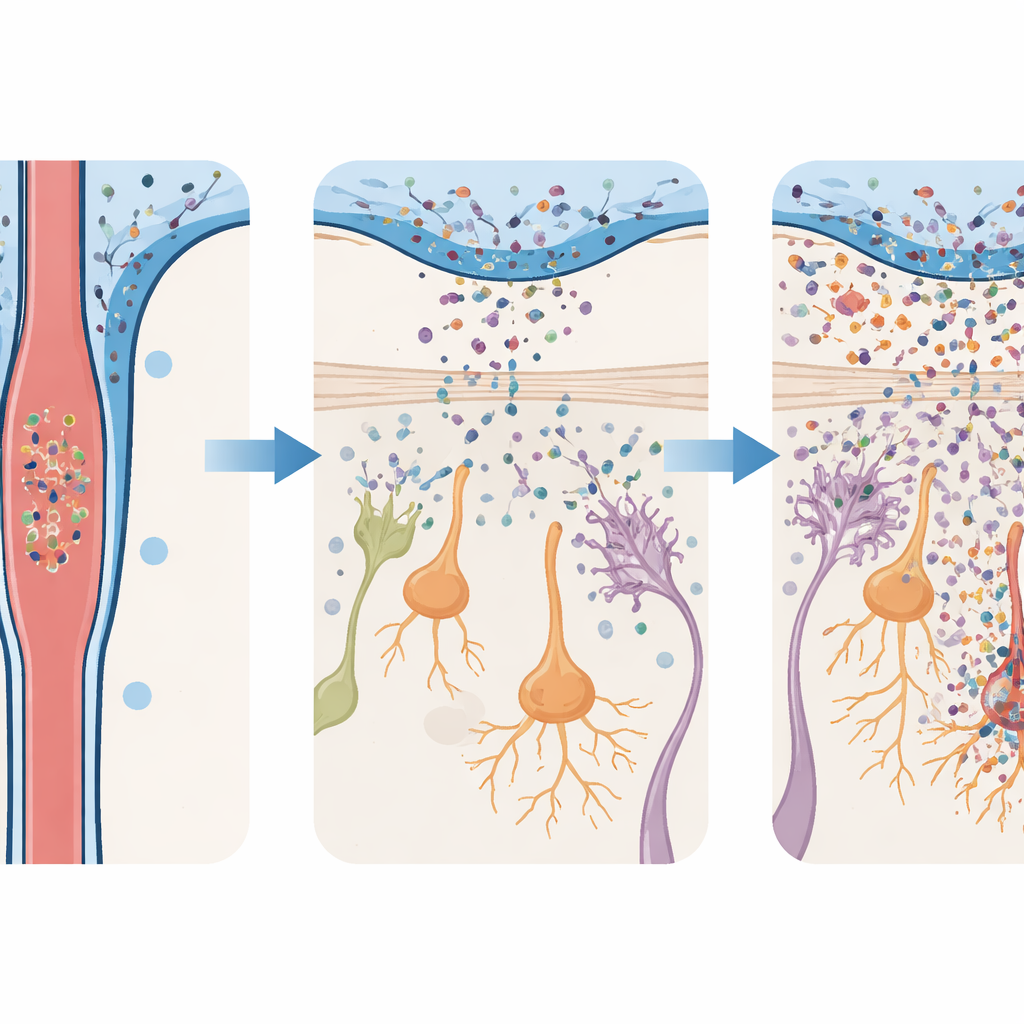
早期嗅觉障碍与晚期运动问题
小鼠的行为变化与细胞损伤的时间线一致。接受α‑突触核蛋白寡聚体注入的动物很快在嗅寻隐藏食物时遇到困难,对诸如雌鼠尿液等吸引气味的兴趣降低,并且不太倾向于回避令人不快的气味。这些基于嗅觉的缺陷在几天内出现,并持续近两个月。然而,同一批小鼠在标准运动测试中如行走、平衡与协调保持正常,直到更晚才出现明显的运动困难。值得注意的是,当研究者降低注入寡聚体的剂量时,嗅球的炎症与神经元丧失明显减少,动物的嗅觉能力总体保持正常。这种剂量依赖性提示,脑脊液中有毒蛋白的负荷直接决定了早期损伤的程度。
对未来治疗的意义
综上所述,这些发现支持一种新的帕金森病观:脑脊液中有毒的α‑突触核蛋白寡聚体不仅是疾病进展的标志——它们通过沿血管周通道回流入脑而主动扩散病变。由于嗅球接收到更大量的此类流入,它较早且更严重地受损,从而解释了嗅觉丧失可在震颤与僵硬出现前多年出现。关键是,这项工作也提示了干预方向:如果我们能安全降低或清除脑脊液中的这些寡聚体——通过过滤装置、靶向抗体或其他“脑脊液清除”策略——就可能保护像嗅球这样易感的区域,减缓帕金森样病理的整个级联过程。
引用: Zhu, WX., He, XZ., Meng, JC. et al. Perivascular spread of CSF-derived α-synuclein oligomers drives region-specific Parkinson’s-like pathology. npj Parkinsons Dis. 12, 84 (2026). https://doi.org/10.1038/s41531-026-01300-3
关键词: 帕金森病, α‑突触核蛋白, 脑脊液, 糖淋巴系统, 嗅觉功能障碍