Clear Sky Science · nl
Perivasculaire verspreiding van CSF-afgeleide α-synucleïne-oligomeren drijft regiogebonden Parkinson-achtige pathologie
Waarom dit belangrijk is voor de ziekte van Parkinson
Mensen zien de ziekte van Parkinson vaak als een bewegingsstoornis, gekenmerkt door tremor en stijfheid. Maar jaren voordat deze motorische problemen zichtbaar worden, verliezen veel patiënten hun reukzin. Deze studie stelt een eenvoudige maar krachtige vraag: zouden toxische eiwitten die in de heldere vloeistof van de hersenen zweven kunnen helpen de ziekte te starten in hersenregio’s die met reuk te maken hebben, lang voordat bewegingscentra worden aangetast? Door te volgen hoe deze eiwitten reizen en welke schade ze veroorzaken bij muizen, onthullen de onderzoekers een verborgen ‘riolering’ die de stapsgewijze progressie van Parkinson kan aandrijven — en wijzen ze op een onverwachte nieuwe manier om die te vertragen.
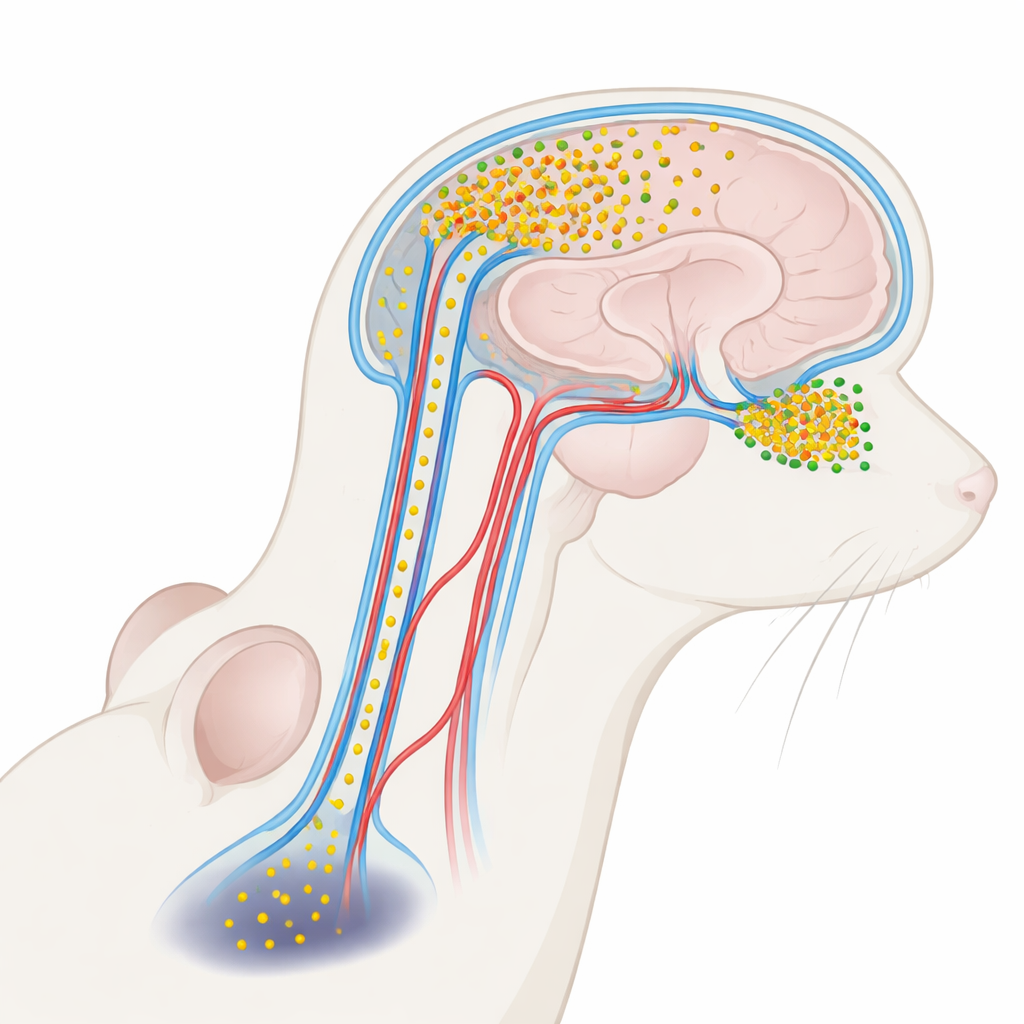
Een schadelijk eiwit dat meereist in hersenvocht
De ziekte van Parkinson wordt sterk geassocieerd met een eiwit dat alfa‑synucleïne heet. In gezonde hersenen helpt het bij de communicatie tussen zenuwcellen. Onder ziekteomstandigheden kan alfa‑synucleïne echter samenklonteren tot kleine oplosbare clusters, oligomeren genoemd, die bijzonder toxisch zijn voor neuronen. Deze oligomeren komen in hogere concentraties voor in de heldere vloeistof die de hersenen en het ruggenmerg omgeeft — het cerebrospinale vocht (CSF) — van mensen met Parkinson. Tot nu toe werd CSF‑alfa‑synucleïne meestal gezien als een nuttige merker van ziekte, niet als een actieve speler. De auteurs van dit artikel vroegen zich af of deze in het CSF aanwezige oligomeren daadwerkelijk terug in de hersenen kunnen sijpelen en specifieke regio’s kunnen beschadigen, wat zou kunnen uitleggen waarom reukproblemen vroeg optreden terwijl bewegingsproblemen later ontstaan.
De ‘riolering’ van de hersenen en een kwetsbaar reukcentrum
CSF dempt de hersenen niet alleen; het circuleert ook door een netwerk van kanalen langs bloedvaten, de perivasculaire ruimtes, onderdeel van een breder “glymfatisch” klaringssysteem. Met behulp van lichtgevende labels en geavanceerde driedimensionale microscopen injecteerden de onderzoekers gelabelde alfa‑synucleïne in het CSF van muizen en volgden waar het heen ging. Ze ontdekten dat het eiwit via deze perivasculaire routes de hersenen binnendrong en zich zeer ongelijkmatig ophoopte. De bulbus olfactorius — de kleine structuur aan de voorkant van de hersenen die geuren verwerkt — nam veel meer van het binnenkomende eiwit op dan diepere regio’s zoals de substantia nigra, die beweging reguleert. Zelfs binnen de bulbus zelf lieten sommige subregio’s een zwaardere instroom zien dan andere, wat wijst op een fijnmazige kwetsbaarheid die wordt bepaald door lokale vloeistofstroming en de indeling van vaten.
Van stille instroom naar ontsteking en neuronverlies
Om te testen wat deze instroom veroorzaakt, infuseerde het team muizen met toxische alfa‑synucleïne‑oligomeren en onderzocht hun hersenen over tijd. In zowel de bulbus olfactorius als de substantia nigra raakten immuun‑ondersteunende cellen, micro‑glia en astrocyten, geactiveerd en namen ontstekingsmoleculen toe. Maar deze reacties waren veel sterker in de bulbus olfactorius. Daar begonnen dopamineproducerende neuronen — cellen die dezelfde neurotransmitter gebruiken die bij Parkinson een rol speelt — vroeg af te sterven en bleven ze wekenlang afnemen. Ter vergelijking: dopamine‑neuronen in de substantia nigra bleven grotendeels intact totdat veel later pas verlies zichtbaar werd. Deze gefaseerde schade weerspiegelt het klinische beeld: vroege problemen in reukcircuits, gevolgd door latere aantasting van cellen die beweging controleren.
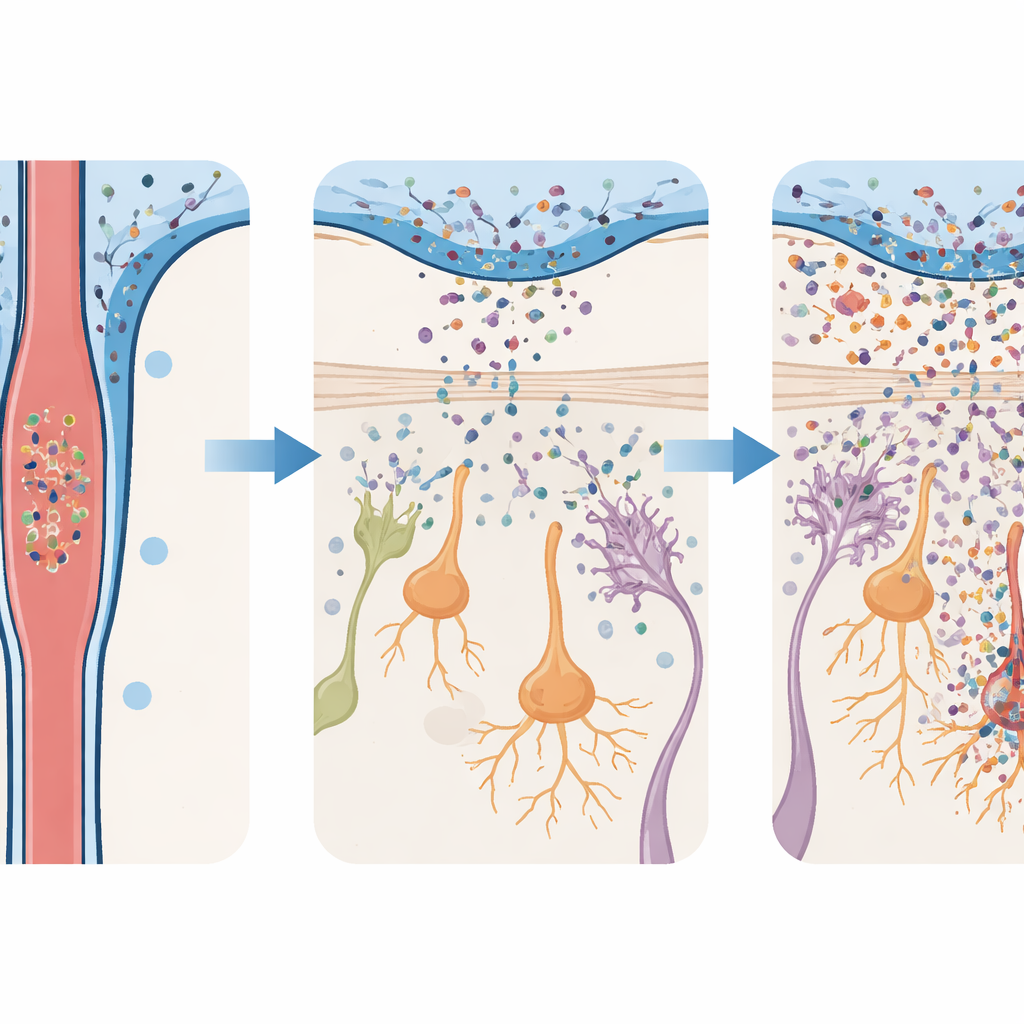
Vroege reukproblemen en latere bewegingsklachten
De gedragsveranderingen bij de muizen volgden hetzelfde tijdspad als de cellulaire schade. Dieren die alfa‑synucleïne‑oligomeren kregen, ontwikkelden snel moeite met het vinden van verborgen voedsel op geur, toonden minder interesse in aantrekkelijke geuren zoals vrouwelijke muizenurine en waren minder geneigd onaangename geuren te vermijden. Deze geurgebaseerde tekorten deden zich binnen enkele dagen voor en hielden bijna twee maanden aan. Toch liepen, balanceerden en coördineerden dezelfde muizen normaal op standaard bewegingsproeven totdat veel later duidelijke motorische problemen verschenen. Belangrijk is dat toen de onderzoekers de toegediende dosis oligomeren verlaagden, de bulbus olfactorius veel minder ontsteking en neuronverlies vertoonde en de dieren grotendeels hun normale reukvermogen behielden. Deze dosisgevoeligheid suggereert dat de hoeveelheid toxisch eiwit in het CSF direct bepaalt hoeveel vroege schade optreedt.
Wat dit betekent voor toekomstige behandelingen
Gezamenlijk ondersteunen de bevindingen een nieuw beeld van de ziekte van Parkinson waarin toxische alfa‑synucleïne‑oligomeren in CSF meer doen dan alleen bestaande schade aangeven — ze verspreiden die actief door terug in de hersenen te vloeien langs perivasculaire kanalen. Omdat de bulbus olfactorius een groter aandeel van deze instroom ontvangt, ondergaat zij eerder en ernstiger schade, wat verklaart waarom verlies van reukzin jaren vóór tremor en stijfheid kan optreden. Cruciaal is dat het werk ook een interventierichting suggereert: als we deze oligomeren veilig uit het CSF kunnen verminderen of verwijderen — via filtratiesystemen, gerichte antilichamen of andere ‘CSF‑reinigende’ strategieën — kunnen we kwetsbare regio’s zoals de bulbus olfactorius mogelijk beschermen en de hele cascade van Parkinson‑achtige pathologie vertragen.
Bronvermelding: Zhu, WX., He, XZ., Meng, JC. et al. Perivascular spread of CSF-derived α-synuclein oligomers drives region-specific Parkinson’s-like pathology. npj Parkinsons Dis. 12, 84 (2026). https://doi.org/10.1038/s41531-026-01300-3
Trefwoorden: Ziekte van Parkinson, alpha-synucleïne, hersenvocht, glymfatisch systeem, reukstoornis