Clear Sky Science · pl
Rozprzestrzenianie się oligomerów α-synukleiny po naczyniach okołonaczyniowych w płynie mózgowo-rdzeniowym napędza regionowo-specyficzną patologię podobną do choroby Parkinsona
Dlaczego to ma znaczenie dla choroby Parkinsona
Ludzie często myślą o chorobie Parkinsona jako o zaburzeniu ruchowym, charakteryzującym się drżeniem i sztywnością. Jednak na wiele lat przed pojawieniem się objawów ruchowych, wielu pacjentów traci węch. To badanie stawia proste, lecz istotne pytanie: czy toksyczne białka unoszące się w przezroczystym płynie otaczającym mózg mogą zapoczątkować chorobę w rejonach mózgu związanych z węchem, na długo zanim zajęte zostaną ośrodki ruchu? Śledząc, jak te białka podróżują i jakie wyrządzają szkody u myszy, badacze odkrywają ukrytą „instalację hydrauliczną”, która może napędzać etapowy rozwój Parkinsona — i wskazują na nieoczekiwany sposób, by go spowolnić.
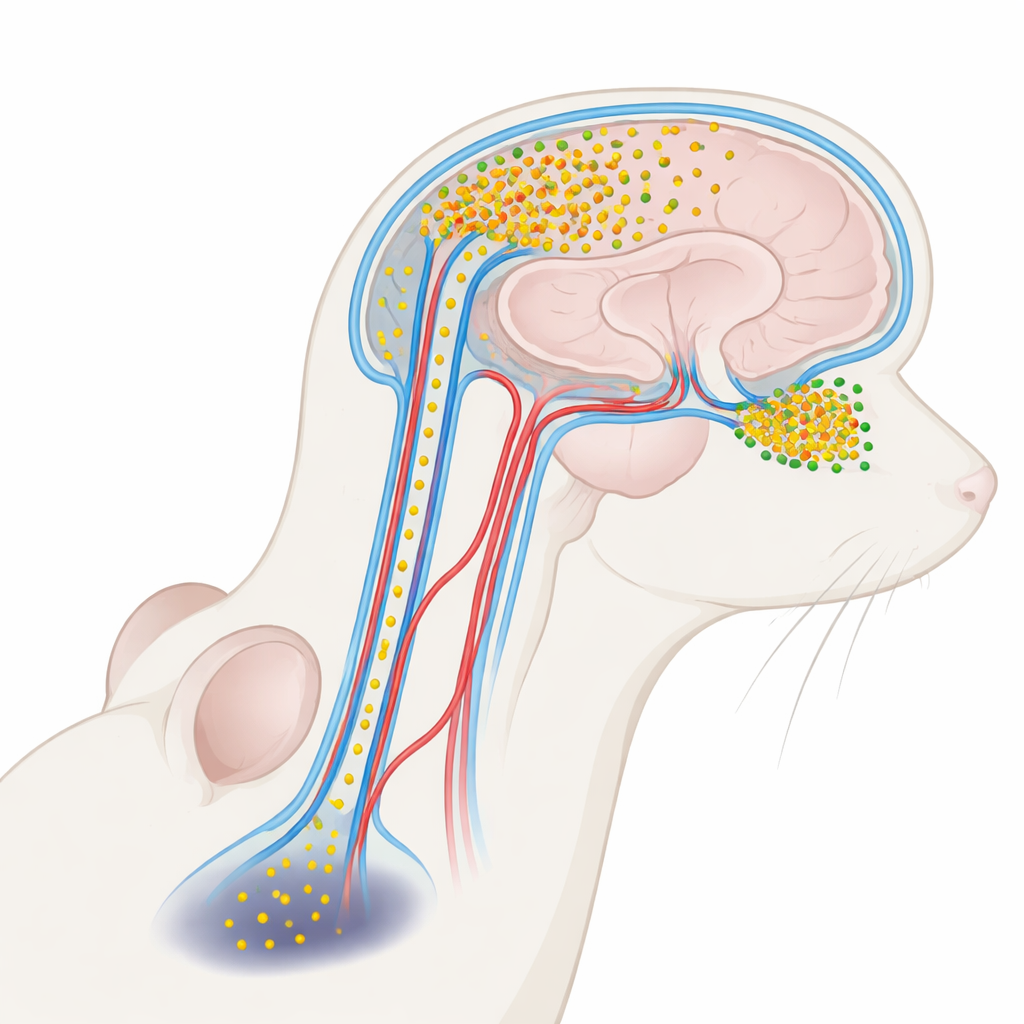
Szkodliwe białko płynące w płynie mózgowym
Choroba Parkinsona jest ściśle związana z białkiem zwanym alfa‑synukleiną. W zdrowym mózgu pomaga ono komórkom nerwowym w komunikacji. W warunkach chorobowych alfa‑synukleina może jednak zlepiać się w małe rozpuszczalne skupiska zwane oligomerami, które są szczególnie toksyczne dla neuronów. Te oligomery występują w wyższych stężeniach w przezroczystym płynie kąpiącym mózg i rdzeń kręgowy — płynie mózgowo‑rdzeniowym (PMR) — u osób z chorobą Parkinsona. Dotychczas większość badań traktowała alfa‑synukleinę w PMR jako użyteczny marker choroby, a nie jako aktywnego sprawcę. Autorzy tej pracy zapytali, czy oligomery znajdujące się w PMR mogą faktycznie przedostawać się z powrotem do mózgu i uszkadzać określone regiony, pomagając wyjaśnić, dlaczego zaburzenia węchu pojawiają się wcześnie, podczas gdy problemy ruchowe występują później.
Hydraulika mózgu i wrażliwe centrum węchowe
PMR nie tylko amortyzuje mózg; krąży także siecią kanałów obok naczyń krwionośnych, znanych jako przestrzenie okołonaczyniowe, będących częścią szerszego systemu oczyszczania „glimfatycznego”. Korzystając z fluorescencyjnych znaczników i zaawansowanych mikroskopów trójwymiarowych, badacze wstrzyknęli znakowaną alfa‑synukleinę do PMR myszy i obserwowali jej losy. Stwierdzili, że białko wchodzi do mózgu wzdłuż tych okołonaczyniowych tras i kumuluje się bardzo nierównomiernie. Opuszka węchowa — niewielka struktura z przodu mózgu przetwarzająca zapachy — chłonęła znacznie więcej napływającego białka niż głębsze rejony, takie jak istota czarna, która kontroluje ruch. Nawet w samej opuszce węchowej niektóre podregiony wykazywały większy napływ niż inne, co sugeruje drobną podatność uwarunkowaną lokalnym przepływem płynu i układem naczyń.
Od cichego napływu do stanu zapalnego i utraty neuronów
Aby sprawdzić, co powoduje ten napływ, zespół wprowadził myszom toksyczne oligomery alfa‑synukleiny i badał ich mózgi w czasie. Zarówno w opuszce węchowej, jak i w istocie czarnej, komórki wsparcia immunologicznego zwane mikroglejem i astrocytami uległy aktywacji, a poziomy cząsteczek zapalnych wzrosły. Reakcje te były jednak znacznie silniejsze w opuszce węchowej. Tam neurony produkujące dopaminę — komórki wykorzystujące ten sam neuroprzekaźnik zaangażowany w chorobę Parkinsona — zaczęły umierać wcześnie i ich liczba nadal spadała przez tygodnie. W przeciwieństwie do tego, neurony dopaminergiczne w istocie czarnej pozostawały w dużej mierze nienaruszone aż do znacznie późniejszego momentu, gdy straty w końcu się pojawiły. To stopniowe uszkodzenie odzwierciedla obraz kliniczny: wczesne zaburzenia w obwodach węchowych, a następnie późniejsze uszkodzenie komórek kontrolujących ruch.
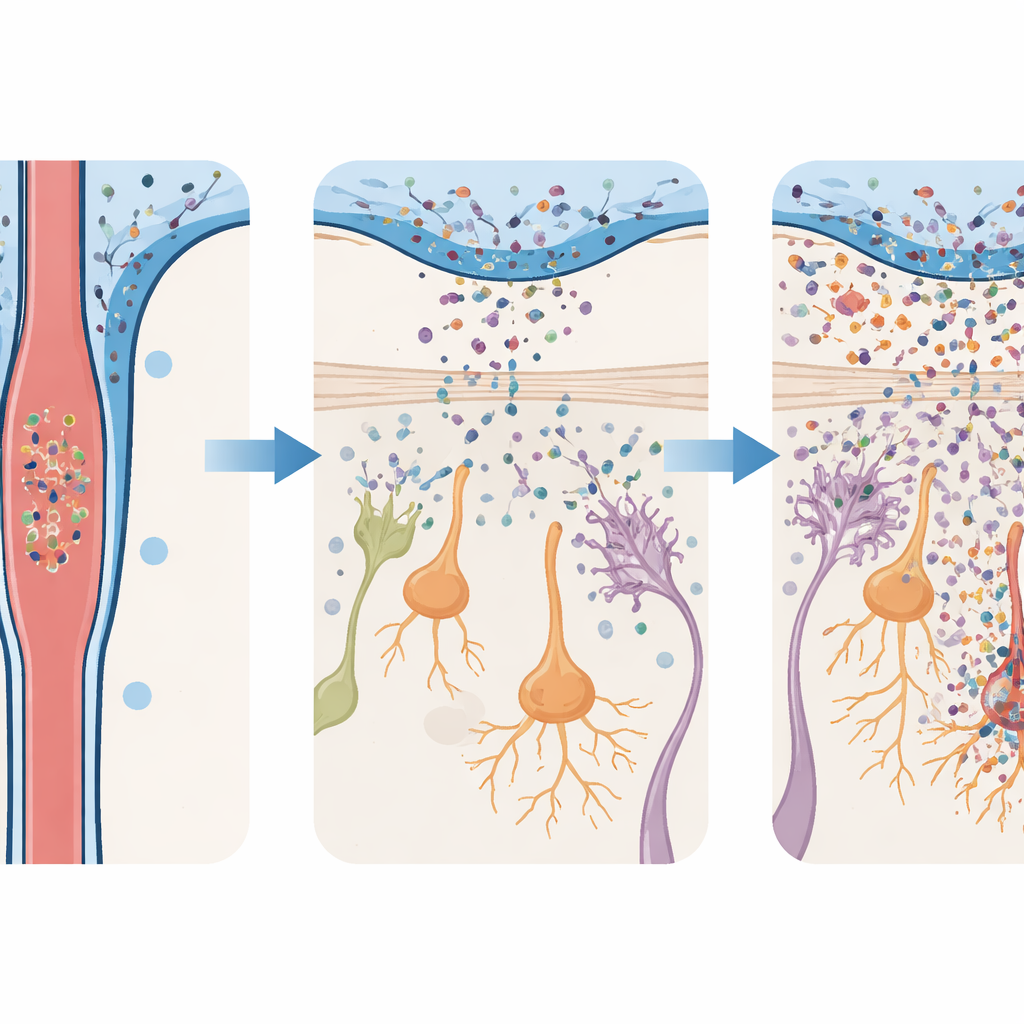
Wczesne problemy z węchem i późne zaburzenia ruchowe
Zmiany behawioralne u myszy przebiegały zgodnie z tym samym harmonogramem co uszkodzenia komórkowe. Zwierzęta otrzymujące oligomery alfa‑synukleiny szybko miały problemy ze znajdowaniem ukrytego jedzenia węchem, wykazywały mniejsze zainteresowanie przyciągającymi zapachami, takimi jak mocz myszy samicy, i rzadziej unikały nieprzyjemnych zapachów. Zaburzenia węchowe pojawiały się w ciągu kilku dni i utrzymywały przez prawie dwa miesiące. Tymczasem te same myszy normalnie chodziły, utrzymywały równowagę i koordynację w standardowych testach ruchowych aż do znacznie późniejszego etapu, kiedy pojawiły się wyraźne trudności motoryczne. Co ważne, gdy badacze obniżyli dawkę wstrzykniętych oligomerów, opuszka węchowa wykazywała znacznie mniejsze zapalenie i utratę neuronów, a zwierzęta w dużej mierze zachowywały prawidłowy węch. Ta zależność od dawki sugeruje, że obciążenie toksycznego białka w PMR bezpośrednio kształtuje, ile wczesnych uszkodzeń występuje.
Co to oznacza dla przyszłych terapii
W sumie wyniki wspierają nową wizję choroby Parkinsona, w której toksyczne oligomery alfa‑synukleiny w PMR robią więcej niż jedynie sygnalizują trwające uszkodzenia — aktywnie je rozprzestrzeniając przez cofanie się do mózgu wzdłuż kanałów okołonaczyniowych. Ponieważ opuszka węchowa otrzymuje silniejszą część tego napływu, ponosi wcześniejsze i cięższe uszkodzenia, co wyjaśnia, dlaczego utrata węchu może poprzedzać drżenie i sztywność o wiele lat. Co kluczowe, praca ta sugeruje także interwencję: jeśli uda się bezpiecznie zmniejszyć lub usunąć te oligomery z PMR — poprzez urządzenia filtrujące, ukierunkowane przeciwciała lub inne strategie „oczyszczania PMR” — możemy chronić wrażliwe regiony, takie jak opuszka węchowa, i spowolnić cały kaskadę patologii podobnej do Parkinsona.
Cytowanie: Zhu, WX., He, XZ., Meng, JC. et al. Perivascular spread of CSF-derived α-synuclein oligomers drives region-specific Parkinson’s-like pathology. npj Parkinsons Dis. 12, 84 (2026). https://doi.org/10.1038/s41531-026-01300-3
Słowa kluczowe: choroba Parkinsona, alfa-synukleina, płyn mózgowo-rdzeniowy, układ glimfatyczny, zaburzenia węchu