Clear Sky Science · es
La propagación perivascular de oligómeros de α‑sinucleína derivados del LCR impulsa una patología tipo Parkinson específica por región
Por qué importa para la enfermedad de Parkinson
La gente suele pensar en la enfermedad de Parkinson como un trastorno del movimiento, caracterizado por temblor y rigidez. Pero años antes de que aparezcan esos problemas motores, muchos pacientes pierden el sentido del olfato. Este estudio plantea una pregunta sencilla pero potente: ¿podrían proteínas tóxicas flotando en el claro líquido que baña el cerebro iniciar la enfermedad en regiones relacionadas con el olfato mucho antes de que se afecten los centros del movimiento? Al trazar cómo viajan estas proteínas y qué daño causan en ratones, los investigadores descubren una tubería oculta que puede impulsar la progresión escalonada del Parkinson, y señalan una vía inesperada para frenarla.
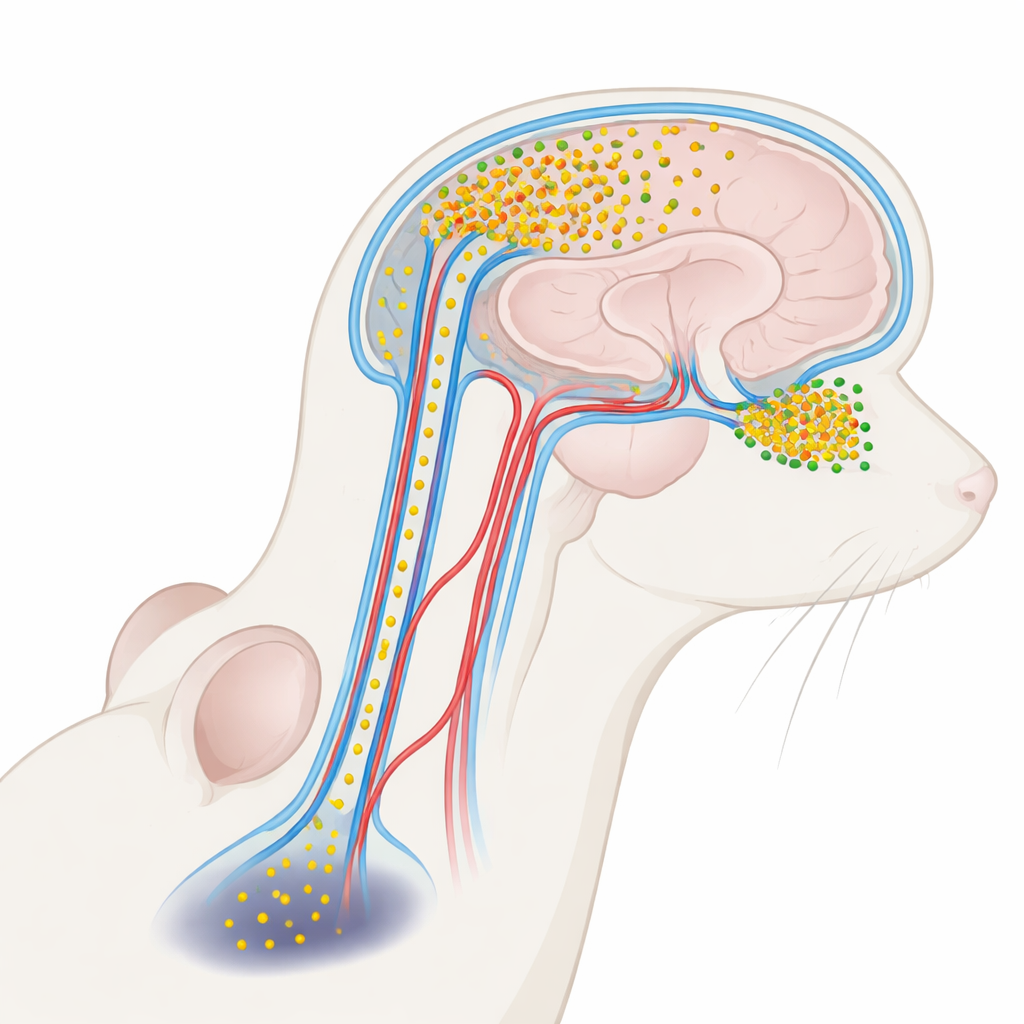
Una proteína dañina transportada en el líquido cerebral
La enfermedad de Parkinson está estrechamente ligada a una proteína llamada alfa‑sinucleína. En cerebros sanos, ayuda a las neuronas a comunicarse. Bajo condiciones de enfermedad, sin embargo, la alfa‑sinucleína puede agregarse en pequeños racimos solubles llamados oligómeros que son especialmente tóxicos para las neuronas. Estos oligómeros aparecen en niveles más altos en el claro líquido que baña el cerebro y la médula espinal—el líquido cefalorraquídeo, o LCR—de personas con Parkinson. Hasta ahora, la mayoría de los trabajos trataban la alfa‑sinucleína en LCR como un marcador útil de la enfermedad, no como un actor activo. Los autores de este artículo se preguntaron si estos oligómeros transportados por el LCR podrían en realidad filtrarse de nuevo al cerebro y lesionar regiones específicas, ayudando a explicar por qué los problemas olfativos aparecen temprano mientras los problemas motores emergen más tarde.
La plomería del cerebro y un centro olfativo vulnerable
El LCR no solo amortigua el cerebro; circula a través de una red de canales junto a los vasos sanguíneos conocidos como espacios perivasculares, parte de un sistema de aclaramiento más amplio «glinfático». Usando etiquetas fluorescentes y microscopios tridimensionales avanzados, los investigadores inyectaron alfa‑sinucleína marcada en el LCR de ratones y observaron a dónde iba. Encontraron que la proteína entraba en el cerebro a lo largo de estas rutas perivasculares y se acumulaba de forma muy desigual. El bulbo olfatorio—la pequeña estructura en la parte frontal del cerebro que procesa los olores—absorbe mucho más de la proteína entrante que regiones más profundas como la sustancia negra, que controla el movimiento. Incluso dentro del propio bulbo olfatorio, algunas subregiones mostraron una mayor afluencia que otras, lo que sugiere una vulnerabilidad de grano fino modelada por el flujo local de líquido y la disposición de los vasos.
De una afluencia silenciosa a la inflamación y la pérdida neuronal
Para probar qué provoca esta afluencia, el equipo infundió en ratones oligómeros tóxicos de alfa‑sinucleína y examinó sus cerebros con el tiempo. Tanto en el bulbo olfatorio como en la sustancia negra, las células de soporte inmunitario llamadas microglía y astroglía se activaron, y aumentaron las moléculas inflamatorias. Pero estas reacciones fueron mucho más intensas en el bulbo olfatorio. Allí, las neuronas productoras de dopamina—células que utilizan el mismo mensajero químico implicado en el Parkinson—comenzaron a morir temprano y continuaron disminuyendo durante semanas. En contraste, las neuronas dopaminérgicas de la sustancia negra permanecieron en gran parte intactas hasta mucho más tarde, cuando finalmente aparecieron pérdidas. Este daño escalonado refleja el panorama clínico: problemas tempranos en el circuito olfativo, seguidos de una lesión posterior en las células que controlan el movimiento.
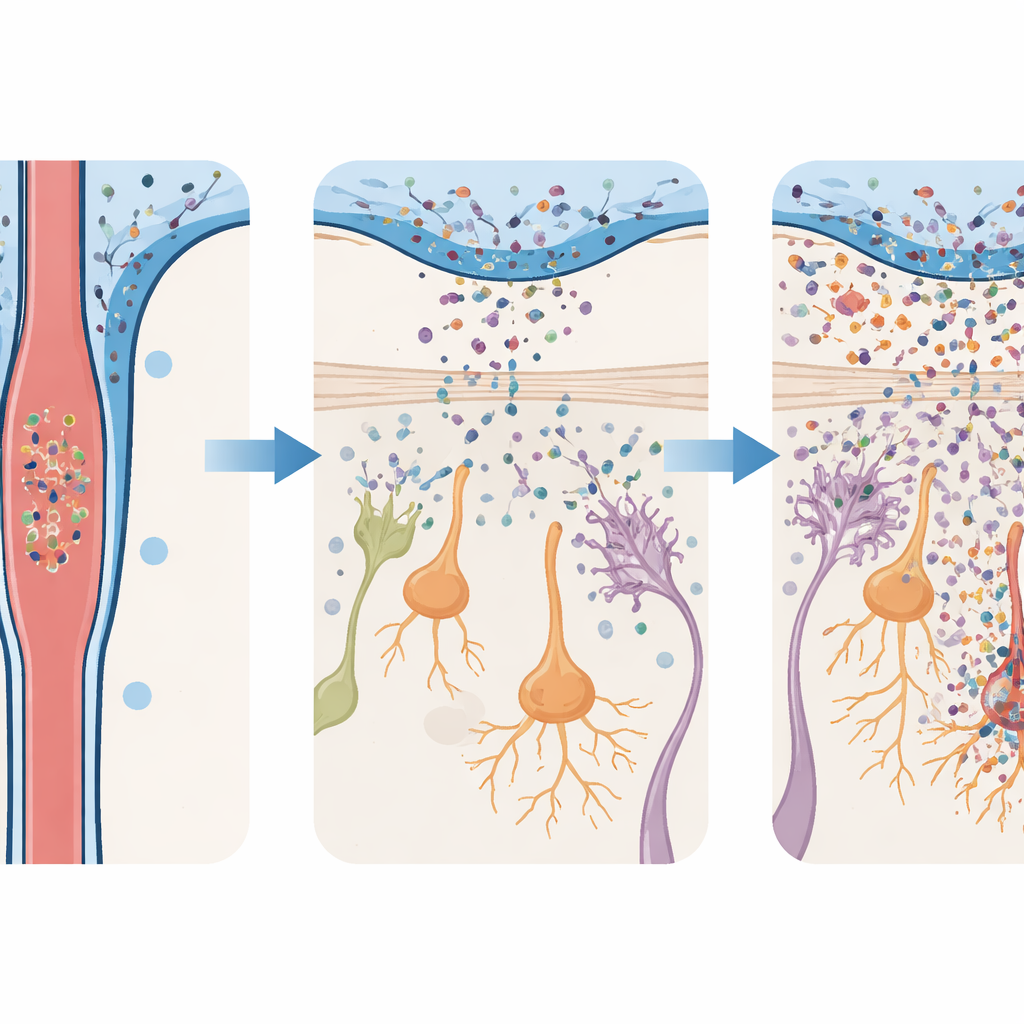
Problemas olfativos tempranos y dificultades de movimiento tardías
Los cambios conductuales en los ratones siguieron la misma cronología que el daño celular. Los animales a los que se administraron oligómeros de alfa‑sinucleína desarrollaron rápidamente dificultades para encontrar comida oculta por el olor, mostraron menos interés por olores atractivos como la orina de hembras, y se mostraron menos inclinados a evitar olores desagradables. Estos déficits basados en el olfato aparecieron en días y persistieron casi dos meses. Sin embargo, los mismos ratones caminaron, se equilibraron y coordinaron con normalidad en pruebas estándar de movimiento hasta mucho más tarde, cuando finalmente surgieron dificultades motoras evidentes. Es importante que, cuando los investigadores redujeron la dosis de oligómeros inyectados, el bulbo olfatorio mostró mucha menos inflamación y pérdida neuronal, y los animales conservaron en gran medida la capacidad olfativa normal. Esta sensibilidad a la dosis sugiere que la carga de proteína tóxica en el LCR modela directamente cuánta lesión temprana ocurre.
Qué significa esto para tratamientos futuros
En conjunto, los hallazgos respaldan una nueva visión de la enfermedad de Parkinson en la que los oligómeros tóxicos de alfa‑sinucleína en el LCR hacen más que señalizar daño en curso: lo propagan activamente al fluir de nuevo hacia el cerebro a lo largo de canales perivasculares. Dado que el bulbo olfatorio recibe una parte más fuerte de esta afluencia, sufre una lesión más temprana y severa, lo que explica por qué la pérdida del olfato puede preceder al temblor y la rigidez por años. De forma crucial, el trabajo también sugiere una intervención: si podemos reducir o eliminar de forma segura estos oligómeros del LCR—mediante dispositivos de filtración, anticuerpos dirigidos u otras estrategias de «limpieza del LCR»—podríamos proteger regiones vulnerables como el bulbo olfatorio y frenar toda la cascada de la patología tipo Parkinson.
Cita: Zhu, WX., He, XZ., Meng, JC. et al. Perivascular spread of CSF-derived α-synuclein oligomers drives region-specific Parkinson’s-like pathology. npj Parkinsons Dis. 12, 84 (2026). https://doi.org/10.1038/s41531-026-01300-3
Palabras clave: Enfermedad de Parkinson, alfa‑sinucleína, líquido cefalorraquídeo, sistema glinfático, disfunción olfativa