Clear Sky Science · tr
BOS kaynaklı α-sinüklein oligomerlerinin perivasküler yayılımı bölgeye özgü Parkinson benzeri patolojiyi tetikliyor
Parkinson hastalığı açısından neden önemli
İnsanlar genellikle Parkinson hastalığını titreme ve sertlik ile karakterize bir hareket bozukluğu olarak düşünürler. Ancak bu motor sorunlar ortaya çıkmadan yıllar önce birçok hasta koku alma duyusunu kaybeder. Bu çalışma basit ama güçlü bir soruyu gündeme getiriyor: Beyni yıkayan şeffaf sıvıda yüzen toksik proteinler, hareket merkezleri etkilenmeden çok önce hastalığı koku ile ilgili beyin bölgelerinde başlatıyor olabilir mi? Araştırmacılar bu proteinlerin nasıl yol aldığını ve farelerde ne tür hasara yol açtığını izleyerek, Parkinson ilerleyişini adım adım tetikliyor olabilecek gizli bir sıvı dağıtım sistemini ortaya çıkarıyor ve ilerlemeyi yavaşlatmaya yönelik beklenmedik bir yol işaret ediyorlar.
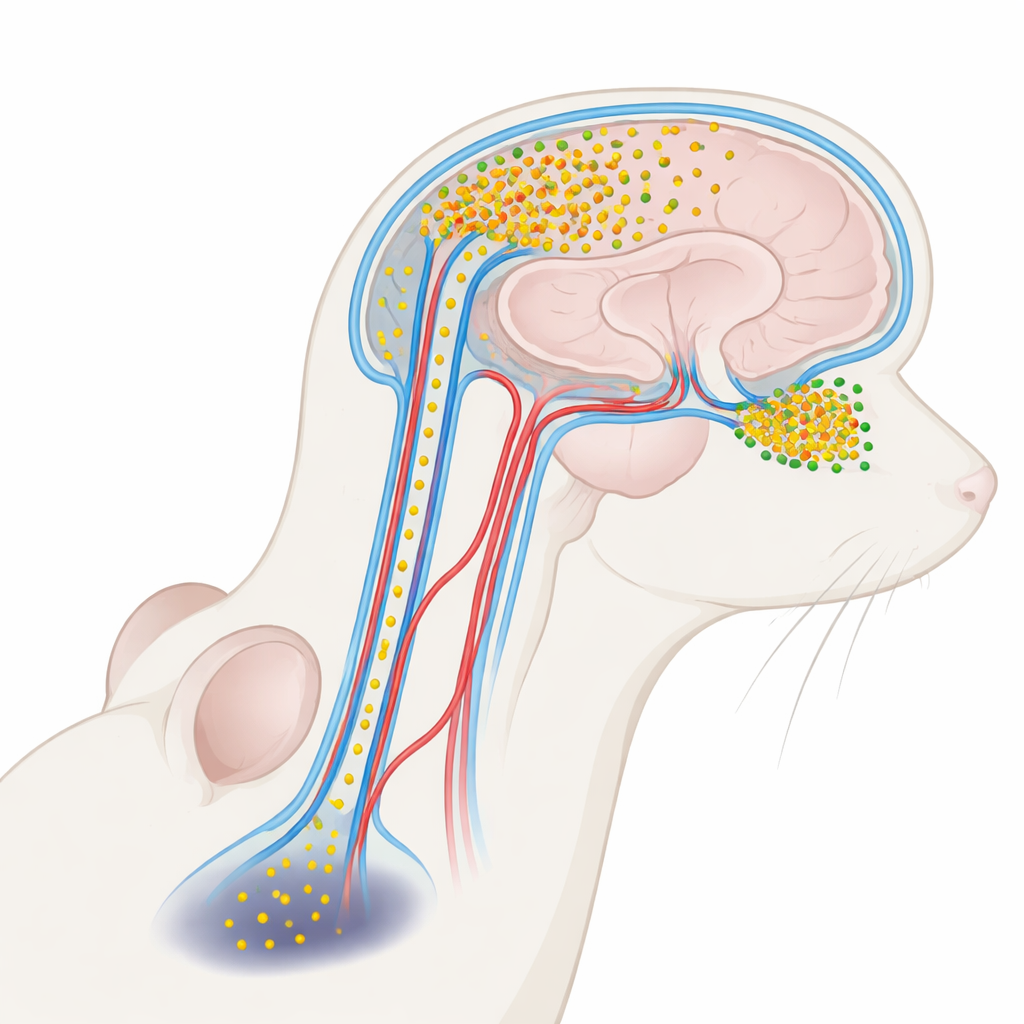
Beyin sıvısında sürüklenen zararlı bir protein
Parkinson hastalığı alfa‑sinüklein adlı bir proteinle yakından ilişkilidir. Sağlıklı beyinlerde bu protein sinir hücrelerinin iletişim kurmasına yardımcı olur. Ancak hastalık koşullarında alfa‑sinüklein, nöronlar için özellikle toksik olan küçük çözünebilir kümeler olan oligomerler halinde toplanabilir. Bu oligomerler, Parkinson hastalarının beyin ve omuriliği yıkayan şeffaf sıvı olan beyin-omurilik sıvısında (BOS) daha yüksek düzeylerde görülür. Şimdiye dek çoğu çalışma BOS alfa‑sinükleini hastalığın yararlı bir belirteci olarak ele aldı, etkin bir etken olarak değil. Bu makalenin yazarları, BOS kaynaklı bu oligomerlerin gerçekten beyine sızıp belirli bölgeleri incitebileceğini ve koku sorunlarının erken ortaya çıkmasını, hareket sorunlarının ise daha sonra görülmesini açıklamaya yardımcı olup olmayacağını sordular.
Beyninin sıhhi tesisatı ve hassas bir koku merkezi
BOS yalnızca beyni korumakla kalmaz; perivasküler boşluklar olarak bilinen kan damarları boyunca uzanan kanallar ağı üzerinden dolaşır; bu ağ daha geniş bir “glimfatik” temizleme sisteminin parçasıdır. Parlak işaretçiler ve gelişmiş üç boyutlu mikroskoplar kullanarak araştırmacılar etiketli alfa‑sinükleini farelerin BOS’una enjekte etti ve nereye gittiğini izledi. Proteinin perivasküler yollar boyunca beyne girdiğini ve çok düzensiz bir şekilde biriktiğini buldular. Kokunun işlendiği beynin ön kısmındaki küçük yapı olan koku soğanı, hareketi kontrol eden substantia nigra gibi daha derin bölgelerden çok daha fazla proteini emdi. Koku soğanı içinde bile bazı alt bölgeler diğerlerinden daha yoğun giriş gösterdi; bu da yerel sıvı akışı ve damar düzeni tarafından şekillendirilen ince ölçekli bir hassasiyet olduğunu düşündürüyor.
Sessiz girişten iltihaplanma ve nöron kaybına
Bu girişin ne yaptığına bakmak için ekip farelere toksik alfa‑sinüklein oligomerleri verdi ve beyinlerini zaman içinde inceledi. Hem koku soğanında hem de substantia nigrada mikroglia ve astrosit adı verilen bağışıklık destek hücreleri aktive oldu ve iltihap molekülleri arttı. Ancak bu reaksiyonlar koku soğanında çok daha güçlüydü. Burada dopamin üreten nöronlar—Parkinson’da rol oynayan aynı kimyasal haberciyi kullanan hücreler—erken dönemde ölmeye başladı ve haftalar boyunca azalmaya devam etti. Buna karşılık, substantia nigradaki dopamin nöronları çok daha sonra kayıplar ortaya çıkana kadar büyük ölçüde sağlam kaldı. Bu aşamalı hasar klinik tabloyu yansıtıyor: ilk olarak koku devresinde sorunlar, ardından hareketi kontrol eden hücrelere daha geç zarar.
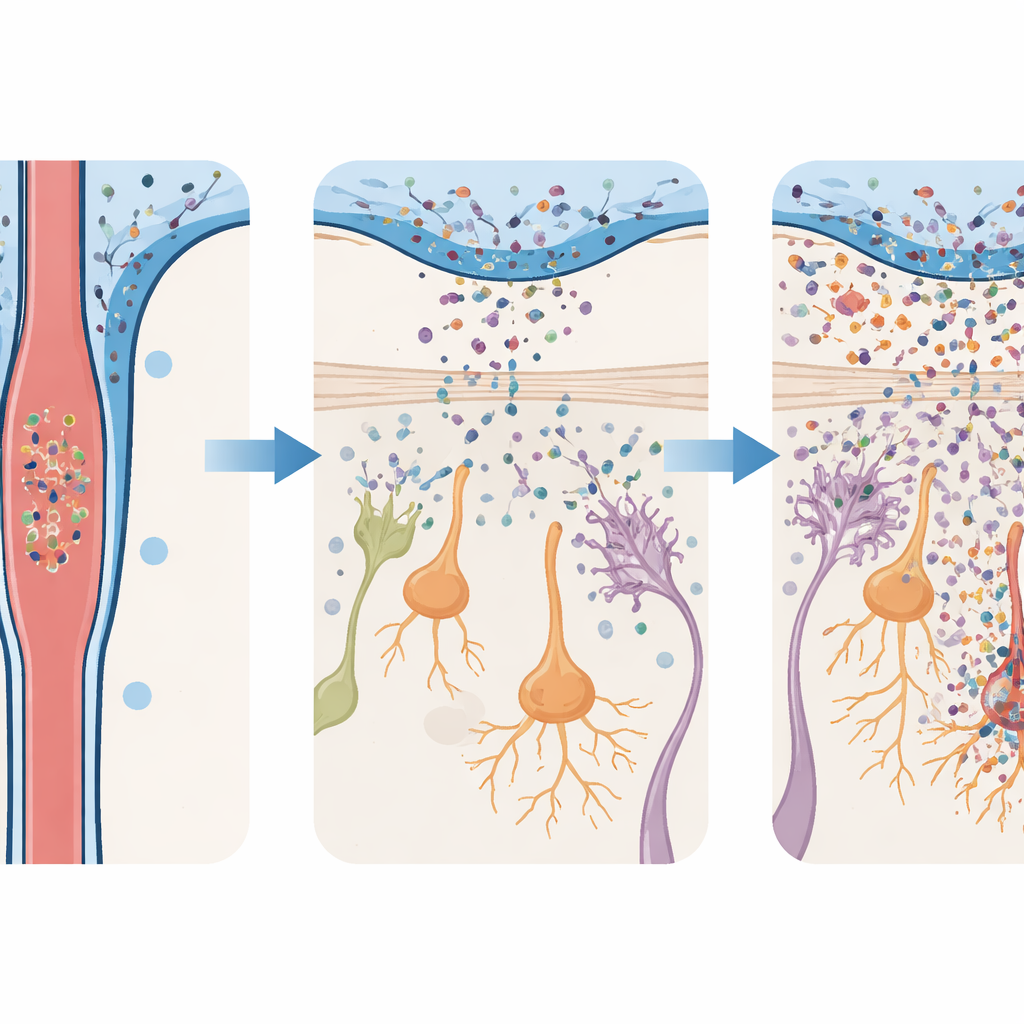
Erken koku sorunları ve geç ortaya çıkan hareket problemleri
Farelerdeki davranış değişiklikleri hücresel hasarla aynı zaman çizelgesini izledi. Alfa‑sinüklein oligomerleri verilen hayvanlar hızla saklı yiyeceği koku ile bulmada zorluk yaşamaya başladı, dişi fare idrarı gibi çekici kokulara daha az ilgi gösterdi ve hoş olmayan kokulardan kaçınma eğilimleri azaldı. Bu kokuya dayalı yetersizlikler günler içinde ortaya çıktı ve neredeyse iki ay sürdü. Oysa aynı fareler standart hareket testlerinde yürüyüş, denge ve koordinasyon açısından çok daha sonra net motor zorluklar ortaya çıkana kadar normal kaldı. Önemli olarak, araştırmacılar enjekte edilen oligomer dozunu düşürdüklerinde koku soğanında daha az iltihap ve nöron kaybı görüldü ve hayvanlar büyük ölçüde normal koku yeteneğini korudu. Bu doz‑duyarlılığı, BOS’taki toksik protein yükünün erken dönemde ne kadar hasar oluşacağını doğrudan şekillendirdiğini öne sürüyor.
Gelecekteki tedaviler için anlamı
Birlikte ele alındığında bulgular, BOS’taki toksik alfa‑sinüklein oligomerlerinin yalnızca devam eden hasarın bir göstergesi olmakla kalmayıp—perivasküler kanallar boyunca geri akarak beyne yaydığı ve böylece hasarı ilerlettiği—yeni bir Parkinson görüşünü destekliyor. Koku soğanı bu girişin daha güçlü bir payını aldığı için daha erken ve daha şiddetli zarar görüyor; bu da koku kaybının titreme ve sertlikten yıllar önce ortaya çıkabilmesini açıklıyor. Hayati olarak, çalışma bir müdahale olasılığını da ima ediyor: Eğer bu oligomerleri BOS’tan güvenli bir şekilde azaltabilir veya temizleyebilirsek—filtrasyon cihazları, hedefe yönelik antikorlar veya diğer “BOS temizleme” stratejileri aracılığıyla—koku soğanı gibi hassas bölgeleri koruyabilir ve Parkinson benzeri patolojinin tüm kaskadını yavaşlatabiliriz.
Atıf: Zhu, WX., He, XZ., Meng, JC. et al. Perivascular spread of CSF-derived α-synuclein oligomers drives region-specific Parkinson’s-like pathology. npj Parkinsons Dis. 12, 84 (2026). https://doi.org/10.1038/s41531-026-01300-3
Anahtar kelimeler: Parkinson hastalığı, alfa-sinüklein, beyin-omurilik sıvısı, glimfatik sistem, koku bozukluğu