Clear Sky Science · he
התפשטות פרי-וסקולרית של אוליגומרים של α‑סינוקלאין הנובעים מנוזל המוח והשדרה מייצרת פתולוגיה שדומה לפרקינסון באזורים ספציפיים
מדוע זה חשוב למחלת פרקינסון
הרבה אנשים מחשיבים את מחלת פרקינסון כהפרעה בתנועה, המתאפיינת ברעידות ונוקשות. אבל שנים לפני שמופיעים ההפרעות המוטוריות הללו, מטופלים רבים מאבדים את חוש הריח. המחקר שואל שאלה פשוטה אך משמעותית: האם חלבונים רעילים הצפים בנוזל הרחצה של המוח עלולים להפעיל את המחלה באזורים במוח הקשורים לריח, זמן רב לפני שמרכזי התנועה נפגעים? על ידי סימון המולקולות הללו ומעקב אחר מסלולי נסיעתן והנזקים שהן גורמות בעכברים, החוקרים חושפים מערכת צינורות סמויה שעשויה להניע את התקדמות מחלת פרקינסון בשלבים — ומצביעים על דרך בלתי צפויה להאטתה.
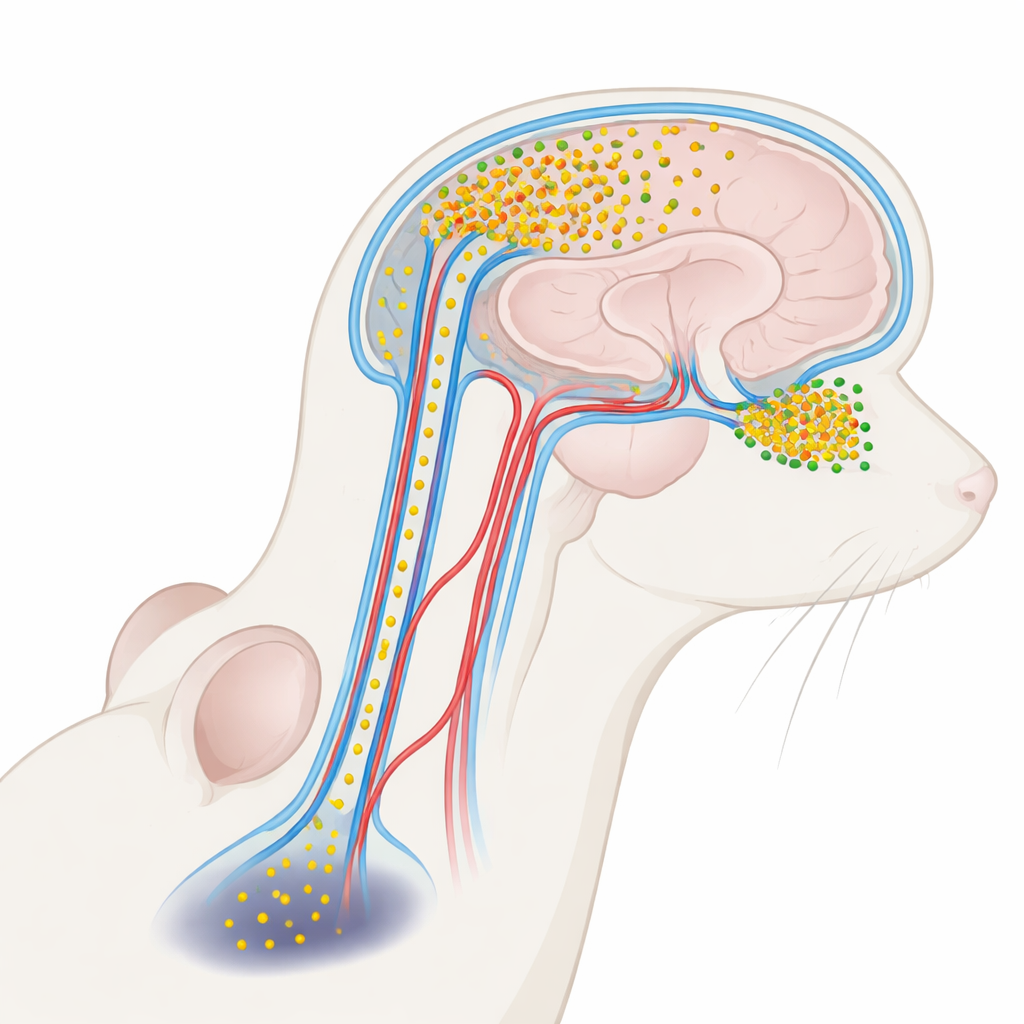
חלבון מזיק הנוסע בנוזל המוח
מחלת פרקינסון קשורה קשר הדוק לחלבון שנקרא אלפא‑סינוקלאין. במוח בריא הוא מסייע לתאי עצב לתקשר. תחת תנאי מחלה, עם זאת, אלפא‑סינוקלאין יכול להתאגד לצברי מולקולות קטנים וממסיסים הנקראים אוליגומרים, שהם רעילים במיוחד לנוירונים. אוליגומרים אלה מופיעים ברמות גבוהות יותר בנוזל הצלול המרחץ את המוח ואת חוט השדרה — נוזל המוח־שדרה (CSF) — של אנשים עם פרקינסון. עד כה רוב המחקרים ראו באלפא‑סינוקלאין ב‑CSF אינדיקטור שימושי למחלה, לא כשחקן פעיל. מחברי המאמר שאלו האם אוליגומרים הנשאים ב‑CSF עלולים למעשה להיספג חזרה אל תוך המוח ולפגוע באזורים מסוימים, וכך להסביר מדוע בעיות ריח מופיעות מוקדם בעוד בעיות תנועה מאחרות מופיעות מאוחר יותר.
צנרת המוח ומרכז ריח רגיש
נוזל ה‑CSF לא רק מרפד את המוח; הוא גם זורם ברשת של תעלות לאורך כלי דם, הידועות כמקומות פרי‑וסקולריים, כחלק ממערכת ניקוז רחבה יותר — מערכת הגלימפה. בעזרת תיוג זוהר ומיקרוסקופים תלת‑ממדיים מתקדמים, החוקרים הזריקו אלפא‑סינוקלאין מסומן ל‑CSF של עכברים וצפינו לאן הוא מגיע. הם מצאו שהחלבון נכנס למוח דרך מסלולים פרי‑וסקולריים והצטבר באופן לא אחיד. בלבלב הריח — המבנה הקטן בקדמת המוח שעובד ריחות — נספג הרבה יותר מהחלבון הנכנס מאשר אזורים עמוקים יותר כמו הסובסטנסיה ניגרה, האחראית על תנועה. אפילו בתוך בלבלב הריח עצמו, תתי‑איזורים מסוימים הראו חדירה כבדה יותר מאחרים, מה שמרמז על פגיעות מדורגת המושפעת ממסלולי הזרימה המקומיים ופריסת כלי הדם.
מחדירה שקטה לדלקת ואובדן נוירונים
כדי לבדוק מה גורמת חדירת החלבון, הצוות החליק עכברים באוליגומרים רעילים של אלפא‑סינוקלאין ובחן את מוחם לאורך זמן. הן בבלבלב הריח והן בסובסטנסיה ניגרה, תאי תמיכה חיסוניים הנקראים מיקרוגליה ואסטרוציטים הופעלו, ורמות מולקולות דלקת עלו. אבל התגובות הללו היו חזקות הרבה יותר בבלבלב הריח. שם, תאי דופמין — תאים המייצרים את המוליך הכימי המעורב בפרקינסון — החלו למות מוקדם והמשיכו להידרדר במשך שבועות. לעומת זאת, תאי הדופמין בסובסטנסיה ניגרה נותרו ברובם שלמים עד מאוחר יותר, כאשר אובדנים הופיעו בסופו של דבר. דפוס הנזק המובנה הזה משקף את התמונה הקלינית: בעיות ראשוניות במעגלי הריח, ואחריהן פגיעה מאוחרת בתאים השולטים בתנועה.
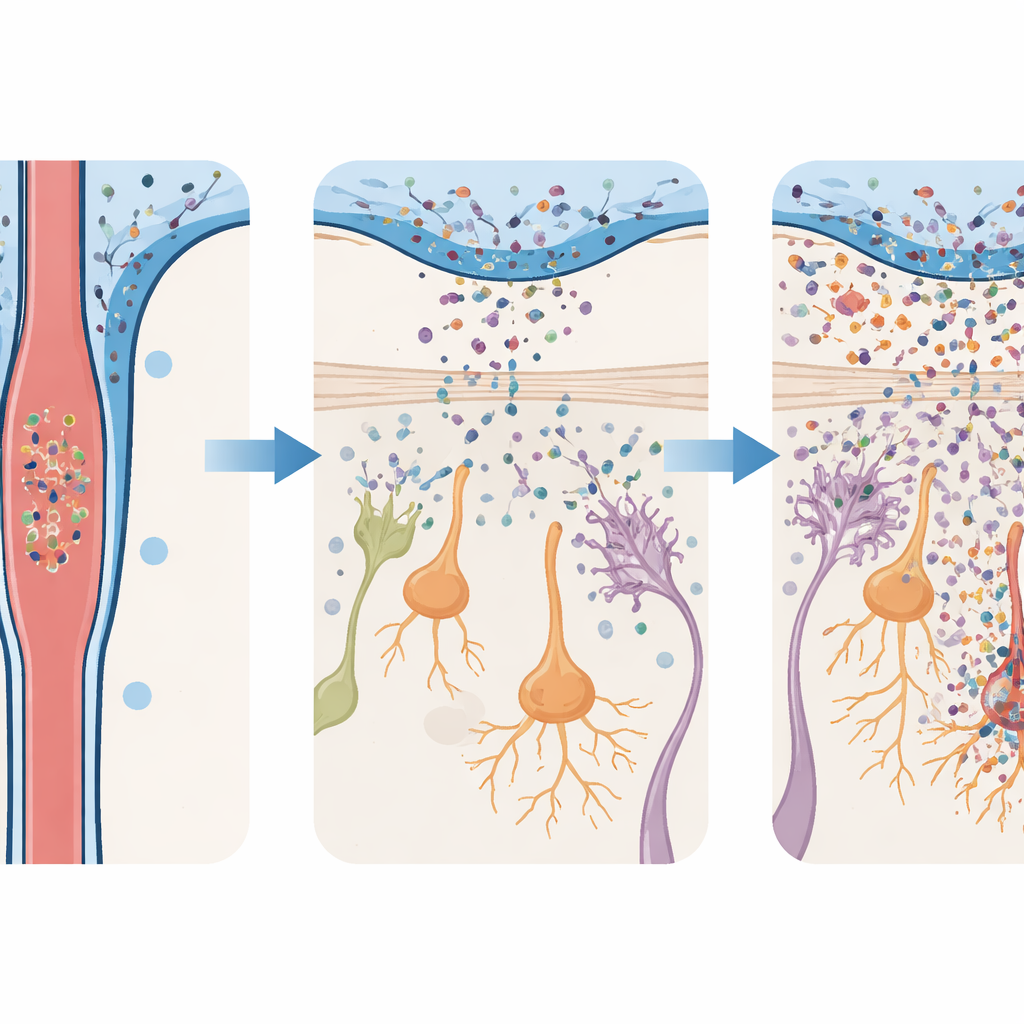
בעיות ריח מוקדמות ובעיות תנועה מאוחרות
השינויים ההתנהגותיים בעכברים עקבו אחרי קו הזמן של הנזק התאי. בעלי החיים שקיבלו אוליגומרים של אלפא‑סינוקלאין פיתחו במהירות קושי למצוא מזון מוסתר באמצעות הריח, הראו עניין מופחת בריחות מושכים כמו שתן עכברית, והיו פחות נוטים להימנע מריחות בלתי נעימים. החולשות המבוססות‑ריח הופיעו בתוך ימים ועמדו למשך כמעט חודשיים. עם זאת, אותם עכברים הלכו, שמרו על שווי משקל ותיאום כרגיל במבחני תנועה סטנדרטיים עד הרבה מאוחר יותר, כאשר בעיות מוטוריות ברורות התגלו סוף סוף. חשוב לציין, שכאשר החוקרים הורידו את מינון האוליגומרים המוזרקים, בלבלב הריח נרשמה דלקת ואובדן נוירונים מצומצמים יותר, והחיות שמרו ברובן על יכולות ריח תקינות. רגישות זו למינון מרמזת שמטען החלבון הרעיל ב‑CSF מעצב במישרין כמה נזק מוקדם יקרה.
מה המשמעות לטיפולים עתידיים
בסיכום, הממצאים תומכים בתפיסה חדשה של מחלת פרקינסון שבה אוליגומרים רעילים של אלפא‑סינוקלאין ב‑CSF אינם רק איתות להרס מתמשך — הם מפיצים אותו בפועל על ידי זרימה חזרה אל המוח לאורך תעלות פרי‑וסקולריות. מאחר שבלבלב הריח מקבל חלק חזק יותר מהחדירה הזו, הוא סובל מפגיעה מוקדמת וחמורה יותר, מה שמסביר מדוע אובדן הריח יכול להקדים את הרעד והנוקשות בשנים רבות. והעיקר — העבודה מציעה גישה התערבותית: אם נצליח להפחית או להסיר בבטחה את האוליגומרים האלה מ‑CSF — באמצעות מתקני סינון, נוגדנים ממוקדים או אסטרטגיות אחרות של "ניקוי CSF" — אנו עשויים להגן על אזורים פגיעים כמו בלבלב הריח ולהאט את כל מפלס הפתולוגיה הדומה לפרקינסון.
ציטוט: Zhu, WX., He, XZ., Meng, JC. et al. Perivascular spread of CSF-derived α-synuclein oligomers drives region-specific Parkinson’s-like pathology. npj Parkinsons Dis. 12, 84 (2026). https://doi.org/10.1038/s41531-026-01300-3
מילות מפתח: מחלת פרקינסון, אלפא-סינוקלאין, נוזל מוח־שדרה, מערכת הגלימפתית, תפקוד חוש הריח