Clear Sky Science · ar
انتشار فوق الوعائي لأوليجوميرات α‑سينوكلين المشتقة من السائل الدماغي الشوكي يدفع باتجاه نمط مرض شبيه بباركنسون في مناطق محددة
لماذا هذا مهم لمرض باركنسون
غالباً ما يُنظر إلى مرض باركنسون على أنه اضطراب حركي يتسم بالرجفان وتصلب العضلات. لكن قبل سنوات من ظهور هذه المشاكل الحركية، يفقد العديد من المرضى حاسة الشم. تطرح هذه الدراسة سؤالاً بسيطاً لكنه قوي: هل يمكن أن البروتينات السامة العائمة في السائل الشفاف الذي يحيط بالمخ تُسهم في بدء المرض في المناطق المرتبطة بالشم، قبل أن تتأثر مراكز الحركة بوقت طويل؟ من خلال تتبُّع كيفية تنقّل هذه البروتينات وما الضرر الذي تُحدثه في الفئران، يكشف الباحثون عن نظام «سباكة» خفي قد يدفع بتقدّم باركنسون على مراحل — ويشير إلى وسيلة غير متوقعة لبطئه.
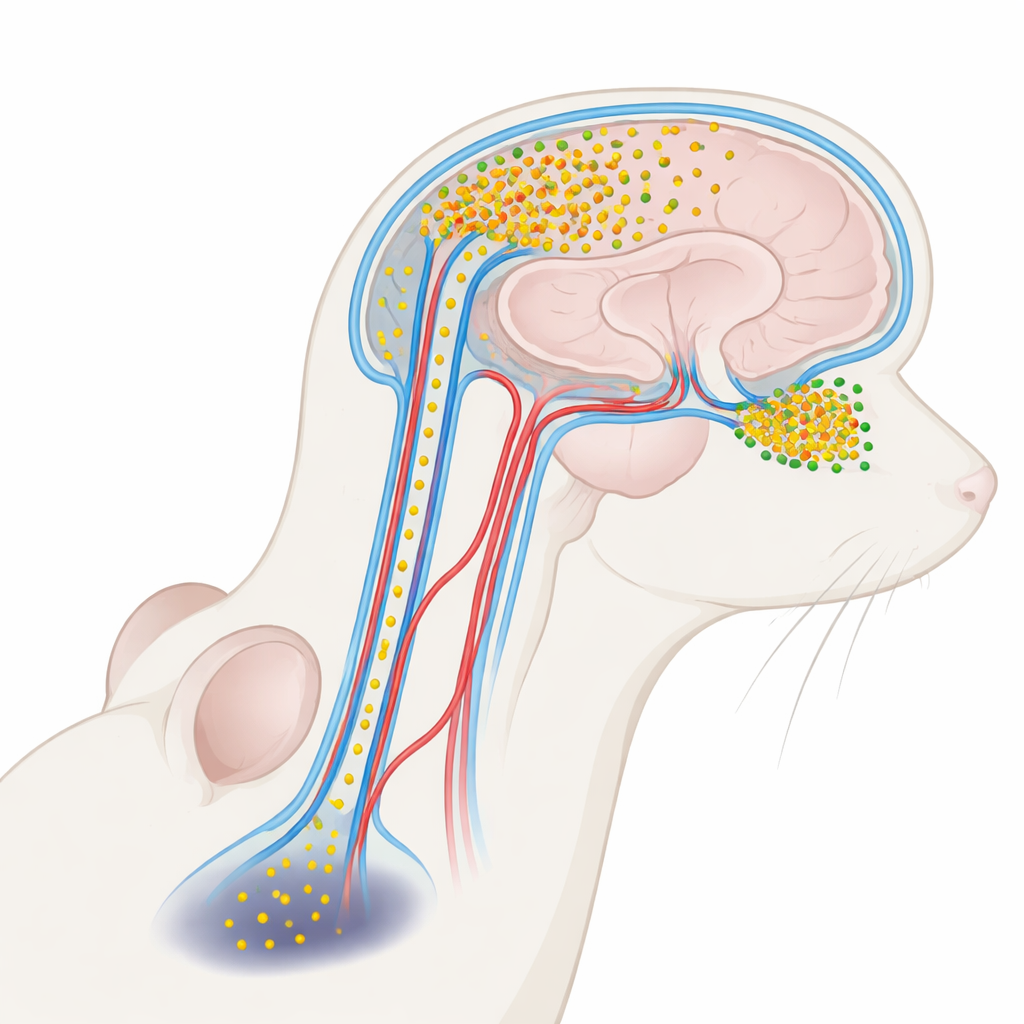
بروتين ضار يركب في سوائل المخ
يرتبط مرض باركنسون ارتباطاً وثيقاً ببروتين يُدعى ألفا‑سينوكلين. في المخ السليم، يساعد هذا البروتين الخلايا العصبية على التواصل. لكن في ظروف المرض، يمكن أن يتكتل ألفا‑سينوكلين إلى مجموعات قابلة للذوبان صغيرة تُعرف بالأوليغوميرات، وهي سامة بشكل خاص للخلايا العصبية. تظهر هذه الأوليغوميرات بمستويات أعلى في السائل الشفاف الذي يغمر المخ والحبل الشوكي — السائل الدماغي الشوكي — لدى الأشخاص المصابين بباركنسون. وحتى الآن، اعتُبر ألفا‑سينوكلين في السائل الدماغي الشوكي غالباً كمؤشر مفيد للمرض وليس كعامل فعّال. تساءل مؤلفو هذه الورقة عما إذا كانت هذه الأوليغوميرات المحمولة في السائل الدماغي الشوكي قد تتسرّب فعلاً مرة أخرى إلى المخ وتتسبب في إصابة مناطق محددة، مما يساعد على تفسير سبب ظهور مشاكل الشم مبكراً بينما تظهر اضطرابات الحركة لاحقاً.
سباكة المخ ومركز الشم الضعيف
لا يقتصر دور السائل الدماغي الشوكي على حماية المخ ميكانيكياً؛ بل يَتداول عبر شبكة من القنوات المحاذية للأوعية الدموية المعروفة بالمساحات فوق الوعائية، كجزء من نظام تنظيف أوسع يُدعى «الغليمفاتيك». باستخدام علامات متوهجة ومجاهر ثلاثية الأبعاد متقدمة، حقن الباحثون ألفا‑سينوكلين معنّماً في السائل الدماغي الشوكي عند الفئران وتتبّعوا مساره. وجدوا أن البروتين يدخل المخ على طول هذه المسارات فوق الوعائية ويتراكم بشكل غير متساوٍ للغاية. تَمتص البُصلة الشمية — البنية الصغيرة في مقدمة المخ المسؤولة عن معالجة الروائح — كمية أكبر بكثير من البروتين الوارد مقارنة بمناطق أعمق مثل المادة السوداء التي تتحكّم في الحركة. وحتى داخل البُصلة الشمية نفسها، أظهرت بعض المناطق الفرعية تدفّقاً أكبر من غيرها، ما يشير إلى هشاشة بدرجة دقيقة تتشكل وفق تدفق السائل المحلي وتوزيع الأوعية الدموية.
من تدفّق صامت إلى التهاب وفقدان للعصبونات
لاختبار ماذا يفعل هذا التدفق، غمر الفريق الفئران بأوليغوميرات ألفا‑سينوكلين السامة وفحص أدمغتها عبر الزمن. في كل من البُصلة الشمية والمادة السوداء، تنبّهت خلايا الدعم المناعي المسماة ميكروغليا والنجمية، وارتفعت جزيئات الالتهاب. لكن هذه التفاعلات كانت أقوى بكثير في البُصلة الشمية. هناك، بدأت الخلايا المنتجة للدوبامين — وهي الخلايا التي تستخدم نفس الناقل الكيميائي المرتبط بباركنسون — بالموت مبكراً واستمرت في التناقص لأسابيع. بالمقابل، بقيت خلايا الدوبامين في المادة السوداء سليمة إلى حد كبير حتى مراحل لاحقة، حين ظهرت الخسائر أخيراً. يعكس هذا الضرر المتدرج الصورة السريرية: مشكلات مبكرة في دوائر الشم تليها إصابة لاحقة للخلايا المتحكمة بالحركة.
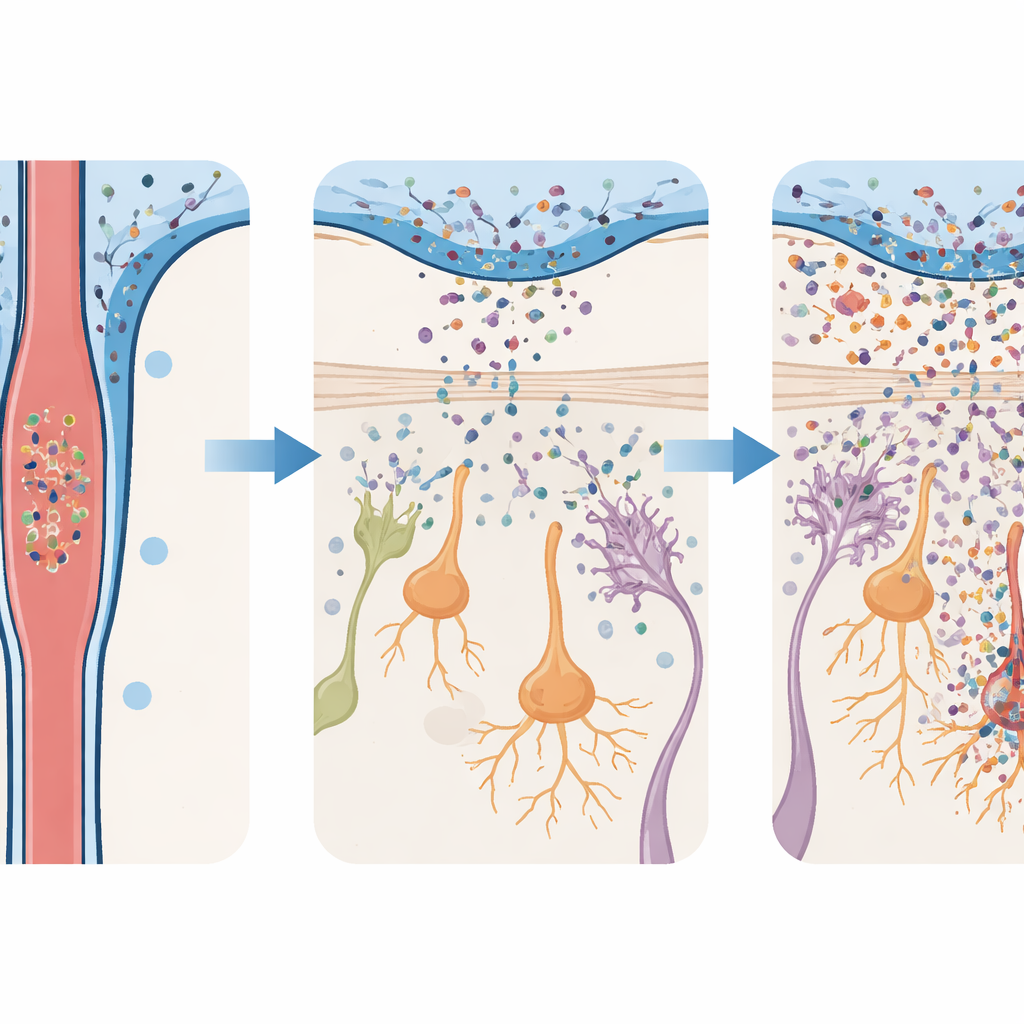
مشكلات شمية مبكرة ومشكلات حركية متأخرة
تتبعت التغيرات السلوكية عند الفئران نفس الجدول الزمني للتلف الخلوي. الفئران التي تعرّضت لأوليغوميرات ألفا‑سينوكلين طورت بسرعة صعوبة في العثور على طعام مخفي باستخدام الشم، وأبدت اهتماماً أقل بالروائح الجذابة مثل بول الفأرة الأنثى، وكانت أقل ميلاً لتجنّب الروائح المزعجة. ظهرت هذه العجزات الشمية خلال أيام واستمرت لما يقرب من شهرين. ومع ذلك، سارَت الفئران نفسها وتزنّنت وتناسقت طبيعتها في اختبارات الحركة القياسية بشكل طبيعي حتى وقت لاحق بكثير، عندما ظهرت صعوبات حركية واضحة أخيراً. ومن المهم أن الباحثين عندما خفضوا جرعة الأوليغوميرات المحقونة، شهدت البُصلة الشمية التهابات وخسائر عصبية أقل بكثير، واحتفظت الحيوانات إلى حد كبير بقدرات شم طبيعية. تشير حساسية الجرعة هذه إلى أن عبء البروتين السام في السائل الدماغي الشوكي يُحدّد مباشرة مقدار التلف المبكر الذي يحدث.
ما يعنيه هذا للعلاجات المستقبلية
تدعم النتائج مجتمعة رؤية جديدة لمرض باركنسون مفادها أن أوليغوميرات ألفا‑سينوكلين السامة في السائل الدماغي الشوكي لا تقتصر على الإشارة إلى تلف جارٍ — بل تنشره فعلياً عبر التدفق مرة أخرى إلى المخ على طول القنوات فوق الوعائية. وبما أن البُصلة الشمية تتلقى حصة أكبر من هذا التدفق، فهي تتعرض لإصابة أبكر وأكثر شدة، مما يفسّر لماذا قد يسبق فقدان الشم الرجفان والتصلب بعد سنوات. والأهم من ذلك أن العمل يلمّح إلى تدخل محتمل: إذا استطعنا تقليل أو إزالة هذه الأوليغوميرات من السائل الدماغي الشوكي بأمان — عبر أجهزة ترشيح، أجسام مضادة مستهدفة، أو استراتيجيات أخرى «لتنقية السائل الدماغي الشوكي» — فقد نتمكن من حماية مناطق عرضة مثل البُصلة الشمية وإبطاء سلسلة الأمراض الشبيهة بباركنسون.
الاستشهاد: Zhu, WX., He, XZ., Meng, JC. et al. Perivascular spread of CSF-derived α-synuclein oligomers drives region-specific Parkinson’s-like pathology. npj Parkinsons Dis. 12, 84 (2026). https://doi.org/10.1038/s41531-026-01300-3
الكلمات المفتاحية: مرض باركنسون, ألفا‑سينوكلين, السائل الدماغي الشوكي, النظام الغليمفاتي, خلل الشم