Clear Sky Science · de
Perivaskuläre Ausbreitung von CSF‑getragenen α‑Synuklein‑Oligomeren treibt regionsspezifische Parkinson‑ähnliche Pathologie an
Warum das für die Parkinson‑Krankheit wichtig ist
Viele denken bei Parkinson vor allem an eine Bewegungsstörung mit Tremor und Steifheit. Doch Jahre bevor diese motorischen Probleme auftreten, verlieren viele Patienten ihren Geruchssinn. Diese Studie stellt eine einfache, aber folgenschwere Frage: Könnten toxische Proteine, die in der klaren Hirnflüssigkeit herumschwimmen, die Erkrankung in geruchszentrierten Hirnregionen auslösen, lange bevor motorische Zentren betroffen sind? Indem die Forschenden verfolgen, wie diese Proteine sich ausbreiten und welchen Schaden sie bei Mäusen anrichten, enthüllen sie ein verborgenes ‚Sanitärsystem‘, das die schrittweise Progression von Parkinson antreiben könnte — und weisen auf eine unerwartete neue Möglichkeit hin, das Fortschreiten zu verlangsamen.
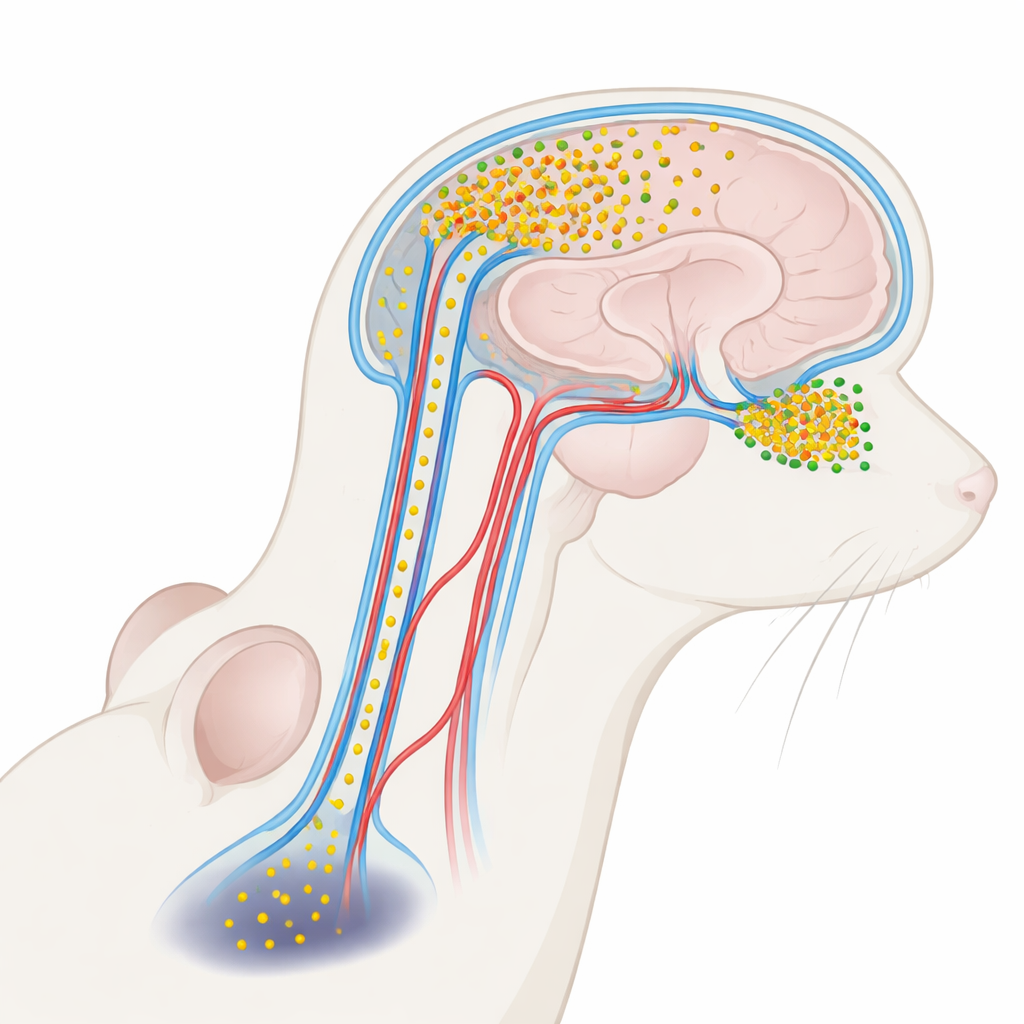
Ein schädliches Protein in der Hirnflüssigkeit
Die Parkinson‑Krankheit steht in engem Zusammenhang mit einem Protein namens Alpha‑Synuklein. In gesunden Gehirnen unterstützt es die Kommunikation von Nervenzellen. Unter Krankheitsbedingungen kann Alpha‑Synuklein jedoch zu kleinen löslichen Klumpen, sogenannten Oligomeren, aggregieren, die besonders toxisch für Neurone sind. Diese Oligomere treten in erhöhtem Maß in der klaren Flüssigkeit auf, die Gehirn und Rückenmark umgibt — dem Liquor cerebrospinalis (CSF) — von Menschen mit Parkinson. Bisher wurde CSF‑Alpha‑Synuklein meist als nützlicher Biomarker der Krankheit behandelt, nicht als aktiver Mitverursacher. Die Autorinnen und Autoren dieser Arbeit fragten, ob diese im CSF herumreichenden Oligomere tatsächlich wieder ins Gehirn eindringen und bestimmte Regionen schädigen könnten, was erklären würde, warum Riechstörungen früh, motorische Probleme später auftreten.
Die Hirn‑'Sanitärinstallation' und ein verwundbares Riechzentrum
CSF polstert das Gehirn nicht nur ab; es zirkuliert durch ein Netzwerk von Kanälen entlang der Blutgefäße, den perivaskulären Räumen, die Teil eines umfassenderen „glymphatischen“ Reinigungssystems sind. Mit leuchtenden Markern und fortgeschrittener 3‑D‑Mikroskopie injizierten die Forschenden markiertes Alpha‑Synuklein in den CSF von Mäusen und verfolgten seinen Weg. Sie fanden, dass das Protein entlang dieser perivaskulären Routen ins Gehirn gelangte und sich sehr ungleichmäßig anreicherte. Die Riechkolben — die kleine vordere Struktur des Gehirns, die Gerüche verarbeitet — nahmen weitaus mehr des eingehenden Proteins auf als tiefere Regionen wie die Substantia nigra, die die Bewegung steuert. Selbst innerhalb des Riechkolbens zeigten einige Unterregionen stärkere Einströmung als andere, was auf eine feinkörnige Verwundbarkeit hindeutet, die durch lokale Flüssigkeitsströmung und Gefäßanordnung geprägt ist.
Von stiller Einströmung zu Entzündung und Neuronenverlust
Um zu prüfen, welche Folgen diese Einströmung hat, infundierte das Team Mäuse mit toxischen Alpha‑Synuklein‑Oligomeren und untersuchte ihre Gehirne über die Zeit. In sowohl dem Riechkolben als auch der Substantia nigra wurden die Immununterstützungszellen, sogenannte Mikroglia und Astrozyten, aktiviert und entzündliche Moleküle erhöht. Diese Reaktionen waren jedoch im Riechkolben wesentlich ausgeprägter. Dort begannen Dopamin produzierende Neurone — Zellen, die denselben in Parkinson involvierten Botenstoff verwenden — früh abzusterben und nahmen über Wochen weiter ab. Im Gegensatz dazu blieben Dopamin‑Neurone in der Substantia nigra weitgehend intakt bis zu einem deutlich späteren Zeitpunkt, an dem Verluste schließlich sichtbar wurden. Diese gestaffelte Schädigung spiegelt das klinische Bild wider: frühe Probleme in Geruchsnetzwerken, gefolgt von späteren Schäden an bewegungssteuernden Zellen.
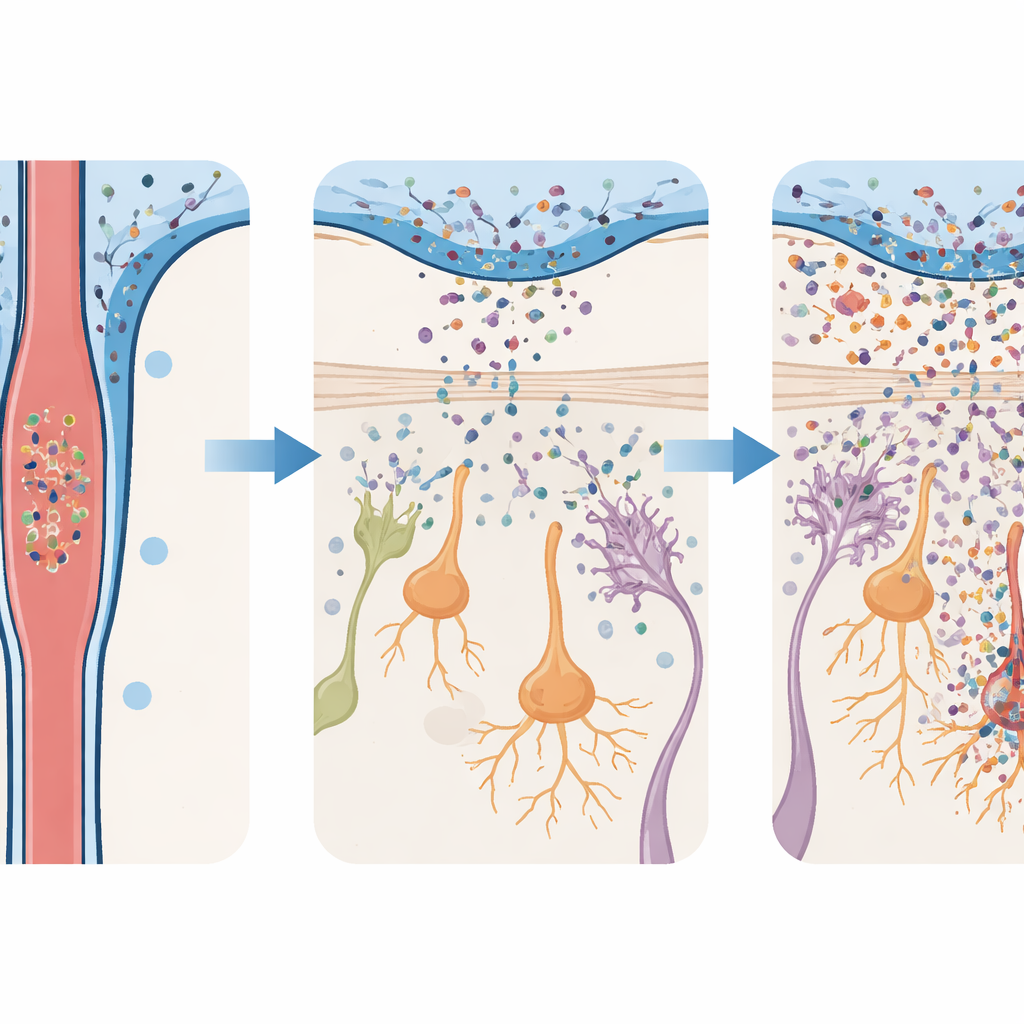
Frühe Riechstörungen und spätere Bewegungsprobleme
Die Verhaltensänderungen bei den Mäusen folgten demselben Zeitverlauf wie die zellulären Schäden. Tiere, die Alpha‑Synuklein‑Oligomere erhielten, entwickelten schnell Schwierigkeiten, versteckte Nahrung mithilfe des Geruchs zu finden, zeigten weniger Interesse an anziehenden Gerüchen wie Urin von Weibchen und waren weniger geneigt, unangenehme Gerüche zu meiden. Diese geruchsbedingten Defizite traten innerhalb weniger Tage auf und hielten fast zwei Monate an. Die gleichen Tiere gingen jedoch in Standardtests zu Gehen, Gleichgewicht und Koordination bis deutlich später normal umher, bis schließlich eindeutige motorische Schwierigkeiten auftraten. Wichtig ist: Wenn die Forschenden die Dosis der injizierten Oligomere verringerten, zeigte der Riechkolben deutlich weniger Entzündung und Neuronenverlust, und die Tiere behielten größtenteils ihre normalen Geruchsfähigkeiten. Diese Dosis‑Empfindlichkeit deutet darauf hin, dass die Last an toxischem Protein im CSF direkt bestimmt, wie viel frühen Schaden es gibt.
Was das für künftige Behandlungen bedeutet
Insgesamt stützen die Ergebnisse eine neue Sicht auf die Parkinson‑Krankheit, wonach toxische Alpha‑Synuklein‑Oligomere im CSF mehr sind als ein Zeichen bereits ablaufender Schäden — sie verbreiten die Schädigung aktiv, indem sie entlang perivaskulärer Kanäle zurück ins Gehirn fließen. Da der Riechkolben einen stärkeren Anteil dieses Eintrags erhält, erleidet er frühere und schwerere Schäden, was erklärt, warum Geruchsverlust Tremor und Steifheit um Jahre vorausgehen kann. Entscheidend ist, dass die Arbeit auch auf eine mögliche Intervention hinweist: Wenn wir diese Oligomere sicher aus dem CSF reduzieren oder entfernen können — etwa durch Filtrationsgeräte, gezielte Antikörper oder andere „CSF‑reinigende“ Strategien — könnten wir verwundbare Regionen wie den Riechkolben schützen und die gesamte Kaskade Parkinson‑ähnlicher Pathologie verlangsamen.
Zitation: Zhu, WX., He, XZ., Meng, JC. et al. Perivascular spread of CSF-derived α-synuclein oligomers drives region-specific Parkinson’s-like pathology. npj Parkinsons Dis. 12, 84 (2026). https://doi.org/10.1038/s41531-026-01300-3
Schlüsselwörter: Parkinson‑Krankheit, Alpha‑Synuklein, Liquor cerebrospinalis, Glymphatisches System, Riechstörung