Clear Sky Science · it
Diffusione perivascolare di oligomeri di α-sinucleina derivati dal LCR guida una patologia simile al Parkinson specifica per regione
Perché questo è importante per la malattia di Parkinson
Molti considerano la malattia di Parkinson un disturbo del movimento, caratterizzato da tremore e rigidità. Ma anni prima che compaiano questi problemi motori, molti pazienti perdono l’olfatto. Questo studio pone una domanda semplice ma potente: proteine tossiche sospese nel fluido che bagna il cervello potrebbero avviare la malattia nelle regioni cerebrali legate all’olfatto, molto prima che vengano colpiti i centri del movimento? Tracciando come queste proteine si spostano e quali danni causano nei topi, i ricercatori scoprono un sistema idraulico nascosto che potrebbe guidare la progressione graduale del Parkinson—e indicano un modo inatteso per rallentarla.
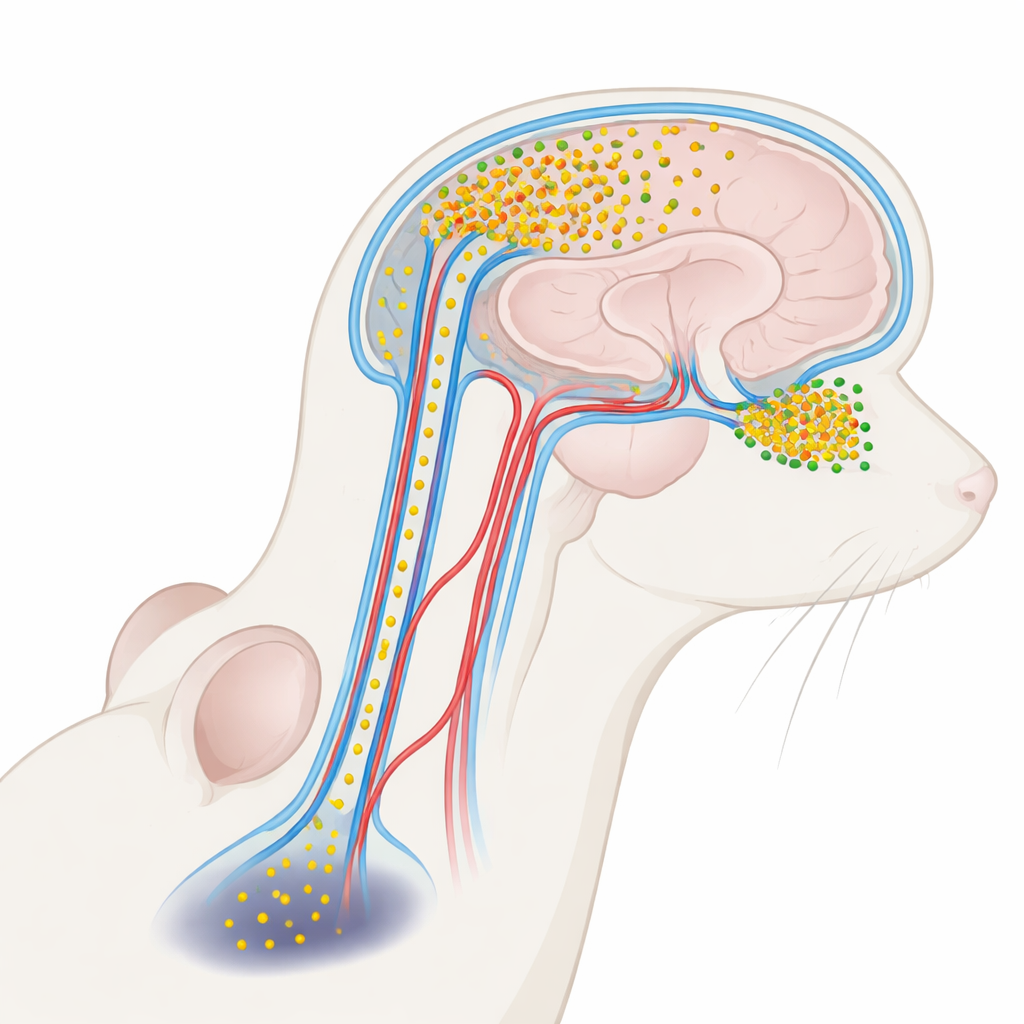
Una proteina dannosa che viaggia nel fluido cerebrale
La malattia di Parkinson è strettamente associata a una proteina chiamata alpha‑sinucleina. Nel cervello sano aiuta le cellule nervose a comunicare. In condizioni patologiche, tuttavia, la alpha‑sinucleina può aggregarsi in piccoli ammassi solubili chiamati oligomeri, particolarmente tossici per i neuroni. Questi oligomeri risultano elevati nel liquido chiaro che bagna cervello e midollo spinale—il liquido cerebrospinale, o LCR—nelle persone con Parkinson. Finora, la maggior parte degli studi ha considerato la alpha‑sinucleina nel LCR come un utile marcatore della malattia, non come un attore attivo. Gli autori di questo lavoro hanno chiesto se questi oligomeri presenti nel LCR possano effettivamente filtrare nuovamente nel cervello e danneggiare regioni specifiche, contribuendo a spiegare perché i problemi olfattivi compaiono precocemente mentre i disturbi del movimento emergono più tardi.
Gli impianti idraulici del cervello e un centro olfattivo vulnerabile
Il LCR non si limita a ammortizzare il cervello; circola attraverso una rete di canali lungo i vasi sanguigni noti come spazi perivascolari, parte di un più ampio sistema di drenaggio «glinfatico». Usando marcatori fluorescenti e microscopi tridimensionali avanzati, i ricercatori hanno iniettato alpha‑sinucleina marcata nel LCR dei topi e seguito il suo percorso. Hanno osservato che la proteina entrava nel cervello lungo queste vie perivascolari e si accumulava in modo molto disomogeneo. Il bulbo olfattivo—la piccola struttura frontale che elabora gli odori—assorbiva molto più della proteina in ingresso rispetto a regioni più profonde come la sostanza nera, che controlla il movimento. Anche all’interno del bulbo olfattivo, alcune sottozone mostravano un’affluenza maggiore di altre, suggerendo una vulnerabilità fine determinata dal flusso locale dei fluidi e dalla disposizione dei vasi.
Dall’afflusso silenzioso a infiammazione e perdita neuronale
Per testare l’effetto di questo afflusso, il team ha infuso nei topi oligomeri tossici di alpha‑sinucleina ed esaminato i loro cervelli nel tempo. Sia nel bulbo olfattivo sia nella sostanza nera, le cellule di supporto immunitario chiamate microglia e astrociti si sono attivate e sono aumentate le molecole infiammatorie. Ma queste reazioni sono state molto più intense nel bulbo olfattivo. Qui, i neuroni produttori di dopamina—cellule che usano lo stesso mediatore chimico implicato nel Parkinson—hanno iniziato a morire precocemente e hanno continuato a declinare per settimane. Al contrario, i neuroni dopaminergici della sostanza nera sono rimasti in gran parte intatti fino a tempi molto più avanzati, quando è comparsa infine la perdita. Questo danno in stadi rispecchia il quadro clinico: problemi precoci nel circuito olfattivo, seguiti da un danno successivo alle cellule che controllano il movimento.
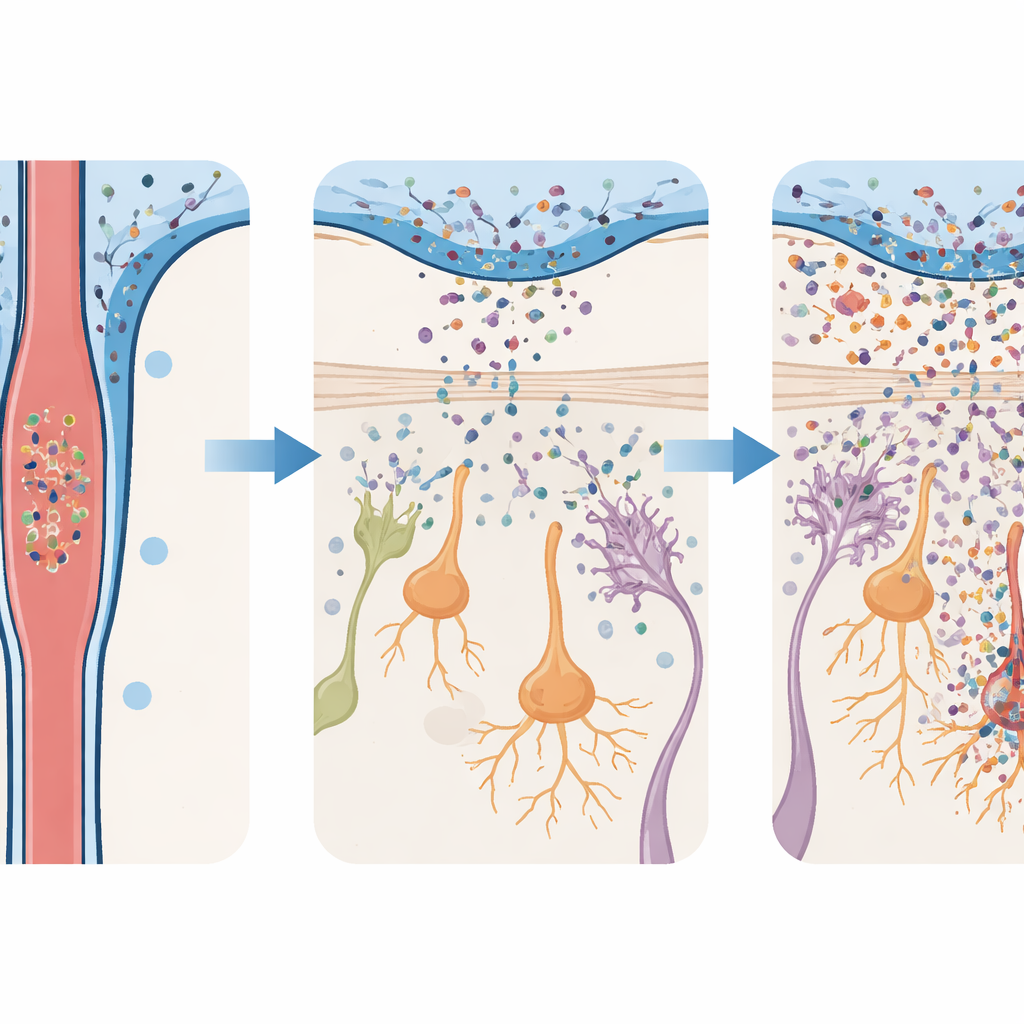
Problemi olfattivi precoci e disturbi motori tardivi
I cambiamenti comportamentali nei topi hanno seguito la stessa cronologia del danno cellulare. Gli animali trattati con oligomeri di alpha‑sinucleina hanno rapidamente sviluppato difficoltà a trovare cibo nascosto con l’olfatto, hanno mostrato meno interesse per odori attraenti come l’urina di femmina e sono stati meno inclini a evitare odori sgradevoli. Questi deficit olfattivi sono comparsi in pochi giorni e sono perdurati per quasi due mesi. Tuttavia gli stessi topi camminavano, si bilanciavano e si coordinavano normalmente nei test motori standard fino a tempi molto più tardivi, quando sono emerse difficoltà motorie chiare. È importante che, quando i ricercatori hanno ridotto la dose di oligomeri iniettati, il bulbo olfattivo abbia mostrato molta meno infiammazione e perdita neuronale, e gli animali abbiano in gran parte mantenuto normali capacità olfattive. Questa sensibilità alla dose suggerisce che il carico di proteina tossica nel LCR modella direttamente l’entità del danno precoce.
Cosa significa per i trattamenti futuri
Complessivamente, i risultati supportano una nuova visione della malattia di Parkinson in cui gli oligomeri tossici di alpha‑sinucleina nel LCR non si limitano a segnalare il danno in corso—ma lo diffondono attivamente ritornando nel cervello lungo i canali perivascolari. Poiché il bulbo olfattivo riceve una quota maggiore di questo afflusso, subisce un danno più precoce e grave, spiegando perché la perdita dell’olfatto può precedere di anni tremori e rigidità. Elemento cruciale, il lavoro suggerisce anche un intervento: se potessimo ridurre o rimuovere in sicurezza questi oligomeri dal LCR—attraverso dispositivi di filtrazione, anticorpi mirati o altre strategie di «pulizia» del LCR—potremmo proteggere regioni vulnerabili come il bulbo olfattivo e rallentare l’intera cascata di patologia simile al Parkinson.
Citazione: Zhu, WX., He, XZ., Meng, JC. et al. Perivascular spread of CSF-derived α-synuclein oligomers drives region-specific Parkinson’s-like pathology. npj Parkinsons Dis. 12, 84 (2026). https://doi.org/10.1038/s41531-026-01300-3
Parole chiave: Malattia di Parkinson, alpha-sinucleina, liquido cerebrospinale, sistema glinfatico, disfunzione olfattiva