Clear Sky Science · fr
La dissémination périvasculaire d’oligomères d’α-synucléine dérivés du LCS provoque une pathologie de type Parkinson spécifique à certaines régions
Pourquoi cela compte pour la maladie de Parkinson
On considère souvent la maladie de Parkinson comme un trouble moteur, caractérisé par des tremblements et une raideur. Mais des années avant l’apparition de ces troubles moteurs, de nombreux patients perdent l’odorat. Cette étude pose une question simple mais puissante : des protéines toxiques en suspension dans le liquide clair qui baigne le cerveau pourraient‑elles déclencher la maladie dans les régions liées à l’odorat, bien avant que les centres du mouvement ne soient touchés ? En traçant le trajet de ces protéines et les lésions qu’elles causent chez la souris, les chercheurs mettent au jour un réseau de « canalisations » caché susceptible de conduire la progression pas à pas de la maladie de Parkinson — et suggèrent une voie inattendue pour la ralentir.
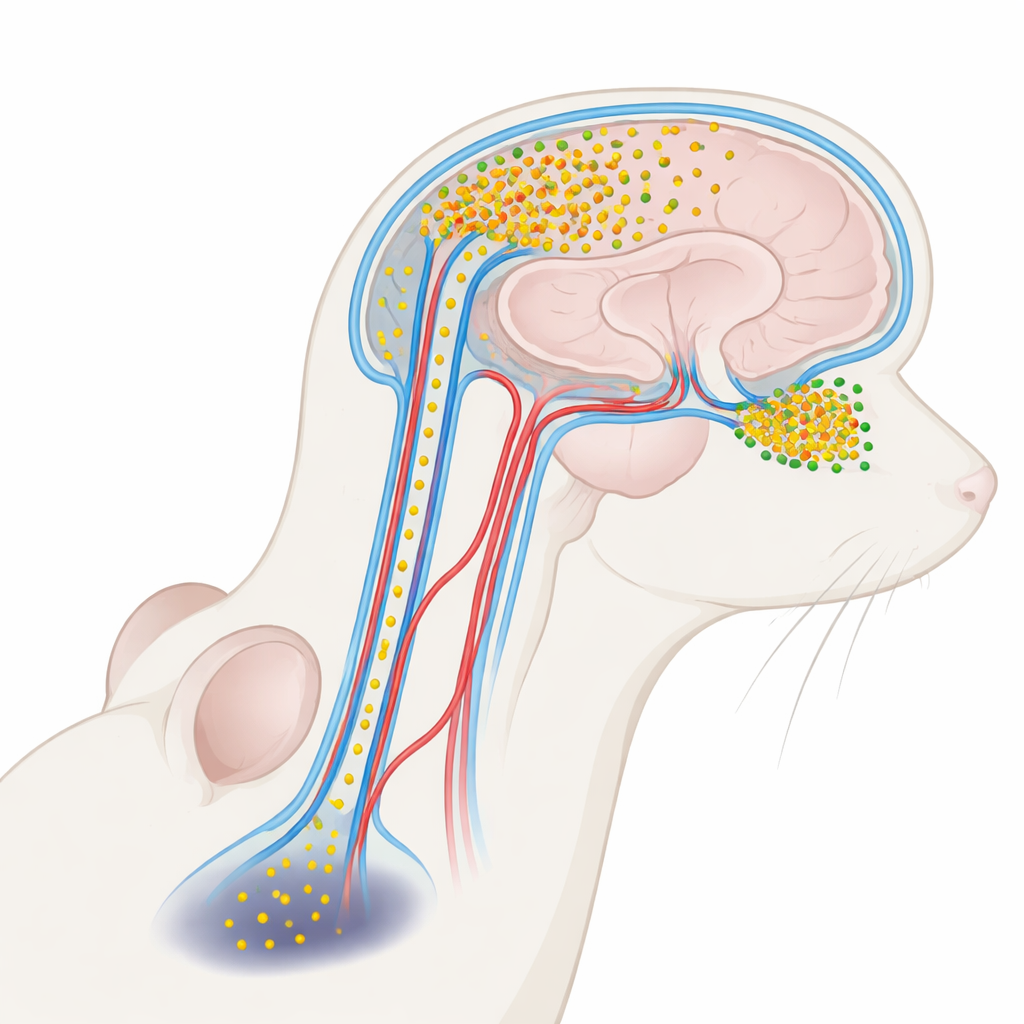
Une protéine nocive portée par le liquide cérébral
La maladie de Parkinson est étroitement liée à une protéine appelée alpha‑synucléine. Dans un cerveau sain, elle aide les neurones à communiquer. En cas de maladie, cependant, l’alpha‑synucléine peut s’agréger en petits amas solubles appelés oligomères, particulièrement toxiques pour les neurones. Ces oligomères sont présents à des niveaux plus élevés dans le liquide clair qui baigne le cerveau et la moelle épinière — le liquide céphalo‑rachidien (LCR) — chez les personnes atteintes de Parkinson. Jusqu’à présent, la plupart des travaux considéraient l’alpha‑synucléine du LCR comme un marqueur utile de la maladie, pas comme un acteur actif. Les auteurs de cet article se sont demandé si ces oligomères véhiculés par le LCR pouvaient en réalité s’infiltrer à nouveau dans le cerveau et endommager des régions spécifiques, ce qui aiderait à expliquer pourquoi les troubles de l’odorat apparaissent tôt alors que les problèmes moteurs surviennent plus tard.
La plomberie du cerveau et un centre olfactif vulnérable
Le LCR ne sert pas seulement d’amortisseur pour le cerveau ; il circule aussi à travers un réseau de canaux le long des vaisseaux sanguins appelés espaces périvasculaires, partie d’un système de clairance plus large dit « glymphatique ». En utilisant des marqueurs fluorescents et des microscopes tridimensionnels avancés, les chercheurs ont injecté de l’alpha‑synucléine marquée dans le LCR de souris et observé sa distribution. Ils ont constaté que la protéine pénétrait dans le cerveau le long de ces trajets périvasculaires et s’accumulait de manière très inégale. Le bulbe olfactif — la petite structure à l’avant du cerveau qui traite les odeurs — absorbait beaucoup plus de protéine entrante que des régions plus profondes comme la substance noire, qui contrôle le mouvement. Même au sein du bulbe olfactif, certaines sous‑régions présentaient un afflux plus important que d’autres, ce qui suggère une vulnérabilité à fine échelle façonnée par le flux local de liquide et l’agencement des vaisseaux.
D’un afflux silencieux à l’inflammation et à la perte neuronale
Pour tester les effets de cet afflux, l’équipe a administré aux souris des oligomères toxiques d’alpha‑synucléine et examiné leur cerveau au fil du temps. Dans le bulbe olfactif comme dans la substance noire, des cellules de soutien immunitaire appelées microglies et astrocytes se sont activées, et des molécules inflammatoires ont augmenté. Mais ces réactions ont été beaucoup plus fortes dans le bulbe olfactif. Là, des neurones producteurs de dopamine — des cellules utilisant le même messager chimique impliqué dans la Parkinson — ont commencé à mourir précocement et ont continué à décliner pendant des semaines. En revanche, les neurones dopaminergiques de la substance noire sont restés en grande partie intacts jusqu’à un stade beaucoup plus tardif, lorsque des pertes sont finalement apparues. Cette lésion par paliers reflète l’image clinique : des problèmes précoces dans le circuit olfactif, suivis d’une atteinte ultérieure des cellules contrôlant le mouvement.
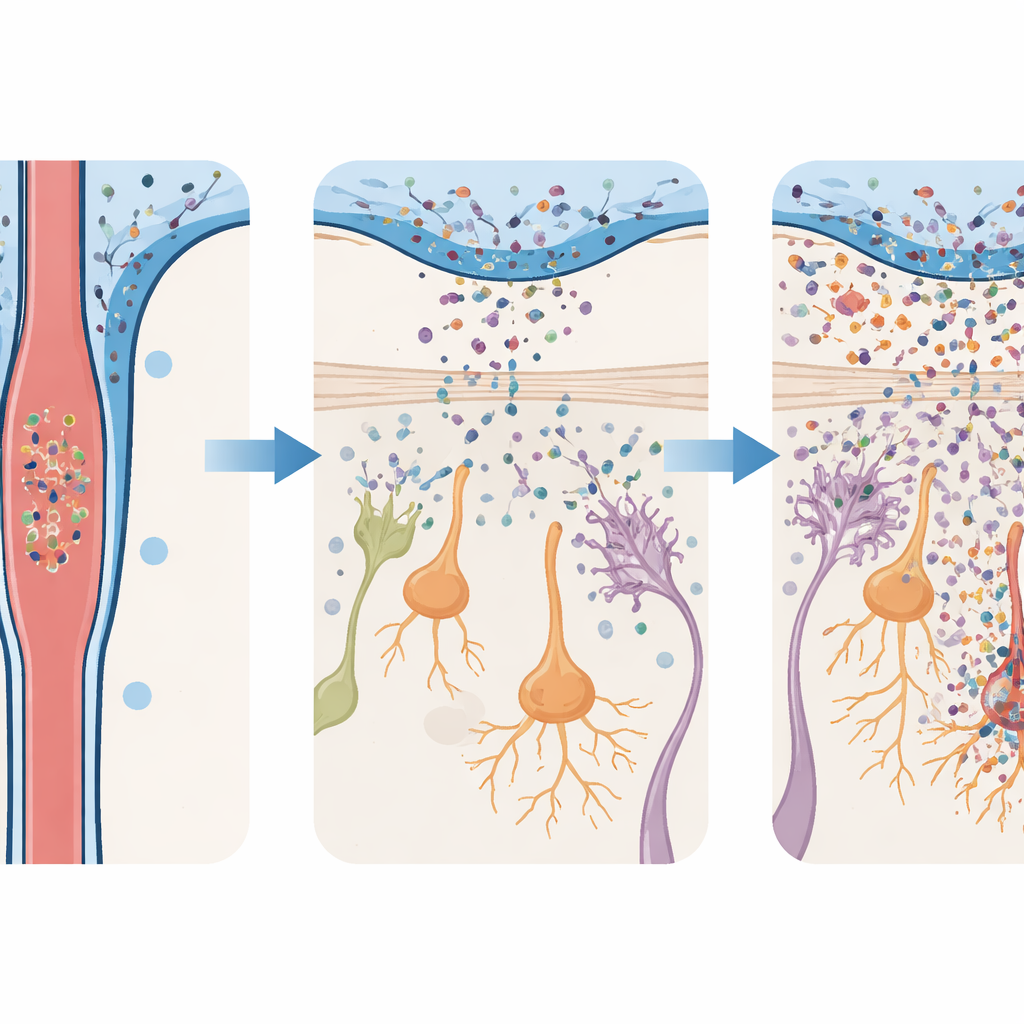
Problèmes précoces d’odorat et troubles moteurs tardifs
Les changements comportementaux chez les souris ont suivi la même chronologie que les lésions cellulaires. Les animaux exposés aux oligomères d’alpha‑synucléine ont rapidement eu des difficultés à retrouver de la nourriture cachée par l’odorat, ont montré moins d’intérêt pour des odeurs attractives comme l’urine de femelle, et étaient moins enclins à éviter les odeurs désagréables. Ces déficits olfactifs sont apparus en quelques jours et ont persisté près de deux mois. Pourtant, ces mêmes souris marchaient, gardaient l’équilibre et coordonnaient normalement leurs mouvements aux tests standards jusqu’à une phase beaucoup plus tardive, quand des difficultés motrices nettes sont finalement apparues. Fait important, lorsque les chercheurs ont réduit la dose d’oligomères injectés, le bulbe olfactif a présenté beaucoup moins d’inflammation et de perte neuronale, et les animaux ont en grande partie conservé des capacités olfactives normales. Cette sensibilité à la dose suggère que la charge de protéine toxique dans le LCR influence directement l’importance des dommages précoces.
Ce que cela implique pour les traitements futurs
Dans l’ensemble, ces résultats soutiennent une nouvelle vision de la maladie de Parkinson dans laquelle des oligomères toxiques d’alpha‑synucléine présents dans le LCR font plus que signaler un dommage en cours : ils le propagent activement en refluant dans le cerveau le long des canaux périvasculaires. Parce que le bulbe olfactif reçoit une part plus importante de cet afflux, il subit plus tôt et plus sévèrement des lésions, ce qui explique pourquoi la perte d’odorat peut précéder de plusieurs années les tremblements et la raideur. De façon cruciale, ce travail suggère aussi une piste d’intervention : si l’on peut réduire ou éliminer en toute sécurité ces oligomères du LCR — par des dispositifs de filtration, des anticorps ciblés ou d’autres stratégies de « nettoyage du LCR » — on pourrait protéger les régions vulnérables comme le bulbe olfactif et ralentir l’ensemble de la cascade de la pathologie de type Parkinson.
Citation: Zhu, WX., He, XZ., Meng, JC. et al. Perivascular spread of CSF-derived α-synuclein oligomers drives region-specific Parkinson’s-like pathology. npj Parkinsons Dis. 12, 84 (2026). https://doi.org/10.1038/s41531-026-01300-3
Mots-clés: Maladie de Parkinson, alpha-synucléine, liquide cérébrospinal, système glymphatique, trouble de l’olfaction