Clear Sky Science · sv
Perivaskulär spridning av CSF‑burna α‑synuklein‑oligomerer driver regionspecifik Parkinson‑liknande patologi
Varför detta spelar roll för Parkinsons sjukdom
Många tänker på Parkinsons sjukdom som en rörelsestörning, kännetecknad av tremor och stelhet. Men år innan dessa motoriska problem dyker upp förlorar många patienter luktsinnet. Denna studie ställer en enkel men kraftfull fråga: kan giftiga proteiner som flyter i hjärnans klara badvätska bidra till att starta sjukdomen i luktrelaterade hjärnregioner långt innan rörelsencentra påverkas? Genom att spåra hur dessa proteiner färdas och vilken skada de orsakar i möss avslöjar forskarna ett dolt rörsystem som kan driva den stegvisa utvecklingen av Parkinsons — och som pekar mot ett oväntat nytt sätt att bromsa den.
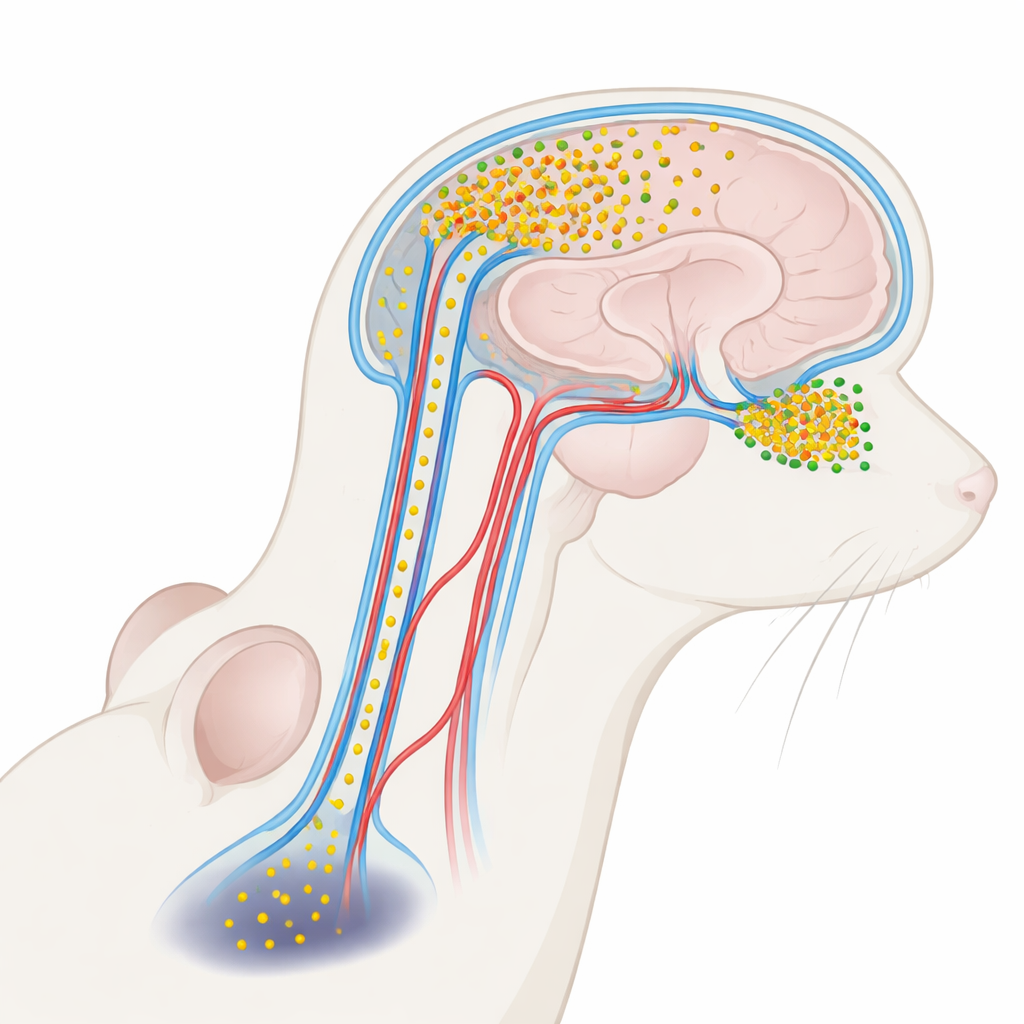
Ett skadligt protein i hjärnvätskan
Parkinsons sjukdom är tätt kopplad till ett protein kallat alfa‑synuklein. I friska hjärnor hjälper det nervceller att kommunicera. Under sjukdomsförhållanden kan dock alfa‑synuklein klumpa ihop sig till små lösliga kluster, så kallade oligomerer, som är särskilt giftiga för neuroner. Dessa oligomerer förekommer i högre nivåer i den klara vätska som omsluter hjärnan och ryggmärgen — cerebrospinalvätskan, eller CSF — hos personer med Parkinsons. Fram tills nu har det mesta arbetet betraktat CSF‑alfa‑synuklein som en användbar markör för sjukdom, inte som en aktiv aktör. Författarna till denna studie frågade om dessa CSF‑burna oligomerer faktiskt kunde tränga tillbaka in i hjärnan och skada specifika regioner, vilket skulle kunna förklara varför luktproblem kommer tidigt medan motoriska problem dyker upp senare.
Hjärnans rörsystem och ett sårbart luktcentrum
CSF både dämpar hjärnan och cirkulerar genom ett nätverk av kanaler längs blodkärl, så kallade perivaskulära utrymmen, som är en del av ett bredare glymfatiskt rensningssystem. Med hjälp av lysande taggar och avancerade tredimensionella mikroskop injicerade forskarna märkta alfa‑synuklein i CSF hos möss och följde dess väg. De fann att proteinet trängde in i hjärnan längs dessa perivaskulära rutter och ansamlades mycket ojämnt. Luktkroppen — den lilla strukturen i hjärnans front som bearbetar dofter — tog upp betydligt mer av det inkommande proteinet än djupare regioner som substantia nigra, som styr rörelser. Även inom själva luktkroppen visade vissa subregioner större inflöde än andra, vilket tyder på en finmaskig sårbarhet formad av lokala vätskeflöden och kärlstruktur.
Från tyst inflöde till inflammation och neuronförlust
För att pröva vad detta inflöde orsakar injicerade teamet giftiga alfa‑synuklein‑oligomerer i möss och undersökte deras hjärnor över tid. I både luktkroppen och substantia nigra aktiverades stödjande immunceller kallade mikroglia och astrocyter, och inflammatoriska molekyler ökade. Men dessa reaktioner var mycket starkare i luktkroppen. Där började dopaminproducerande neuroner — celler som använder samma signalsubstans som är inblandad i Parkinsons — att dö tidigt och fortsatte att minska under veckor. I kontrast förblev dopamincellerna i substantia nigra i stort sett intakta tills mycket senare, när förluster slutligen uppträdde. Denna stegvisa skada speglar den kliniska bilden: tidiga problem i luktkretsarna, följt av senare skada på de celler som kontrollerar rörelse.
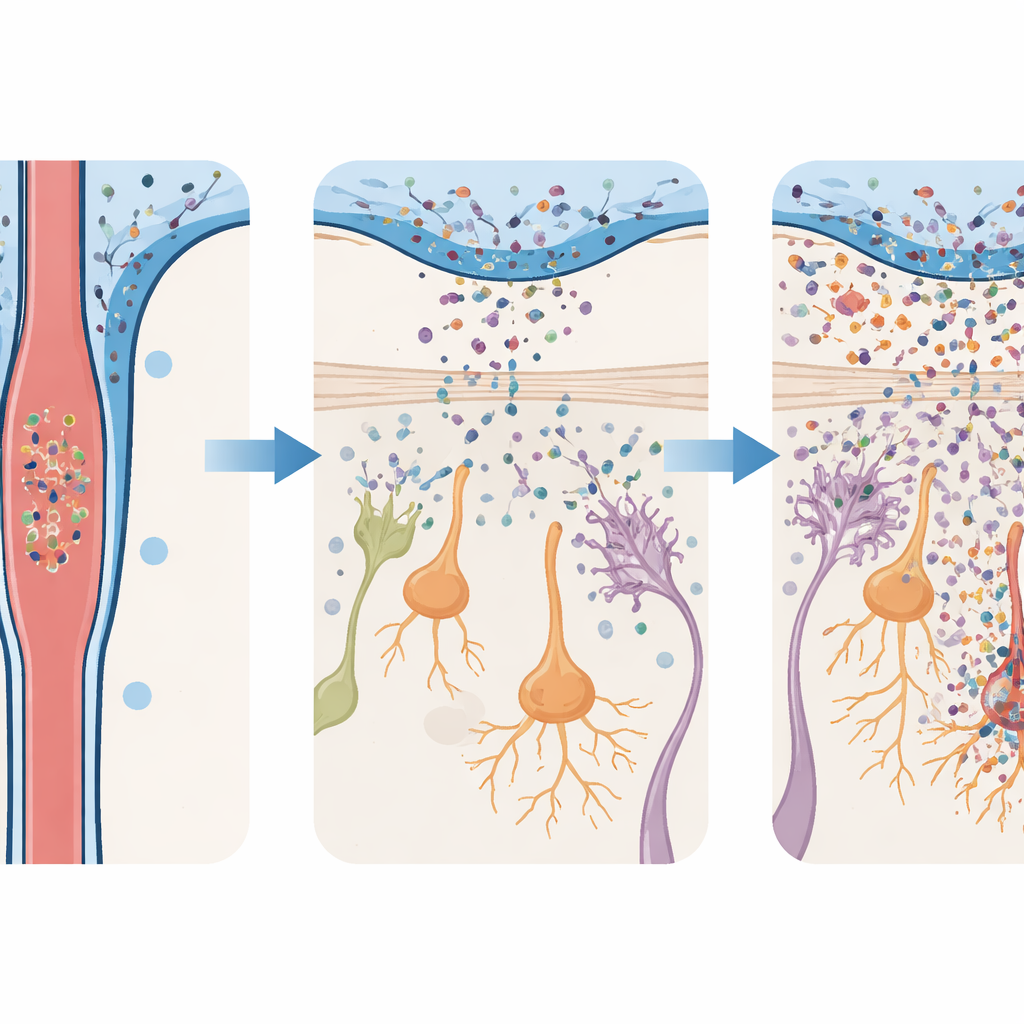
Tidiga luktproblem och sena rörelsestörningar
Beteendeförändringarna hos mössen följde samma tidslinje som de cellulära skadorna. Djur som fick alfa‑synuklein‑oligomerer utvecklade snabbt svårigheter att hitta gödd mat med hjälp av lukten, visade mindre intresse för attraktiva dofter som honmusurin och hade mindre benägenhet att undvika obehagliga lukter. Dessa luktbaserade underskott framträdde inom dagar och kvarstod i nästan två månader. Samma möss gick dock, balanserade och samordnade normalt i standardtester av motorik tills betydligt senare, när tydliga motoriska svårigheter slutligen dök upp. Viktigt är att när forskarna sänkte dosen av injicerade oligomerer visade luktkroppen mycket mindre inflammation och neuronförlust, och djuren behöll i stor utsträckning normala luktsinne. Denna doskänslighet tyder på att bördan av giftigt protein i CSF direkt påverkar hur mycket tidig skada som uppstår.
Vad detta innebär för framtida behandlingar
Tillsammans stöder fynden en ny syn på Parkinsons sjukdom där giftiga alfa‑synuklein‑oligomerer i CSF gör mer än att bara signalera pågående skada — de sprider aktivt skadan genom att flöda tillbaka in i hjärnan längs perivaskulära kanaler. Eftersom luktkroppen tar emot en större andel av detta inflöde, drabbas den tidigare och hårdare, vilket förklarar varför förlust av lukt kan föregå tremor och stelhet med flera år. Avgörande är att arbetet även antyder en interventionsmöjlighet: om vi säkert kan minska eller avlägsna dessa oligomerer från CSF — genom filtreringsenheter, riktade antikroppar eller andra ”CSF‑rensande” strategier — kan vi kanske skydda sårbara regioner som luktkroppen och bromsa hela kaskaden av Parkinson‑liknande patologi.
Citering: Zhu, WX., He, XZ., Meng, JC. et al. Perivascular spread of CSF-derived α-synuclein oligomers drives region-specific Parkinson’s-like pathology. npj Parkinsons Dis. 12, 84 (2026). https://doi.org/10.1038/s41531-026-01300-3
Nyckelord: Parkinsons sjukdom, alfa‑synuklein, cerebrospinalvätska, glymfatiskt system, luktsvikt