Clear Sky Science · pt
Propagação perivascular de oligômeros de α-sinucleína derivados do LCR impulsiona patologia semelhante à de Parkinson em regiões específicas
Por que isso importa para a doença de Parkinson
Muitas pessoas pensam na doença de Parkinson como um distúrbio do movimento, marcado por tremor e rigidez. Mas anos antes desses problemas motores aparecerem, muitos pacientes perdem o olfato. Este estudo faz uma pergunta simples, porém poderosa: proteínas tóxicas flutuando no fluido que banha o cérebro poderiam iniciar a doença em regiões relacionadas ao olfato, muito antes de atingirem centros motores? Ao rastrear como essas proteínas se deslocam e que danos causam em camundongos, os pesquisadores descobrem um sistema de circulação oculto que pode impulsionar a progressão passo a passo do Parkinson — e apontam para uma maneira inesperada de retardá‑la.
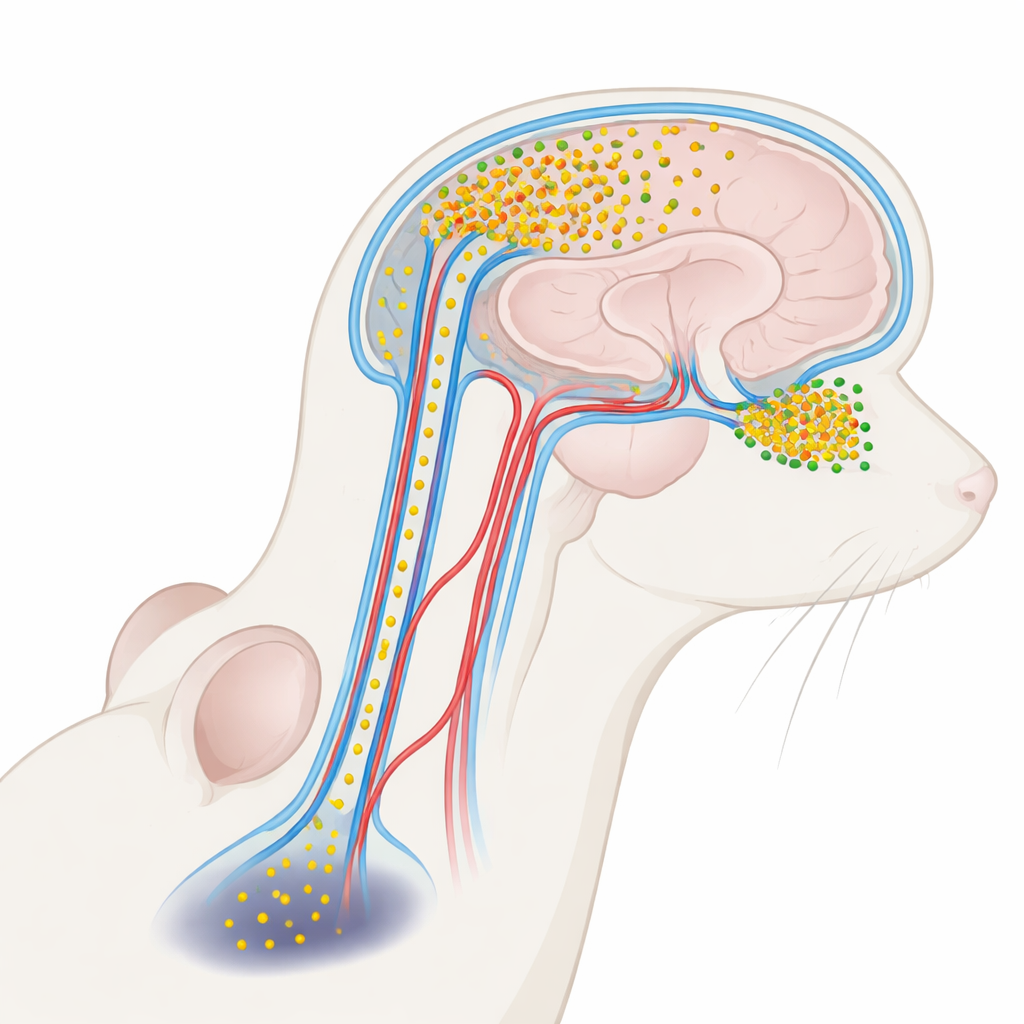
Uma proteína prejudicial transportada pelo fluido cerebral
A doença de Parkinson está fortemente associada a uma proteína chamada alfa‑sinucleína. Em cérebros saudáveis, ela auxilia na comunicação entre neurônios. Em condições de doença, no entanto, alfa‑sinucleína pode se agrupar em pequenos agregados solúveis chamados oligômeros, que são especialmente tóxicos para os neurônios. Esses oligômeros aparecem em níveis mais altos no líquido claro que banha o cérebro e a medula espinhal — o líquido cefalorraquidiano (LCR) — de pessoas com Parkinson. Até agora, a maioria dos estudos tratou a alfa‑sinucleína no LCR como um marcador útil da doença, e não como um agente ativo. Os autores deste trabalho perguntaram se esses oligômeros presentes no LCR poderiam, na verdade, infiltrar‑se de volta no cérebro e lesar regiões específicas, ajudando a explicar por que problemas olfativos surgem cedo enquanto distúrbios motores aparecem depois.
O encanamento do cérebro e um centro olfativo vulnerável
O LCR não apenas amortece o cérebro; ele circula por uma rede de canais ao longo dos vasos sanguíneos conhecidos como espaços perivasculares, parte de um sistema mais amplo de remoção “glicemática”. Usando marcadores fluorescentes e microscópios tridimensionais avançados, os pesquisadores injetaram alfa‑sinucleína marcada no LCR de camundongos e observaram para onde ela ia. Eles descobriram que a proteína entrou no cérebro por essas rotas perivasculares e se acumulou de forma muito desigual. O bulbo olfatório — a pequena estrutura na frente do cérebro que processa odores — absorveu muito mais da proteína do que regiões mais profundas, como a substância negra, que controla o movimento. Mesmo dentro do próprio bulbo olfatório, algumas subregiões mostraram influxo mais intenso que outras, sugerindo uma vulnerabilidade em detalhes finos moldada pelo fluxo local de fluido e pela disposição dos vasos.
Do influxo silencioso à inflamação e perda neuronal
Para testar o que esse influxo provoca, a equipe infundiu camundongos com oligômeros tóxicos de alfa‑sinucleína e examinou seus cérebros ao longo do tempo. Tanto no bulbo olfatório quanto na substância negra, células de suporte imune chamadas microglia e astrócitos foram ativadas, e moléculas inflamatórias aumentaram. Mas essas reações foram muito mais intensas no bulbo olfatório. Ali, neurônios produtores de dopamina — células que utilizam o mesmo mensageiro químico implicado no Parkinson — começaram a morrer cedo e continuaram a declinar por semanas. Em contraste, os neurônios dopaminérgicos na substância negra permaneceram em grande parte intactos até bem mais tarde, quando perdas finalmente apareceram. Esse dano em estágios reflete o quadro clínico: problemas precoces na via olfativa, seguidos de lesão posterior nas células que controlam o movimento.
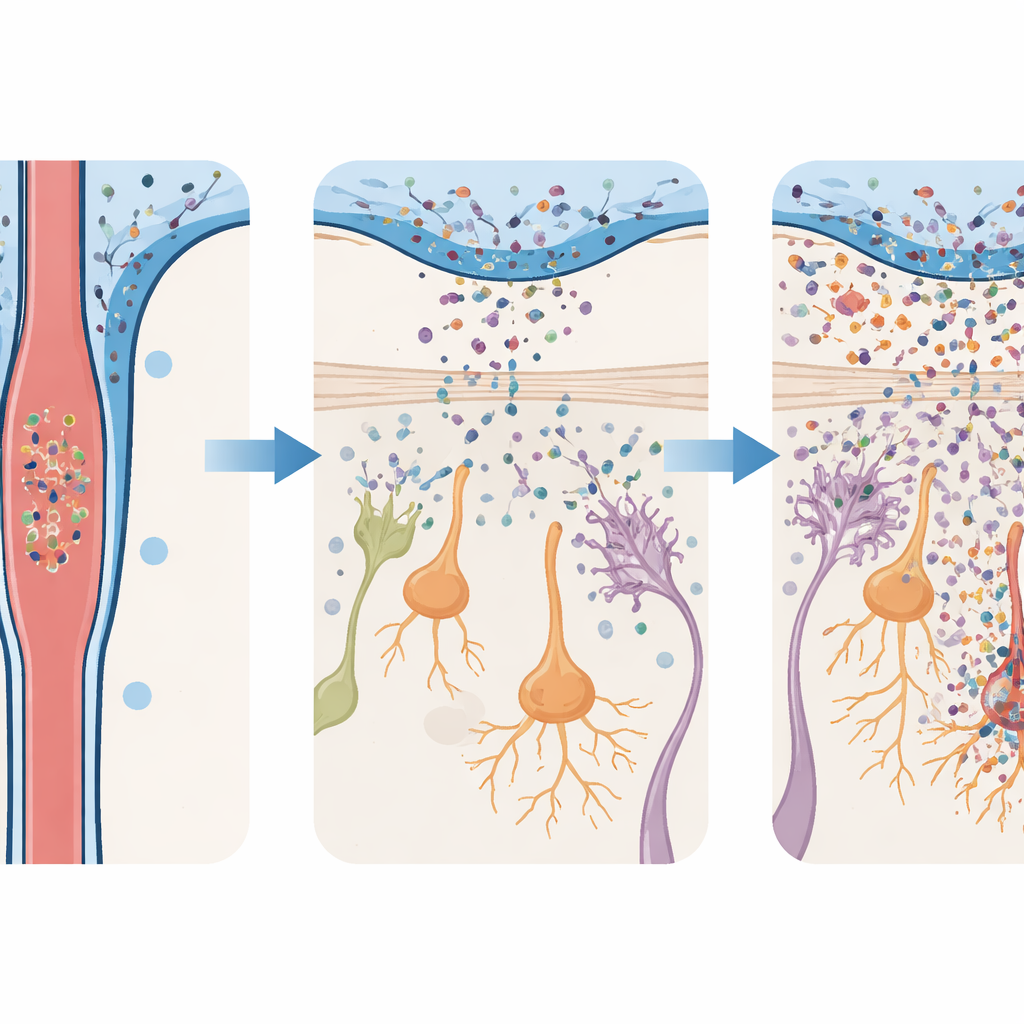
Problemas olfativos precoces e questões motoras tardias
As alterações comportamentais nos camundongos seguiram o mesmo cronograma que os danos celulares. Os animais expostos a oligômeros de alfa‑sinucleína rapidamente apresentaram dificuldade em encontrar alimentos escondidos pelo olfato, mostraram menos interesse por odores atrativos como urina de fêmea e estavam menos inclinados a evitar cheiros desagradáveis. Esses déficits olfativos surgiram em dias e persistiram por quase dois meses. Ainda assim, os mesmos camundongos caminharam, se equilibraram e se coordenaram normalmente em testes padrão de movimento até muito mais tarde, quando dificuldades motoras claras finalmente surgiram. Importante: quando os pesquisadores reduziram a dose de oligômeros injetados, o bulbo olfatório mostrou muito menos inflamação e perda neuronal, e os animais em grande parte mantiveram habilidades olfativas normais. Essa sensibilidade à dose sugere que o fardo de proteína tóxica no LCR molda diretamente a quantidade de dano precoce que ocorre.
O que isso significa para tratamentos futuros
Em conjunto, os achados sustentam uma nova visão da doença de Parkinson na qual oligômeros tóxicos de alfa‑sinucleína no LCR fazem mais do que sinalizar dano em curso — eles o espalham ativamente ao fluir de volta para o cérebro por canais perivasculares. Como o bulbo olfatório recebe uma fração maior desse influxo, sofre lesões mais cedo e mais graves, o que explica por que a perda do olfato pode preceder tremor e rigidez por anos. O trabalho é, crucialmente, sugestivo de uma intervenção: se pudermos reduzir ou remover com segurança esses oligômeros do LCR — por meio de dispositivos de filtração, anticorpos direcionados ou outras estratégias de "limpeza do LCR" — poderíamos proteger regiões vulneráveis como o bulbo olfatório e desacelerar toda a cascata de patologia semelhante ao Parkinson.
Citação: Zhu, WX., He, XZ., Meng, JC. et al. Perivascular spread of CSF-derived α-synuclein oligomers drives region-specific Parkinson’s-like pathology. npj Parkinsons Dis. 12, 84 (2026). https://doi.org/10.1038/s41531-026-01300-3
Palavras-chave: Doença de Parkinson, alfa-sinucleína, líquido cefalorraquidiano, sistema glicemático, disfunção olfativa