Clear Sky Science · ru
Перивазальное распространение олигомеров α‑синуклеина из спинномозговой жидкости вызывает регион‑специфическую патологию, подобную болезни Паркинсона
Почему это важно для болезни Паркинсона
Болезнь Паркинсона многие считают двигательным расстройством, характеризующимся тремором и скованностью. Но за годы до появления этих моторных симптомов у многих пациентов ухудшается обоняние. В этом исследовании поставлен простой, но мощный вопрос: могут ли токсичные белки, плавающие в прозрачной «ванночке» мозга, запускать заболевание в областях, связанных с обонянием, задолго до поражения центров движения? Отслеживая, как эти белки перемещаются и какой вред наносят у мышей, авторы раскрывают скрытую «водопроводную» систему, которая может приводить к поэтапному прогрессированию болезни Паркинсона — и указывают на неожиданный путь для её замедления.
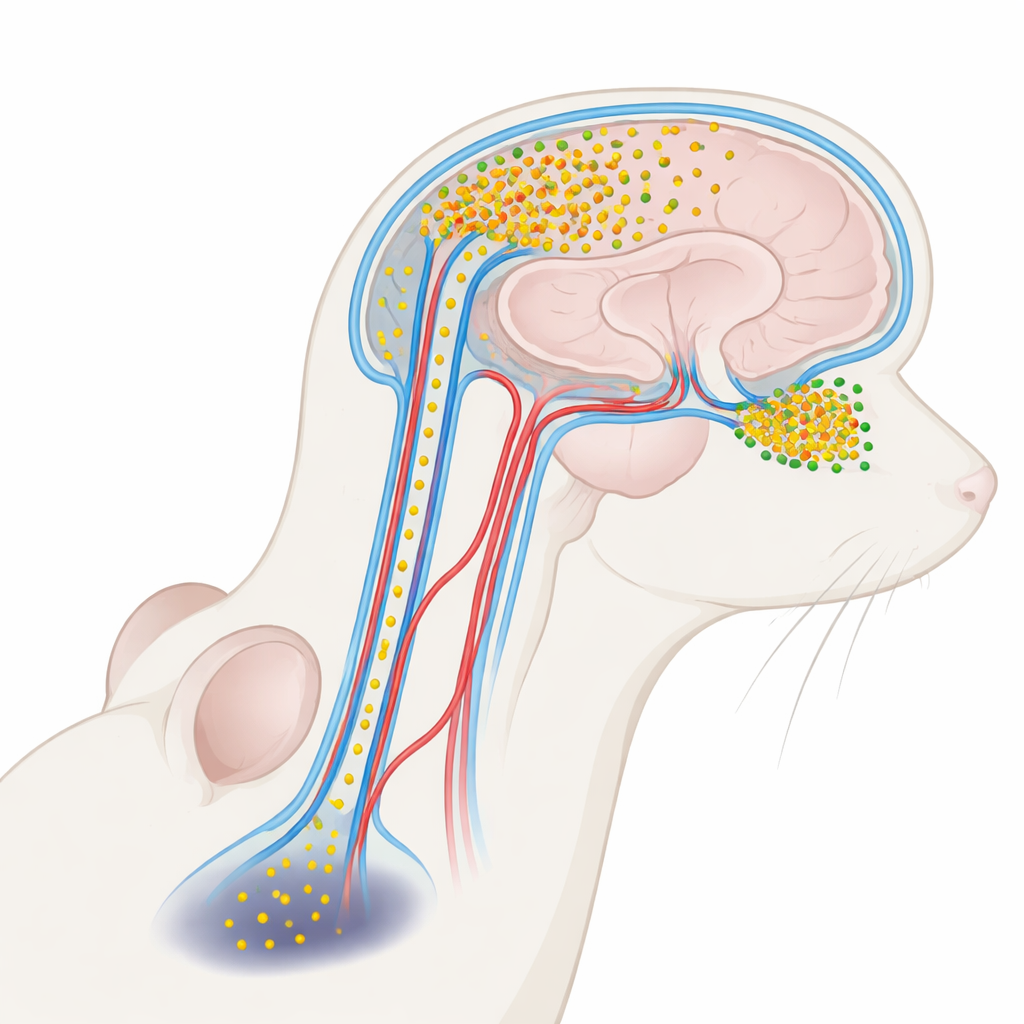
Вредный белок, плывущий в цереброспинальной жидкости
Болезнь Паркинсона тесно связана с белком, называемым альфа‑синуклеином. В здоровом мозге он помогает нейронам общаться. При болезненных состояниях однако альфа‑синуклеин может собираться в малые растворимые кластеры — олигомеры, которые особенно токсичны для нейронов. Эти олигомеры обнаруживаются в повышенных концентрациях в прозрачной жидкости, омывающей мозг и спинной мозг — цереброспинальной жидкости (ЦСЖ) — у людей с болезнью Паркинсона. До настоящего времени большинство работ рассматривали альфа‑синуклеин в ЦСЖ как маркер болезни, а не как активного участника. Авторы этой статьи задали вопрос, не могут ли олигомеры в ЦСЖ на самом деле проникать обратно в мозг и повреждать отдельные регионы, помогая объяснить, почему нарушения обоняния появляются рано, а моторные проблемы — позже.
«Водопровод» мозга и уязвимый центр обоняния
ЦСЖ не только амортизирует мозг; она циркулирует по сети каналов вдоль кровеносных сосудов, известных как перивазальные пространства, которые входят в состав более широкой «глимфатической» системы очистки. Используя светящиеся метки и продвинутую трёхмерную микроскопию, исследователи вводили меченый альфа‑синуклеин в ЦСЖ мышей и наблюдали за его перемещением. Они обнаружили, что белок входил в мозг по этим перивазальным путям и накапливался очень неравномерно. Обонятельная луковица — небольшая структура в передней части мозга, обрабатывающая запахи — впитывала значительно больше поступающего белка, чем более глубокие области, такие как чёрная субстанция (substantia nigra), контролирующая движение. Даже внутри самой обонятельной луковицы некоторые субрегионы демонстрировали более сильный приток, чем другие, что указывает на тонкую уязвимость, определяемую локальными потоками жидкости и расположением сосудов.
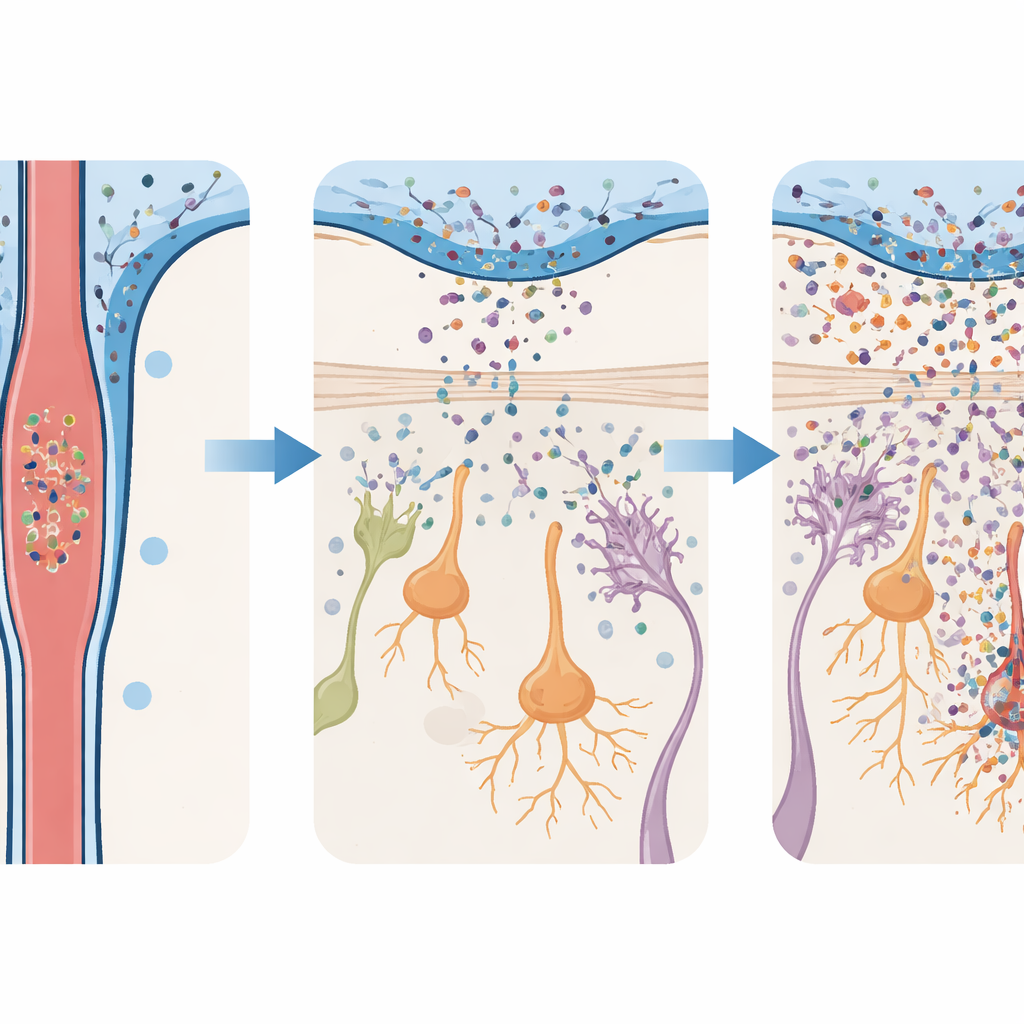
От безмолвного притока к воспалению и гибели нейронов
Чтобы проверить последствия этого притока, команда инфузировала мышей токсичными олигомерами альфа‑синуклеина и исследовала их мозг в динамике. В обонятельной луковице и в чёрной субстанции активировались клетки поддержки иммунной системы — микроглия и астроциты — и повышался уровень провоспалительных молекул. Но эти реакции были значительно сильнее в обонятельной луковице. Там дофаминергические нейроны — клетки, использующие тот же нейромедиатор, причастный к болезни Паркинсона — начали гибнуть рано и продолжали сокращаться в течение недель. В то же время дофаминергические нейроны в чёрной субстанции оставались в основном интактными до более поздних сроков, когда потери стали заметными. Такое поэтапное повреждение отражает клиническую картину: ранние нарушения в цепях обоняния, за которыми следуют более поздние повреждения клеток, контролирующих движение.
Ранние проблемы с обонянием и поздние моторные нарушения
Поведенческие изменения у мышей повторяли ту же временную последовательность, что и клеточные повреждения. Животные, получавшие олигомеры альфа‑синуклеина, быстро стали хуже находить скрытую пищу по запаху, проявляли меньший интерес к привлекательным запахам, таким как моча самки, и были менее склонны избегать неприятных запахов. Эти нарушения обоняния появились в течение нескольких дней и сохранялись почти два месяца. В то же время те же мыши сохраняли нормальную ходьбу, равновесие и координацию при стандартных тестах движения до гораздо более позднего времени, когда появилась выраженная моторная дисфункция. Важно, что при снижении дозы вводимых олигомеров в обонятельной луковице наблюдалось значительно меньше воспаления и гибели нейронов, и животные в основном сохраняли нормальные обонятельные способности. Эта зависимость от дозы указывает на то, что нагрузка токсического белка в ЦСЖ напрямую определяет степень раннего повреждения.
Что это значит для будущего лечения
В совокупности результаты поддерживают новую модель болезни Паркинсона, в которой токсичные олигомеры альфа‑синуклеина в ЦСЖ делают больше, чем просто служат маркером повреждения — они активно распространяют его, возвращаясь в мозг по перивазальным каналам. Поскольку обонятельная луковица получает более сильную долю этого притока, она подвергается раннему и более тяжёлому повреждению, что объясняет, почему потеря обоняния может предшествовать тремору и скованности на годы. Критически важно, что работа также намекает на возможное вмешательство: если мы сможем безопасно уменьшить или удалить эти олигомеры из ЦСЖ — с помощью фильтрации, таргетных антител или других стратегий «очищения ЦСЖ» — мы сможем защитить уязвимые регионы, такие как обонятельная луковица, и замедлить всю цепочку патологических процессов, похожих на болезнь Паркинсона.
Цитирование: Zhu, WX., He, XZ., Meng, JC. et al. Perivascular spread of CSF-derived α-synuclein oligomers drives region-specific Parkinson’s-like pathology. npj Parkinsons Dis. 12, 84 (2026). https://doi.org/10.1038/s41531-026-01300-3
Ключевые слова: Болезнь Паркинсона, альфа‑синуклеин, спинномозговая жидкость, глимфатическая система, нарушение обоняния